3. Физические свойства веществ. Агрегатное состояние. Агрегатное состояние углекислого газа
Газообразные вещества: примеры и свойства
На сегодняшний день известно о существовании более чем 3 миллионов различных веществ. И цифра эта с каждым годом растет, так как химиками-синтетиками и другими учеными постоянно производятся опыты по получению новых соединений, обладающих какими-либо полезными свойствами.
Часть веществ - это природные обитатели, формирующиеся естественным путем. Другая половина - искусственные и синтетические. Однако и в первом и во втором случае значительную часть составляют газообразные вещества, примеры и характеристики которых мы и рассмотрим в данной статье.

Агрегатные состояния веществ
С XVII века принято было считать, что все известные соединения способны существовать в трех агрегатных состояниях: твердые, жидкие, газообразные вещества. Однако тщательные исследования последних десятилетий в области астрономии, физики, химии, космической биологии и прочих наук доказали, что есть еще одна форма. Это плазма.
Что она собой представляет? Это частично или полностью ионизированные газы. И оказывается, таких веществ во Вселенной подавляющее большинство. Так, именно в состоянии плазмы находятся:
- межзвездное вещество;
- космическая материя;
- высшие слои атмосферы;
- туманности;
- состав многих планет;
- звезды.
Поэтому сегодня говорят, что существуют твердые, жидкие, газообразные вещества и плазма. Кстати, каждый газ можно искусственно перевести в такое состояние, если подвергнуть его ионизации, то есть заставить превратиться в ионы.
Газообразные вещества: примеры
Примеров рассматриваемых веществ можно привести массу. Ведь газы известны еще с XVII века, когда ван Гельмонт, естествоиспытатель, впервые получил углекислый газ и стал исследовать его свойства. Кстати, название этой группе соединений также дал он, так как, по его мнению, газы - это нечто неупорядоченное, хаотичное, связанное с духами и чем-то невидимым, но ощутимым. Такое имя прижилось и в России.
Можно классифицировать все газообразные вещества, примеры тогда привести будет легче. Ведь охватить все многообразие сложно.
По составу различают:
- простые,
- сложные молекулы.
К первой группе относятся те, что состоят из одинаковых атомов в любом их количестве. Пример: кислород - О2, озон - О3, водород - Н2, хлор - CL2, фтор - F2, азот - N2 и прочие.
Ко второй категории следует относить такие соединения, в состав которых входит несколько атомов. Это и будут газообразные сложные вещества. Примерами служат:
- сероводород - h3S;
- хлороводород - HCL;
- метан - Ch5;
- сернистый газ - SO2;
- бурый газ - NO2;
- фреон - CF2CL2;
- аммиак - Nh4 и прочие.
Классификация по природе веществ
Также можно классифицировать виды газообразных веществ по принадлежности к органическому и неорганическому миру. То есть по природе входящих в состав атомов. Органическими газами являются:
- первые пять представителей предельных углеводородов (метан, этан, пропан, бутан, пентан). Общая формула Cnh3n+2;
- этилен - С2Н4;
- ацетилен или этин - С2Н2;
- метиламин - Ch4Nh3 и другие.
К категории газов неорганической природы относятся хлор, фтор, аммиак, угарный газ, силан, веселящий газ, инертные или благородные газы и прочие.
Еще одной классификацией, которой можно подвергнуть рассматриваемые соединения, является деление на основе входящих в состав частиц. Именно из атомов состоят не все газообразные вещества. Примеры структур, в которых присутствуют ионы, молекулы, фотоны, электроны, броуновские частицы, плазма, также относятся к соединениям в таком агрегатном состоянии.
Свойства газов
Характеристики веществ в рассматриваемом состоянии отличаются от таковых для твердых или жидких соединений. Все дело в том, что свойства газообразных веществ особенные. Частицы их легко и быстро подвижны, вещество в целом изотропное, то есть свойства не определяются направлением движения входящих в состав структур.
Можно обозначить самые главные физические свойства газообразных веществ, которые и будут отличать их от всех остальных форм существования материи.
- Это такие соединения, которые нельзя увидеть и проконтролировать, ощутить обычными человеческими способами. Чтобы понять свойства и идентифицировать тот или иной газ, опираются на четыре описывающих их все параметра: давление, температура, количество вещества (моль), объем.
- В отличие от жидкостей газы способны занимать все пространство без остатка, ограничиваясь лишь величиной сосуда или помещения.
- Все газы между собой легко смешиваются, при этом у этих соединений нет поверхности раздела.
- Существуют более легкие и тяжелые представители, поэтому под действием силы тяжести и времени, возможно увидеть их разделение.
- Диффузия - одно из важнейших свойств этих соединений. Способность проникать в другие вещества и насыщать их изнутри, совершая при этом совершенно неупорядоченные движения внутри своей структуры.
- Реальные газы электрический ток проводить не могут, однако если говорить о разреженных и ионизированный субстанциях, то проводимость резко возрастает.
- Теплоемкость и теплопроводность газов невысока и колеблется у разных видов.
- Вязкость возрастает с увеличением давления и температуры.
- Существует два варианта межфазового перехода: испарение - жидкость превращается в пар, сублимация - твердое вещество, минуя жидкое, становится газообразным.
Отличительная особенность паров от истинных газов в том, что первые при определенных условиях способны перейти в жидкость или твердую фазу, а вторые нет. Также следует заметить способность рассматриваемых соединений сопротивляться деформациям и быть текучими.

Подобные свойства газообразных веществ позволяют широко применять их в самых различных областях науки и техники, промышленности и народном хозяйстве. К тому же конкретные характеристики являются для каждого представителя строго индивидуальными. Мы же рассмотрели лишь общие для всех реальных структур особенности.
Сжимаемость
При разных температурах, а также под влиянием давления газы способны сжиматься, увеличивая свою концентрацию и снижая занимаемый объем. При повышенных температурах они расширяются, при низких - сжимаются.
Под действием давления также происходят изменения. Плотность газообразных веществ увеличивается и, при достижении критической точки, которая для каждого представителя своя, может наступить переход в другое агрегатное состояние.
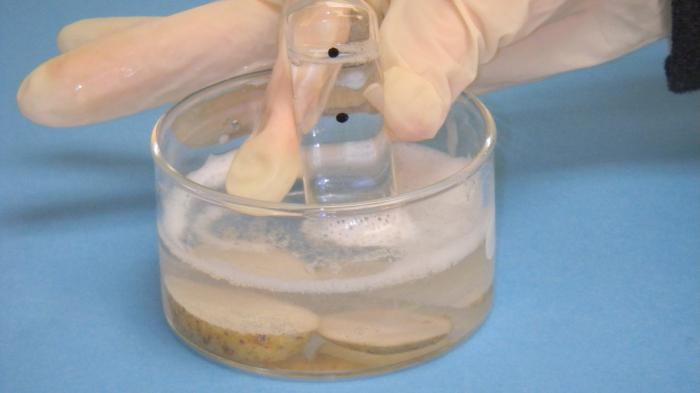
Основные ученые, внесшие вклад в развитие учения о газах
Таких людей можно назвать множество, ведь изучение газов - процесс трудоемкий и исторически долгий. Остановимся на самых известных личностях, сумевших сделать наиболее значимые открытия.
- Амедео Авогадро в 1811 году сделал открытие. Неважно, какие газы, главное, что при одинаковых условиях их в одном объеме их содержится равное количество по числу молекул. Существует рассчитанная величина, имеющая название по фамилии ученого. Она равна 6,03*1023 молекул для 1 моль любого газа.
- Ферми - создал учение об идеальном квантовом газе.
- Гей-Люссак, Бойль-Мариотт - фамилии ученых, создавших основные кинетические уравнения для расчетов.
- Роберт Бойль.
- Джон Дальтон.
- Жак Шарль и многие другие ученые.
Строение газообразных веществ
Самая главная особенность в построении кристаллической решетки рассматриваемых веществ, это то, что в узлах ее либо атомы, либо молекулы, которые соединяются друг с другом слабыми ковалентными связями. Также присутствуют силы ван-дер-ваальсового взаимодействия, когда речь идет о ионах, электронах и других квантовых системах.
Поэтому основные типы строения решеток для газов, это:
- атомная;
- молекулярная.
Связи внутри легко рвутся, поэтому эти соединения не имеют постоянной формы, а заполняют весь пространственный объем. Это же объясняет отсутствие электропроводности и плохую теплопроводность. А вот теплоизоляция у газов хорошая, ведь, благодаря диффузии, они способны проникать в твердые тела и занимать свободные кластерные пространства внутри них. Воздух при этом не пропускается, тепло удерживается. На этом основано применение газов и твердых тел в совокупности в строительных целях.

Простые вещества среди газов
Какие по строению и структуре газы относятся к данной категории, мы уже оговаривали выше. Это те, что состоят из одинаковых атомов. Примеров можно привести много, ведь значительная часть неметаллов из всей периодической системы при обычных условиях существует именно в таком агрегатном состоянии. Например:
Молекулы этих газов могут быть как одноатомными (благородные газы), так и многоатомными (озон - О3). Тип связи - ковалентная неполярная, в большинстве случаев достаточно слабая, но не у всех. Кристаллическая решетка молекулярного типа, что позволяет этим веществам легко переходить из одного агрегатного состояния в другое. Так, например, йод при обычных условиях - темно-фиолетовые кристаллы с металлическим блеском. Однако при нагревании сублимируются в клубы ярко-фиолетового газа - I2.

К слову сказать, любое вещество, в том числе металлы, при определенных условиях могут существовать в газообразном состоянии.
Сложные соединения газообразной природы
Таких газов, конечно, большинство. Различные сочетания атомов в молекулах, объединенные ковалентными связями и ван-дер-ваальсовыми взаимодействиями, позволяют сформироваться сотням различных представителей рассматриваемого агрегатного состояния.
Примерами именно сложных веществ среди газов могут быть все соединения, состоящие из двух и более разных элементов. Сюда можно отнести:
- пропан;
- бутан;
- ацетилен;
- аммиак;
- силан;
- фосфин;
- метан;
- сероуглерод;
- сернистый газ;
- бурый газ;
- фреон;
- этилен и прочие.
Кристаллическая решетка молекулярного типа. Многие из представителей легко растворяются в воде, образуя соответствующие кислоты. Большая часть подобных соединений - важная часть химических синтезов, осуществляемых в промышленности.
Метан и его гомологи
Иногда общим понятием "газ" обозначают природное полезное ископаемое, которое представляет собой целую смесь газообразных продуктов преимущественно органической природы. Именно он содержит такие вещества, как:
- метан;
- этан;
- пропан;
- бутан;
- этилен;
- ацетилен;
- пентан и некоторые другие.
В промышленности они являются очень важными, ведь именно пропан-бутановая смесь - это бытовой газ, на котором люди готовят пищу, который используется в качестве источника энергии и тепла.

Многие из них используются для синтеза спиртов, альдегидов, кислот и прочих органических веществ. Ежегодное потребление природного газа исчисляется триллионами кубометров, и это вполне оправданно.
Кислород и углекислый газ
Какие вещества газообразные можно назвать самыми широко распространенными и известными даже первоклассникам? Ответ очевиден - кислород и углекислый газ. Ведь это они являются непосредственными участниками газообмена, происходящего у всех живых существ на планете.
Известно, что именно благодаря кислороду возможна жизнь, так как без него способны существовать только некоторые виды анаэробных бактерий. А углекислый газ - необходимый продукт "питания" для всех растений, которые поглощают его с целью осуществления процесса фотосинтеза.
С химической точки зрения и кислород, и углекислый газ - важные вещества для проведения синтезов соединений. Первый является сильным окислителем, второй чаще восстановитель.
Галогены
Это такая группа соединений, в которых атомы - это частицы газообразного вещества, соединенные попарно между собой за счет ковалентной неполярной связи. Однако не все галогены - газы. Бром - это жидкость при обычных условиях, а йод - легко возгоняющееся твердое вещество. Фтор и хлор - ядовитые опасные для здоровья живых существ вещества, которые являются сильнейшими окислителями и используются в синтезах очень широко.
fb.ru
Газы (агрегатное состояние вещества) | Авторская платформа Pandia.ru
Газы (французское gaz; название предложено голланским учёным Я. Б. Гельмонтом), агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь предоставленный им объём. Вещество в газообразном состоянии широко распространено в природе. Г. образуют атмосферу Земли, в значительных количествах содержатся в твёрдых земных породах, растворены в воде океанов, морей и рек. Солнце, звёзды, облака межзвёздного вещества состоят из Г. — нейтральных или ионизованных (плазмы). Встречающиеся в природных условиях Г. представляют собой, как правило, смеси химически индивидуальных Г.
Г. обладают рядом характерных свойств. Они полностью заполняют сосуд, в котором находятся, и принимают его форму. В отличие от твёрдых тел и жидкостей, объём Г. существенно зависит от давления и температуры. Коэффициент объёмного расширения Г. в обычных условиях (0—100°С) на два порядка выше, чем у жидкостей, и составляет в среднем 0,003663 град-1. В табл. приведены данные о физических свойствах наиболее распространённых Г.
Любое вещество можно перевести в газообразное состояние надлежащим подбором давления и температуры. Поэтому возможную область существования газообразного состояния графически удобно изобразить в переменных: давление р — температура Т (в р, Т-диаграмме, рис. 1). При температурах ниже критической Тк (см. Критическое состояние) эта область ограничена кривыми сублимации (возгонки) / и парообразования II. Это означает, что при любом давлении ниже критического рк существует температура Т (см. рис. 1), определяемая кривой сублимации или парообразования, выше которой вещество становится газообразным. В состояниях на кривой 1 (ниже тройной точки Tp) газ находится в равновесии с твёрдым веществом (твёрдой фазой), а на кривой II (между тройной и критической точкой К.) — с жидкой фазой. Газ в этих состояниях обычно называют паром вещества.
При Т > Тк граница газообразной области условна, поскольку при этих температурах фазовые превращения не происходят. В ряде случаев за условную границу между Г. и жидкостью при сверхкритических температурах и давлениях принимают критическую изохору вещества (кривую постоянной плотности или удельного объёма, см. рис. 1), в непосредственной близости от которой свойства вещества изменяются, хотя и не скачком, но особенно быстро.
В связи с тем что область газового состояния очень обширна, свойства Г. при изменении температуры и давления могут меняться в широких пределах. Так, в нормальных условиях (при 0° С и атмосферном давлении) плотность Г. примерно в 1000 раз меньше плотности того же вещества в твёрдом или жидком состоянии. При комнатной температуре, но давлении, в 1017 раз меньшем атмосферного (предел, достигнутый современной вакуумной техникой), плотность Г. составляет около 10 -20 г/см3. В космических условиях плотность Г. может быть ещё на 10 порядков меньше (~10-30/см3).
С другой стороны, при высоких давлениях вещество, которое при сверхкритических температурах можно считать Г., обладает огромной плотностью (например, в центре некоторых звёзд ~109 г/см3). В зависимости от условий в широких пределах изменяются и др. свойства Г. — теплопроводность, вязкость и т. д.
Молекулярно-кинетическая теория Г. Молекулярно-кинетическая теория рассматривает Г. как совокупность слабо взаимодействующих частиц (молекул или атомов), находящихся в непрерывном хаотическом (тепловом) движении. На основе этих простых представлений кинетической теории удаётся объяснить основные физические свойства Г., особенно полно — свойства разреженных Г.
У достаточно разреженных Г. средние расстояния между молекулами оказываются значительно больше радиуса действия межмолекулярных сил. Так, например, при нормальных условиях в 1 см3 Г. находится~ 1019 молекул и среднее расстояние между ними составляет ~ 10-6 см, или ~ 100 , тогда как межмолекулярное взаимодействие не существенно на расстояниях свыше 5—10 . Следовательно, в таких условиях молекулы взаимодействуют лишь при сближении на расстояние действия межмолекулярных сил. Такое сближение принято трактовать как столкновение молекул. Радиус действия межмолекулярных сил в рассмотренном примере в 10—20 раз меньше среднего расстояния между молекулами, так что общий объём, в котором эти силы могут сказываться (как бы «собственный объём» всех молекул), составляет 10-3—10-4 от полного объёма Г. Это позволяет считать собственный объём молекул Г. в нормальных условиях пренебрежимо малым и рассматривать молекулы как материальные точки. Газ, молекулы которого рассматриваются как не взаимодействующие друг с другом материальные точки, называется идеальным. При тепловом равновесии идеального Г. все направления движения его молекул равновероятны, а скорости распределены в соответствии с Максвелла распределением. На рис. 2 приведён график этого распределения для азота при температурах 20 и 500°С. Из графика видно, что подавляющее большинство молекул имеет близкие значения скорости (максимум кривой соответствует скорости наиболее вероятной при данной температуре), но существует также известная часть молекул с малыми и очень большими скоростями. При помощи максвелловского распределения может быть определена т. н. средняя квадратичная скорость молекул связанная с температурой Т газа соотношением
Здесь k — Больцмана постоянная, m — масса молекулы. Уравнение (1) позволяет установить связь между средней кинетической энергией одной молекулы и температурой газа:
Эту зависимость часто рассматривают как молекулярно-кинетическое толкование температуры — температура есть мера кинетической энергии молекул.
Поскольку молекулы идеального Г. обладают лишь кинетической энергией, внутренняя энергия такого Г. не зависит от занимаемого им объёма (закон Джоуля).
Молекулярно-кинетическая теория рассматривает давление Г. на стенки сосуда, в котором он находится, как воздействие ударов молекул, усреднённое по поверхности и времени. Количественно давление р определяется импульсом, передаваемым молекулами в единицу времени единице площади стенки:
где n — число молекул в единице объёма. Уравнения (2) и (3) позволяют записать уравнение состояния идеального Г. в виде
p = nkT. (4)
уравнение (4), записанное для 1 моля Г., содержащего N = 6,023- 1023 молекул (см. Авогадро число), называют Клапейрона уравнением:
pv = RT. (5)
Здесь R = kN — универсальная газовая постоянная, v — объём, приходящийся на 1 моль. уравнение Клапейрона обобщает эмпирические газовые законы Бойля — Мариотта и Гей-Люссака (см. Бойля — Мариотта закон, Гей-Люссака законы). Из уравнения (5) следует также, что при одинаковых температуре и давлении идеальные Г., взятые в количестве 1 моля, имеют равные объёмы и в любом таком Г. в единице объёма содержится равное количество молекул (см. Авогадро закон).
В условиях теплового равновесия температура и давление Г. по всему его объёму одинаковы, молекулы движутся хаотично, в Г. нет упорядоченных потоков. Возникновение в Г. перепадов (градиентов) температуры или давления приводит к нарушению равновесия и переносу в направлении градиента энергии, массы или др. физических величин.
Кинетические свойства Г. — теплопроводность, диффузию, вязкость — молекулярно-кинетическая теория рассматривает с единой точки зрения: диффузию как перенос молекулами массы, теплопроводность как перенос ими энергии, вязкость как перенос количества движения. Модель идеального Г. для анализа явлений переноса непригодна, ибо в этих процессах существенную роль играют столкновения молекул (при которых происходит передача какой-нибудь из переносимых величин, например энергии) и «размер» молекул (влияющий на частоту столкновений). Поэтому в простейшем случае явления переноса в Г. рассматриваются для разреженного Г., молекулы которого в первом приближении считаются упругими шариками с определённым диаметром s, причём эти шарики взаимодействуют друг с другом только в момент соударения. В этом приближении диаметр молекулы связан простым соотношением с её средней длиной свободного пробега :
Размер существенно влияет на процессы переноса в разреженном Г. В частности, если характерный размер объёма, занимаемого Г., больше , то теплопроводность и вязкость Г. не зависят от давления. Наоборот, когда больше характерного размера, теплопроводность и вязкость Г. с уменьшением давления (а значит, и числа столкновений) начинают падать. На этом явлении, в частности, основаны теплоизолирующие свойства сосудов с двойными стенками, воздух между которыми откачан (см. Дьюара сосуды).
В более строгой молекулярной теории при анализе явлений переноса в разреженных газах учитывается взаимодействие молекул при любых расстояниях между ними. Характер взаимодействия определяется т. н. потенциалом взаимодействия (см. Межмолекулярное взаимодействие). Строгое рассмотрение динамики парных взаимодействий (столкновений) приводит к тому, что в формулах для расчёта коэффициентов переноса появляются т. н. интегралы столкновений, являющиеся функциями только приведённой температуры T* = kT/e. Эта температура характеризует отношение кинетической энергии молекул (~kT) к их потенциальной энергии (e — глубина потенциальной ямы при данном потенциале взаимодействия). Интегралы столкновений учитывают то обстоятельство, что сталкивающиеся молекулы в зависимости от их кинетической энергии, а значит и температуры Г., могут сближаться на различные расстояния, т. е. как бы изменять свой эффективный размер.
Свойства реальных Г. При повышении плотности изменяются свойства Г., они перестают быть идеальными. Уравнение состояния (5) оказывается неприменимым, т. к. средние расстояния между молекулами Г. становятся сравнимыми с радиусом межмолекулярного взаимодействия. Для описания термодинамических свойств неидеальных, или, как их чаще называют, реальных, Г. пользуются различными уравнениями состояния, имеющими более или менее строгое теоретическое обоснование. Простейшим примером уравнения, которое качественно правильно описывает основные отличия реального Г. от идеального, служит уравнение Ван-дер-Ваальса. Оно учитывает, с одной стороны, существование сил притяжения между молекулами (их действие приводит к уменьшению давления Г.), с другой стороны — сил отталкивания, препятствующих безграничному сжатию Г. (см. Ван-дер-Ваальса уравнение).
К наиболее теоретически обоснованным, во всяком случае для состояний, удалённых от критической точки, относится вириальное уравнение состояния:
Значения вириальных коэффициентов В, С и т. д. определяются соударениями молекул: парными (В), тройными (С) и более высокого порядка для последующих коэффициентов. Существенно, что вириальные коэффициенты являются функциями только температуры.
В Г. малой плотности наиболее вероятны парные столкновения молекул, т. е. для такого Г. в разложении (7) можно пренебречь всеми членами после члена с коэффициента В. В соответствии с температурным изменением В, при т. н. температуре Бойля ТВ (см. Бойля точка) В обращается в нуль, и умеренно плотный Г. ведёт себя как идеальный, т. е. подчиняется уравнению (5). Физически это означает, что при ТВ межмолекулярные силы притяжения и отталкивания практически компенсируют друг друга. Существование межмолекулярного взаимодействия в той или иной степени сказывается на всех свойствах реальных Г. Внутренняя энергия реального Г. оказывается зависящей от его объёма (от расстояний между молекулами), т. к. потенциальная энергия молекул определяется их взаимными расстояниями.
С межмолекулярным взаимодействие связано также изменение температуры реального Г. при протекании его с мало постоянной скоростью через пористую перегородку (этот процесс называется дросселированием). Мерой изменения температуры Г при дросселировании служит Джоуля — Томсона коэффициент который в зависимости от условий может быть положительным (охлаждение Г.), отрицательным (нагрев Г.) либо равным нулю при т. н. температуре инверсии (см. Джоуля — Томсона явление). Эффект охлаждения Г при дросселировании широко применяется в технике как один из методов сжижения газов.
Внутреннее строение молекул Г. слабо влияет на их термические свойства (давление, температуру, плотность и связь между ними). Для этих свойств в первом приближении существенна только молекулярная масса Г. Напротив, калорические свойства Г. (теплоёмкость, энтропия и др.), а также его электрические и магнитные свойства существенно зависят от внутреннего строения молекул. Например, для расчёта (в первом приближении) теплоёмкости Г. при постоянном объёме cv необходимо знать число внутренних степеней свободы молекулы (т. е. число возможных внутренних движений) iвн. В соответствии с равнораспределения законом классической статистической физики на каждую степень свободы молекулы Г. (поступательную, колебательную, вращательную) приходится энергия, равная 1/2 · kT. Отсюда теплоёмкость 1 моля
Для точного расчёта калорических свойств Г. необходимо знать уровни энергии молекулы, сведения о которых в большинстве случаев получают из анализа спектров Г. Для большого числа веществ в состоянии идеального Г. калорические свойства вычислены с высокой точностью и их значения представлены в виде таблиц до температур 10—22 тыс. градусов.
Электрические свойства Г. связаны в первую очередь с возможностью ионизации молекул или атомов, т. е. с появлением в Г. электрически заряженных частиц (ионов и электронов). При отсутствии заряженных частиц Г. являются хорошими диэлектриками. С ростом концентрации зарядов электропроводность Г. увеличивается. Зависимость электропроводности Г. от различных физических факторов рассмотрена в ст. Электрический разряд в газах.
При температурах начиная с нескольких тыс. градусов всякий Г. частично ионизуется и превращается в плазму. Если концентрация зарядов в плазме невелика, то свойства её мало отличаются от свойств обычного Г.
По магнитным свойствам Г. делятся на диамагнитные (к ним относятся, например, инертные газы, h3, N2, CO2, h3O) и парамагнитные (например, O2). Диамагнитны те Г., молекулы которых не имеют постоянного магнитного момента и приобретают его лишь под влиянием внешнего поля (см. Диамагнетизм). Те же Г., у которых молекулы обладают постоянным магнитным моментом, во внешнем магнитном поле ведут себя как парамагнетики (см. Парамагнетизм). Учёт межмолекулярного взаимодействия и внутреннего строения молекул необходим при решении многих проблем физики Г., например при исследовании влияния верхних разреженных слоев атмосферы на движение ракет и спутников (см. Газовая динамика, Аэродинамика разреженных газов).
В современной физике Г. называют не только одно из агрегатных состояний вещества. К Г. с особыми свойствами относят, например, совокупность свободных электронов в металле (электронный Г.), фононов в жидком гелии (фононный Г.) и т. д. Г. элементарных частиц и квазичастиц обладающих целым спином, т. н. бозонов (например, фотонов, p-мезонов, фононов), называется бозе-газом. Его свойства рассматривает квантовая статистика Бозе — Эйнштейна. Свойства частиц Г. с полуцелым спином — фермионов (например, электронов, нейтронов, нейтрино, дырок проводимости и др.) рассматривает квантовая статистика Ферми — Дирака (см. Статистическая физика).
| Свойства газов | Азот N2 | Аргон Ar | Водород h3 | Воздух | Кислород O2 | Углекислый газ CO2 |
| Масса 1 моля (г) | 28,02 | 39,94 | 2,016 | 28,96 | 32,00 | 44,00 |
| Плотность при 0°C и 1 ат* (кг/м3) | 1,2506 | 1,7839 | 0,0899 | 1,2928 | 1,4290 | 1,976 |
| Теплоемкость при постоянном объеме сv и 0°C (кдж/моль•град) | 20,85 | 12,48 | 20,35 | 20,81 | 20,89 | 30,62 (55°C) |
| Скорость звука при 0°C (м/сек) | 333,6 | 319 | 1286 | 331,5 | 314,8 | 260,3 |
| Вязкость h при 0°C (h•106 н•сек /м2) | 16,6 | 21,2 | 8,4 | 17,1 | 19,2 | 13,8 |
| Теплопроводность l при 0°C (l•102 дж/м•сек•град) | 2,43 | 1,62 | 16,84 | 2,41 | 2,44 | 1,45 |
| Диэлектрическая проницаемость e при 0°C и 1 ат* | 1,000588 | 1,000536 | 1,000272 | 1,000590 | 1,000531 | 1,000988 |
| Удельная магнитная восприимчивость c при 20°C (c•106 на 1 г) | -0,43 | -0,49 | -1,99 | — | +107,8 | 0,48 |
Лит.: Кириллин В. А., Сычев В. В. и Шейндлин А. Е., Техническая термодинамика, М., 1969; Кикоин И. К. и Кикоин А. К., Молекулярная физика, М., 1963; Гиршфельдер Дж., Кертисс Ч., Берд Р., Молекулярная теория газов и жидкостей, пер. с англ., М., 1961; Термодинамические свойства индивидуальных веществ. Справочник, под ред. В. П. Глушко, 2 изд., т. 1—2, М., 1962.
Э. Э. Шпильрейн.
Рис. 1. р, Т-диаграмма состояния вещества. Область газообразного состояния заштрихована. Со стороны низких температур и давлений она ограничена кривыми сублимации (I) и парообразования (II). Тр — тройная точка, К — критическая точка. Штриховой линией показана критическая изохора вещества.
Рис. 2. Распределение Максвела для молекул азота при температурах 20 и 500°С. По оси ординат отложена доля молекул (в %), обладающих скоростями между с и (с + 10) м/сек; сн — наиболее вероятная скорость, которой обладает наибольшее число молекул при данной температуре; — средняя арифметическая скорость молекул; — средняя квадратичная скорость.
pandia.ru
Что такое агрегатное состояние? Агрегатное состояние вещества
Вопросы о том, что такое агрегатное состояние, какими особенностями и свойствами обладают твердые вещества, жидкости и газы, рассматриваются в нескольких учебных курсах. Существует три классических состояния материи, со своими характерными чертами строения. Их понимание является важным моментом в постижении наук о Земле, живых организмах, производственной деятельности. Эти вопросы изучают физика, химия, география, геология, физическая химия и другие научные дисциплины. Вещества, находящиеся при определенных условиях в одном из трех базовых типов состояния, могут изменяться при повышении или понижении температуры, давления. Рассмотрим возможные переходы из одних агрегатных состояний в другие, как они осуществляются в природе, технике и повседневной жизни.
Что такое агрегатное состояние?
Слово латинского происхождения "aggrego" в переводе на русский язык означает «присоединять». Научный термин относится к состоянию одного и того же тела, вещества. Существование при определенных температурных значениях и разном давлении твердых тел, газов и жидкостей характерно для всех оболочек Земли. Помимо трех базовых агрегатных состояний, существует еще и четвертое. При повышенной температуре и неизменном давлении газ превращается в плазму. Чтобы лучше понять, что такое агрегатное состояние, необходимо вспомнить о мельчайших частицах, из которых состоят вещества и тела.
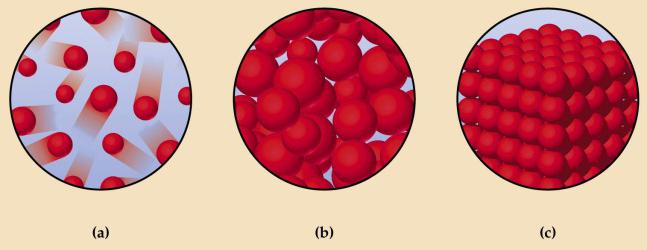
На схеме вверху показаны: а — газ; b — жидкость; с — твердое тело. На подобных рисунках кружочками обозначаются структурные элементы веществ. Это условное обозначение, на самом деле атомы, молекулы, ионы не являются сплошными шариками. Атомы состоят из положительно заряженного ядра, вокруг которого на большой скорости движутся отрицательно заряженные электроны. Знания о микроскопическом строении вещества помогают лучше понять различия, существующие между разными агрегатными формами.
Представления о микромире: от Древней Греции до XVII века
Первые сведения о частицах, из которых сложены физические тела, появились в Древней Греции. Мыслители Демокрит и Эпикур ввели такое понятие, как атом. Они считали, что эти мельчайшие неделимые частицы разных веществ обладают формой, определенными размерами, способны к движению и взаимодействию друг с другом. Атомистика стала наиболее передовым для своего времени учением Древней Греции. Но ее развитие затормозилось в средние века. Так как тогда ученых преследовала инквизиция римской католической церкви. Поэтому вплоть до нового времени не было внятной концепции, что такое агрегатное состояние вещества. Только после XVII века ученые Р. Бойль, М. Ломоносов, Д. Дальтон, А. Лавуазье сформулировали положения атомно-молекулярной теории, не утратившие своего значения и в наши дни.
Атомы, молекулы, ионы — микроскопические частицы строения материи
Значительный прорыв в понимании микромира произошел в XX веке, когда был изобретен электронный микроскоп. С учетом открытий, сделанных учеными ранее, удалось сложить стройную картину микромира. Теории, описывающие состояние и поведение мельчайших частиц вещества, довольно сложные, они относятся к области квантовой физики. Для понимания особенностей разных агрегатных состояний материи достаточно знать названия и особенности основных структурных частиц, которые образуют разные вещества.
- Атомы — химически неделимые частицы. Сохраняются в химических реакциях, но разрушаются в ядерных. Металлы и многие другие вещества атомарного строения имеют твердое агрегатное состояние при обычных условиях.
- Молекулы — частицы, которые разрушаются и образуются в химических реакциях. Молекулярное строение имеют кислород, вода, углекислый газ, сера. Агрегатное состояние кислорода, азота, диоксидов серы, углерода, кислорода при обычных условиях — газообразное.
- Ионы — заряженные частицы, в которые превращаются атомы и молекулы, когда присоединяют или теряют электроны — микроскопические отрицательно заряженные частички. Ионное строение имеют многие соли, например поваренная, железный и медный купорос.
Есть вещества, частицы которых определенным образом расположены в пространстве. Упорядоченное взаимное положение атомов, ионов, молекул называют кристаллической решеткой. Обычно ионные и атомарные кристаллические решетки характерны для твердых веществ, молекулярные - для жидкостей и газов. Высокой твердостью отличается алмаз. Его атомная кристаллическая решетка образована атомами углерода. Но мягкий графит тоже состоит из атомов этого химического элемента. Только они по-другому расположены в пространстве. Обычное агрегатное состояние серы — твердое, но при высоких температурах вещество превращается в жидкость и аморфную массу.
Вещества в твердом агрегатном состоянии
Твердые тела при обычных условиях сохраняют объем и форму. Например, песчинка, крупинка сахара, соли, кусок горной породы или металла. Если нагревать сахар, то вещество начинает плавиться, превращаясь в вязкую коричневую жидкость. Прекратим нагревание — снова получим твердое вещество. Значит, одно из главных условий перехода твердого тела в жидкость — его нагревание или повышение внутренней энергии частиц вещества. Твердое агрегатное состояние соли, которую используют в пищу, тоже можно изменить. Но чтобы расплавить поваренную соль, нужна более высокая температура, чем при нагревании сахара. Дело в том, что сахар состоит из молекул, а поваренная соль - из заряженных ионов, которые сильнее притягиваются друг к другу. Твердые вещества в жидком виде не сохраняют свою форму, потому что кристаллические решетки разрушаются.
Жидкое агрегатное состояние соли при расплавлении объясняется разрывом связи между ионами в кристаллах. Освобождаются заряженные частички, которые могут переносить электрические заряды. Расплавы солей проводят электричество, являются проводниками. В химической, металлургической и машиностроительной промышленности твердые вещества превращают в жидкие для получения из них новых соединений или придания им разной формы. Большое распространение получили сплавы металлов. Есть несколько способов их получения, связанных с изменениями агрегатного состояния твердого сырья.

Жидкость — одно из базовых агрегатных состояний
Если налить в круглодонную колбу 50 мл воды, то можно заметить, что вещество сразу же примет форму химического сосуда. Но как только мы выльем воду из колбы, то жидкость сразу же растечется по поверхности стола. Объем воды останется тот же — 50 мл, а ее форма изменится. Перечисленные особенности характерны для жидкой формы существования материи. Жидкостями являются многие органические вещества: спирты, растительные масла, кислоты.
Молоко — эмульсия, т. е. жидкость, в которой находятся капельки жира. Полезное жидкое ископаемое — нефть. Добывают ее из скважин с помощью буровых вышек на суше и в океане. Морская вода тоже является сырьем для промышленности. Ее отличие от пресной воды рек и озер заключается в содержании растворенных веществ, в основном солей. При испарении с поверхности водоемов в парообразное состояние переходят только молекулы Н2О, растворенные вещества остаются. На этом свойстве основаны методы получения полезных веществ из морской воды и способы ее очистки.
При полном удалении солей получают дистиллированную воду. Она кипит при 100 °С, замерзает при 0 °С. Рассолы кипят и превращаются в лед при других температурных показателях. Например, вода в Северном Ледовитом океане замерзает при температуре на поверхности 2 °С.
Агрегатное состояние ртути при обычных условиях — жидкость. Этим серебристо-серым металлом обычно заполняют медицинские термометры. При нагревании столбик ртути поднимается по шкале, происходит расширение вещества. Почему же в уличных термометрах используется подкрашенный красной краской спирт, а не ртуть? Объясняется это свойствами жидкого металла. При 30-градусных морозах агрегатное состояние ртути меняется, вещество становится твердым.
Если медицинский термометр разбился, а ртуть вылилась, то собирать руками серебристые шарики опасно. Вредно вдыхать пары ртути, это вещество очень токсичное. Детям в таких случаях надо обратиться за помощью к родителям, взрослым.

Газообразное состояние
Газы не способны сохранять ни свой объем, ни форму. Заполним колбу доверху кислородом (его химическая формула О2). Как только мы откроем колбу, молекулы вещества начнут смешиваться с воздухом в помещении. Это происходит благодаря броуновскому движению. Еще древнегреческий ученый Демокрит считал, что частички вещества находятся в постоянном движении. В твердых телах при обычных условиях у атомов, молекул, ионов нет возможности покинуть кристаллическую решетку, освободиться от связей с другими частицами. Такое возможно только при поступлении большого количества энергии извне.
В жидкостях расстояние между частицами немного больше, чем в твердых телах, им требуется меньше энергии для разрыва межмолекулярных связей. К примеру, жидкое агрегатное состояние кислорода наблюдается только при снижении температуры газа до −183 °C. При −223 °C молекулы О2 образуют твердое вещество. При повышении температуры сверх приведенных значений кислород превращается в газ. Именно в таком виде он находится при обычных условиях. На промышленных предприятиях действуют специальные установки для разделения воздуха атмосферы и получения из него азота и кислорода. Сначала воздух охлаждают и сжижают, а затем постепенно повышают температуру. Азот и кислород превращаются в газы при разных условиях.
Атмосфера Земли содержит 21 % по объему кислорода и 78 % азота. В жидком виде эти вещества в газовой оболочке планеты не встречаются. Жидкий кислород имеет светло-синий цвет, им при высоком давлении заполняют баллоны для использования в медицинских учреждениях. В промышленности и строительстве сжиженные газы необходимы для проведения очень многих процессов. Кислород нужен для газовой сварки и резки металлов, в химии — для реакций окисления неорганических и органических веществ. Если открыть вентиль кислородного баллона, давление уменьшается, жидкость превращается в газ.
Сжиженные пропан, метан и бутан находят широкое применение в энергетике, на транспорте, в промышленности и хозяйственно-бытовой деятельности населения. Получают эти вещества из природного газа или при крекинге (расщеплении) нефтяного сырья. Углеродные жидкие и газообразные смеси играют важную роль в экономике многих стран. Но запасы нефти и природного газа сильно истощены. По оценкам ученых, этого сырья хватит на 100–120 лет. Альтернативный источник энергии - воздушный поток (ветер). Используются для работы электростанций быстротекущие реки, приливы на берегах морей и океанов.

Кислород, как и другие газы, может находиться в четвертом агрегатном состоянии, представляя собой плазму. Необычный переход из твердого состояния в газообразное — характерная черта кристаллического йода. Вещество темно-фиолетового цвета подвергается сублимации — превращается в газ, минуя жидкое состояние.
Как осуществляются переходы из одной агрегатной формы материи в другую?
Изменения агрегатного состояния веществ не связаны с химическими превращениями, это физические явления. При повышении температуры многие твердые тела плавятся, превращаются в жидкости. Дальнейшее повышение температуры может привести к испарению, то есть к газообразному состоянию вещества. В природе и хозяйстве такие переходы характерны для одного из главных веществ на Земле. Лед, жидкость, пар — это состояния воды при разных внешних условиях. Соединение одно и то же, его формула — Н2О. При температуре 0 °С и ниже этого значения вода кристаллизуется, то есть превращается в лед. При повышении температуры возникшие кристаллики разрушаются — лед тает, вновь получается жидкая вода. При ее нагревании образуется водяной пар. Испарение — превращение воды в газ — идет даже при низких температурах. Например, замерзшие лужи постепенно исчезают, потому что вода испаряется. Даже в морозную погоду мокрое белье высыхает, но только процесс этот более длительный, чем в жаркий день.
Все перечисленные переходы воды из одного состояния в другое имеют огромное значение для природы Земли. Атмосферные явления, климат и погода связаны с испарением воды с поверхности Мирового океана, переносом влаги в виде облаков и тумана на сушу, выпадением осадков (дождя, снега, града). Эти явления составляют основу Мирового круговорота воды в природе.

Как меняются агрегатные состояния серы?
При обычных условиях сера — это яркие блестящие кристаллы или светло-желтый порошок, т. е. это твердое вещество. Агрегатное состояние серы меняется при нагревании. Сначала при повышении температуры до 190 °C желтое вещество плавится, превращаясь в подвижную жидкость.
Если быстро вылить жидкую серу в холодную воду, то получается коричневая аморфная масса. При дальнейшем нагревании расплава серы он становится все более вязким, темнеет. При температуре свыше 300 °C агрегатное состояние серы снова изменяется, вещество приобретает свойства жидкости, становится подвижным. Эти переходы возникают благодаря способности атомов элемента образовывать цепочки разной длины.
Почему вещества могут находиться в разных физических состояниях?
Агрегатное состояние серы — простого вещества — твердое при обычных условиях. Диоксид серы — газ, серная кислота — маслянистая жидкость тяжелее воды. В отличие от соляной и азотной кислот она не летучая, с ее поверхности не испаряются молекулы. Какое агрегатное состояние имеет пластическая сера, которую получают при нагревании кристаллов?
В аморфном виде вещество имеет структуру жидкости, обладая незначительной текучестью. Но пластическая сера одновременно сохраняет форму (как твердое вещество). Существуют жидкие кристаллы, обладающие рядом характерных свойств твердых веществ. Таким образом, состояние вещества при разных условиях зависит от его природы, температуры, давления и других внешних условий.
Какие существуют особенности в строении твердых тел?
Имеющиеся различия между основными агрегатными состояниями материи объясняются взаимодействием между атомами, ионами и молекулами. Например, почему твердое агрегатное состояние вещества приводит к способности тел сохранять объем и форму? В кристаллической решетке металла или соли структурные частицы притягиваются другу к другу. В металлах положительно заряженные ионы взаимодействуют с так называемым «электронным газом» — скоплением свободных электронов в куске металла. Кристаллы солей возникают благодаря притяжению разноименно заряженных частиц — ионов. Расстояние между вышеперечисленными структурными единицами твердых тел намного меньше, чем размеры самих частиц. В этом случае действует электростатическое притяжение, оно придает прочность, а отталкивание недостаточно сильное.
Чтобы разрушить твердое агрегатное состояние вещества, надо приложить усилия. Металлы, соли, атомные кристаллы плавятся при очень высоких температурах. К примеру, железо становится жидким при температуре выше 1538 °С. Тугоплавким является вольфрам, из него изготавливают нити накаливания для электрических лампочек. Есть сплавы, которые становятся жидкими при температурах свыше 3000 °С. Многие горные породы и минералы на Земле находятся в твердом состоянии. Добывают это сырье с помощью техники в шахтах и карьерах.

Для отрыва даже одного иона от кристалла необходимо затратить большое количество энергии. Но ведь достаточно растворить соль в воде, чтобы кристаллическая решетка распалась! Это явление объясняется удивительными свойствами воды как полярного растворителя. Молекулы Н2О взаимодействуют с ионами соли, разрушая химическую связь между ними. Таким образом, растворение — это не простое перемешивание разных веществ, а физико-химическое взаимодействие между ними.
Как взаимодействуют молекулы жидкостей?
Вода может быть жидкостью, твердым веществом и газом (паром). Это ее основные агрегатные состояния при обычных условиях. Молекулы воды состоят из одного атома кислорода, с которым связаны два атома водорода. Возникает поляризация химической связи в молекуле, на атомах кислорода появляется частичный отрицательный заряд. Водород становится положительным полюсом в молекуле, притягивается атомом кислорода другой молекулы. Это слабое взаимодействие получило название «водородная связь».
Жидкое агрегатное состояние характеризуют расстояния между структурными частицами, сравнимые с их размерами. Притяжение существует, но оно слабое, поэтому вода не сохраняет форму. Парообразование происходит из-за разрушения связей, которое идет на поверхности жидкости даже при комнатной температуре.

Существуют ли межмолекулярные взаимодействия в газах?
Газообразное состояние вещества по ряду параметров отличается от жидкого и твердого. Между структурными частицами газов существуют большие промежутки, намного превышающие размеры молекул. При этом силы притяжения совсем не действуют. Газообразное агрегатное состояние характерно для веществ, присутствующих в составе воздуха: азота, кислорода, диоксида углерода. На рисунке ниже первый куб заполнен газом, второй жидкостью, а третий — твердым вещество.
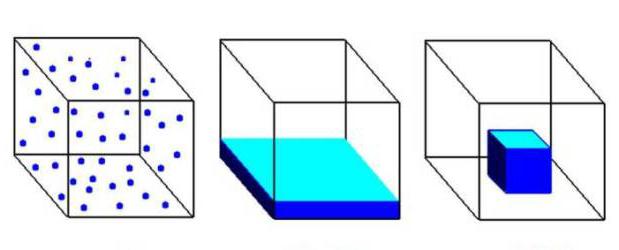
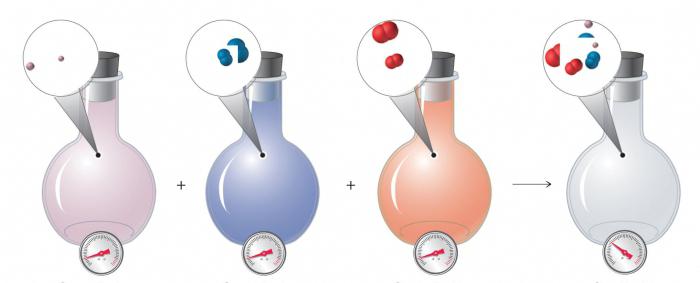
Многие жидкости являются летучими, с их поверхности отрываются и переходят в воздух молекулы вещества. Например, если к отверстию открытой бутылки с соляной кислотой поднести ватку, смоченную в нашатырном спирте, то появляется белый дым. Прямо в воздухе происходит химическая реакция между соляной кислотой и аммиаком, получается хлорид аммония. В каком агрегатном состоянии находится это вещество? Его частички, образующие белый дым, представляют собой мельчайшие твердые кристаллы соли. Этот опыт надо проводить под вытяжкой, вещества являются токсичными.
Заключение
Агрегатное состояние газа изучали многие выдающиеся физики и химики: Авогадро, Бойль, Гей-Люссак, Клайперон, Менделеев, Ле-Шателье. Ученые сформулировали законы, объясняющие поведение газообразных веществ в химических реакциях, при изменении внешних условий. Открытые закономерности не только вошли в школьные и вузовские учебники физики и химии. Многие химические производства основаны на знаниях о поведении и свойствах веществ, находящихся в разных агрегатных состояниях.
fb.ru
Физические свойства веществ. Агрегатное состояние — урок. Химия, 8–9 класс.
Сходство и отличие различных веществ можно установить по отдельным признакам.
Признаки, по которым вещества схожи, или же по которым можно отличить одно вещество от другого, называют свойствами.
Первое (и важнейшее) свойство любого вещества — это его агрегатное состояние при так называемых нормальных условиях (н. у.).
Обрати внимание!
В науке нормальными условиями (н. у.) принято считать такие условия, когда температура составляет \(0°\)С, а давление равно \(101,3\) кПа (килопаскалям).
Агрегатное состояние может быть твёрдым, жидким или газообразным (в звёздах вещество существует ещё в одном — плазменном — состоянии).
В твёрдом агрегатном состоянии частички, из которых состоит вещество (атомы, молекулы или ионы), обладают наименьшим запасом энергии, расстояние между частичками наименьшее, а сами частички совершают колебательные движения.
Например, при нормальных условиях в твёрдом агрегатном состоянии находятся металлы (кроме ртути), алмаз, графит, поваренная соль, пищевая сода, сахар (сахароза).
В жидком агрегатном состоянии частички, из которых состоит вещество, обладают большим запасом энергии, расстояния между ними больше, и движутся они поступательно и хаотично (неупорядоченно).
Например, при нормальных условиях жидкостью является вода, винный спирт, ацетон, а также ртуть.
Если вещество находится в газообразном агрегатном состоянии, частички, из которых состоит вещество, имеют наибольший запас энергии, расстояние между ними наибольшее, и движутся они хаотично с большой скоростью.
Например, при нормальных условиях в газообразном агрегатном состоянии находятся азот, кислород, озон, углекислый газ, аргон и гелий.
Обрати внимание!
При изменении условий агрегатное состояние может измениться.
Так, если температура опускается ниже \(0\) °С, вода переходит из жидкого в твёрдое агрегатное состояние, то есть превращается в лёд. Если же температура повышается до \(100\) °С, вода переходит из жидкого в газообразное агрегатное состояние, то есть превращается в водяной пар.
Обрати внимание!
Большинство веществ, в зависимости от условий, может существовать как в твёрдом, так в жидком или газообразном состояниях.
Однако некоторые вещества, такие как целлюлоза, из которой изготавливают бумагу, бывают только твёрдыми. Сахар можно расплавить, но перевести его в газообразное агрегатное состояние не получится. Дело в том, что такие вещества при нагревании начинают разлагаться, то есть превращаются в другие вещества, обладающие другими свойствами.
 |  |  |
| Хлор — газ жёлто-зелёного цвета, переходит в жидкое агрегатное состояние при температуре \(–34,04\) °С | Жидкая ртуть становится твёрдой при температуре \(–38,83\) °С и переходит в газообразное состояние при температуре \(+356,7\) °С | Лимонно-жёлтая сера переходит в жидкое агрегатное состоянии при нагревании до температуры \(+115,2\) °С |
www.yaklass.ru
Агрегатное состояние - реагирующее вещество
Агрегатное состояние - реагирующее вещество
Cтраница 1
Агрегатное состояние реагирующих веществ или консистенция реакционной массы оказывают влияние не только на общий характер устройства аппарата, но также и на устройство некоторых его деталей. Так, например, устройства размешивающих приспособлений и оформление теплообмениваю-щей поверхности вполне определяются консистенцией реакционной массы и агрегатным состоянием реагирующих продуктов. [1]
Агрегатное состояние реагирующих веществ может отвечать в данном случае системе несмешивающихся жидкостей ( углеводород и сульфирующий агент) или суспензии твердого измельченного продукта в жидком сульфирующем агенте. [2]
В скобках указано агрегатное состояние реагирующих веществ. В данном случае твердый углерод вступает в реакцию с газообразным кислородом с образованием углекислого газа. [3]
В зависимости от агрегатного состояния реагирующих веществ, топохимические реакции могут быть разделены на типы, различающиеся не только кинетикой, но и, как правило, технологическим оформлением соответствующих процессов. [4]
В зависимости от агрегатного состояния реагирующих веществ существуют реакторы газофазных и жидкофазных процессов. По конструкции различают реакторы: колонные, с перемешивающими устройствами, змеевиковые, башенные, трубчатые, пуль-сационные. [5]
В зависимости от агрегатного состояния реагирующих веществ и катализаторов катализ бывает гомогенный и гетерогенный. [6]
Скорость горения при одинаковых агрегатном состоянии реагирующих веществ, расположении их в пространстве, концентрации окислителя в воздухе и тепло-массо-газообмене определяется пожароопасными свойствами горючих веществ. Знание этих свойств, а также их роли в процессе горения и развития пожара необходимо для понимания физической природы загорания, разработки и выбора эффективных средств пожаротушения, правильного решения тактических и других задач по тушению пожаров. [7]
Если известно изменение теплоемкости во всем интервале температур и для всех агрегатных состояний реагирующих веществ, то можно довольно точно рассчитать равновесие, однако расчет будет громоздким. [8]
Они, так же как и вся химическая аппаратура, классифицируются по агрегатному состоянию реагирующих веществ и способу работы - периодическому или непрерывному. Дополнительный фактор, который необходимо учитывать, - наличие или отсутствие катализатора. [9]
По современным представлениям горение есть комплекс сложных быстро протекающих физических явлений ( изменение агрегатного состояния реагирующих веществ и др.) и химических реакций окисления, сопровождающихся, как правило, выделением теплоты, света и дыма. Всякий процесс горения предполагает наличие горючего вещества и окислителя. Окислителем обычно является кислород. Однако известно, что водород и железо могут гореть в хлоре; порох, взрывчатые вещества, в составе которых одновременно содержатся горючие и окислитель - в вакууме. [10]
Конструкция химического аппарата зависит от его технологического назначения, параметров процесса ( давление, температура), агрегатного состояния реагирующих веществ, способа ведения процесса ( периодического или непрерывного), а также от особенностей конструкционных материалов. [11]
При написании термохимических уравнений твердое вещество, жидкость и газ обязательно обозначаются символами ( тв), ( ж) и ( г) соответственно, поскольку изменение энтальпии зависит от агрегатного состояния реагирующих веществ и продуктов реакции. Стандартное состояние: для газа - состояние чистого газа при 105 Па; для жидкости - состояние чистой жидкости при 106 Па; для твердого вещества - наиболее устойчивое при давлении 105 Па кристаллическое состояние, например графит у углерода, ромбическая сера у серы и т.п. Стандартное состояние всегда относится к 298 К. [12]
Агрегатное состояние реагирующих веществ при проведении рассматриваемых процессов конденсации отвечает системе несмешивающихся жидкостей ( серной кислоты и конденсируемых продуктов) или суспензии твердого измельченного конденсируемого продукта в жидком конденсирующем агенте. [13]
По агрегатному состоянию реагирующих веществ и катализатора разли - чают гомогенный катализ, когда реагенты и катализатор находятся в одной фазе, и гетерогенный катализ, когда каталитическая система включает несколько фаз. В нефтепереработке гетерогенный катализ, особенно с твердым катализатором, распространен значительно больше, чем гомогенный. [14]
По агрегатному состоянию реагирующих веществ и катализатора различают гомогенный катализ, когда реагенты и катализатор находятся в одной фазе, и гетерогенный катализ, когда каталитическая система включает несколько фаз. В нефтепереработке гетерогенный катализ, особенно с твердым катализатором, распространен значительно больше, чем гомогенный. [15]
Страницы: 1 2
www.ngpedia.ru
Газ (агрегатное состояние) Википедия
Газ (газообразное состояние) (от нидерл. gas, восходит к др.-греч. χάος) — одно из четырёх основных агрегатных состояний вещества, характеризующееся очень слабыми связями между составляющими его частицами (молекулами, атомами или ионами), а также их большой подвижностью. Частицы газа почти свободно и хаотически движутся в промежутках между столкновениями, во время которых происходит резкое изменение характера их движения. [1] Газообразное состояние вещества в условиях, когда возможно существование устойчивой жидкой или твёрдой фазы этого же вещества, обычно называется па́ром. Реальный газ представляет собой высоко перегретый пар, свойства которого незначительно отличаются от идеального газа. В связи с этим в термодинамическом описании паров и реальных газов следует различать только два состояния — насыщенные пары (двухфазовые системы) и перегретые пары — (однофазовые газообразные состояния)[2]. Существует и другое определение понятия реальный газ, включающее весь диапазон газообразного состояния вещества от насыщенного пара до высоко перегретого и сильно разреженного. Подобно жидкостям, газы обладают текучестью и сопротивляются деформации. В отличие от жидкостей, газы не имеют фиксированного объёма, а стремятся заполнить весь доступный объём (например, сосуда). В планетарном масштабе газ в атмосфере удерживается гравитацией и не образует свободной поверхности. Газообразное состояние — самое распространённое состояние вещества Вселенной (межзвёздное вещество, туманности, звёзды, атмосферы планет и т. д.). По химическим свойствам газы и их смеси весьма разнообразны: от малоактивных инертных газов до взрывчатых газовых смесей. Понятие «газ» иногда распространяют не только на совокупности атомов и молекул, но и на совокупности других элементарных [квантовых] частиц (то есть на квантовую систему) — фотонов, электронов, броуновских частиц, а также плазму.
Некоторые частные случаи
- Идеальный газ — газ, в котором взаимодействие между молекулами сводится к парным столкновениям, причём время межмолекулярного столкновения намного меньше среднего времени между столкновениями. Идеальный газ является простейшим модельным объектом молекулярной физики. В классической (феноменологической) термодинамике идеальный газ — гипотетический, не существующий в природе газ, в точности подчиняющийся уравнению газового состояния Клапейрона — Менделеева:PV=νRT{\displaystyle PV=\nu \;RT}
- Реальный газ — агрегатное состояние вещества (простого тела). Состояние реальных газов достаточно точно описывается уравнением Клапейрона в условиях далёких от температуры конденсации, (высоко перегретые пары), а в условиях, близких к конденсации, где силами молекулярного взаимодействия уже нельзя пренебречь, вместо уравнения Клапейрона — Менделеева используются приближённые эмпирические и полуэмпирические уравнения. Наиболее простым и распространённым является уравнение Ван-дер-Ваальса. Известно немало попыток теоретического вывода уравнения состояния реального газа. Американский физик Д. Майер и советский математик Н. Боголюбов с помощью методов статистической физики вывели уравнение состояния реального газа в наиболее общем виде, включающее так называемые вириальные коэффициенты, являющиеся функциями только температуры. Вириальные коэффициенты не могут быть определены теоретическими методами и должны определяться с помощью экспериментальных данных.[3]
- Газ Ван-дер-Ваальса — идеализированный газ, точно подчиняющийся уравнению Ван-дер-Ваальса. Важнейшим свойством этого газа является существование в такой простой модели фазового перехода газ — жидкость.
- Частично или полностью ионизованный газ называется плазмой (иногда называется следующим агрегатным состоянием).
- Также газом в технике и в быту кратко называют природный газ, основу которого составляет газ метан.
Этимология
Слово «газ» (нидерл. gas) было придумано в начале XVII века фламандским естествоиспытателем Я. Б. ван Гельмонтом для обозначения полученного им «мёртвого воздуха» (углекислого газа). Согласно Я. И. Перельману, Гельмонт писал: «Такой пар я назвал газ, потому что он почти не отличается от хаоса древних»[4]. Не исключено также воздействие немецкого gasen — «кипеть». В России для обозначения газов М. В. Ломоносов употреблял термин «упругие жидкости», но он не прижился.
Физические свойства
Макроскопические характеристики
Большинство газов сложно или невозможно наблюдать непосредственно нашими органами чувств, они описываются с помощью четырёх физических свойств или макроскопических характеристик: давлением, объёмом, количеством частиц (химики используют моль) и температурой. Эти четыре характеристики издавна неоднократно исследовались учёными, такими как Роберт Бойль, Жак Шарль, Джон Дальтон, Гей-Люссак и Амедео Авогадро для различных газов в различных условиях. Их детальное изучение в итоге, привело к установлению математической связи между этими свойствами, выраженной в уравнении состояния идеального газа.
Основной особенностью газа является то, что он заполняет всё доступное пространство, не образуя поверхности. Газы всегда смешиваются. Газ — изотропное вещество, то есть его свойства не зависят от направления. В случаях, когда силами тяготения можно пренебречь или они уравновешены другими силами, давление во всех точках газа одинаково (см. Закон Паскаля). В поле сил тяготения плотность и давление не одинаковы в каждой точке, уменьшаясь с высотой по барометрической формуле. Соответственно, в поле сил тяжести неоднородной становится смесь газов. Тяжёлые газы имеют тенденцию оседать ниже, а более лёгкие — подниматься вверх. В поле тяготения на любое тело, погружённое в газ, действует Архимедова сила[5], которую используют для полёта воздушных шаров и других воздухоплавтельных аппаратов, заполненные лёгкими газами или горячим воздухом. Газ имеет высокую сжимаемость — при увеличении давления возрастает его плотность. При повышении температуры газы расширяются. При сжатии газ может перейти в жидкость, если его температура ниже так называемой критической температуры. Критическая температура является характеристикой конкретного газа и зависит от сил взаимодействия между его молекулами. Так, например, газ гелий можно сжижить только при температуре меньшей, чем 4,2 К. Существуют газы, которые при охлаждении переходят в твёрдое тело, минуя жидкую фазу. Превращение жидкости в газ называется испарением, а непосредственное превращение твёрдого тела в газ — сублимацией.
Сосуществование с жидкостью
В определённом диапазоне температур и давлений газ и жидкость одного и того же вещества могут сосуществовать в виде равновесной двухфазовой системы. Газ над поверхностью жидкости называют насыщенным паром.
Микроскопические характеристики
Если бы можно было наблюдать газ под мощным микроскопом, можно было бы увидеть набор частиц (молекул, атомов и т. д.) без определённой формы и объёма, которые находятся в хаотическом движении. Эти нейтральные частицы газа изменяют направление только тогда, когда они сталкиваются с другими частицами или стенками ёмкости. Если предположить, что эти взаимодействия (удары) абсолютно упругие, это вещество превращается из реального в идеальный газ. Эта доля с микроскопической точки зрения газа описывается молекулярно-кинетической теорией. Все предпосылки, лежащие в этой теории, можно найти в разделе «Основные постулаты» кинетической теории.
Тепловое движение молекул газа
Важнейшей чертой теплового движения молекул газа — это беспорядочность (хаотичность) движения. Экспериментальным доказательством непрерывного характера движения молекул является диффузия и броуновское движение. Диффузия — это явление самопроизвольного проникновения молекул одного вещества в другое. В результате взаимной диффузии веществ происходит постепенное выравнивание их концентрации во всех областях занимаемого ими объёма. Установлено, что скорость протекания процесса диффузии зависит от рода веществ и температуры. Одним из самых интересных явлений, подтверждающих хаотичность движения молекул, является броуновское движение, которое проявляется в виде теплового движения микроскопических частиц вещества, находящихся в газе во взвешенном состоянии. Это явление в 1827 году впервые наблюдал Р. Броун, от имени которого оно получило название. Беспорядочность перемещения таких частиц объясняется случайным характером передачи импульсов от молекул газа частице с разных сторон. Броуновское движение оказывается тем заметнее, чем меньше частица и чем выше температура системы. Зависимость от температуры свидетельствует о том, что скорость хаотического движения молекул возрастает с увеличением температуры, именно поэтому его и называют тепловым движением.
Закон Авогадро
Закон Авогадро — одинаковые объёмы любых газов при одинаковом давлении и температуре содержат одинаковое число молекул. Этот закон был открыт на основе опытов по химии итальянским учёным Амедео Авогадро в 1811 году. Закон касается слабо сжатых газов (например, газов под атмосферным давлением). В случае сильно сжатых газов считать его справедливым нельзя. Закон Авогадро означает, что давление газа при определённой температуре зависит только от числа молекул в единице объёма газа, но не зависит от того, какие это молекулы.
Количество вещества, содержащее число граммов, равное его молекулярной массе, называется грамм-молекулой или молем. Из сказанного следует, что моли разных веществ содержат одинаковое число молекул. Число молекул в одном моле вещества, получившее название «число Авогадро», является важной физической величиной. По ГОСТ 3651.2-97 значение постоянной Авогадро принимается:
NA = 6,0221367 · 1023 ± 0,0000036 · 1023 моль−1число Авогадро по данным CODATA−2010 равно
NA = 6,02214129 · 1023 ± 0,00000027 · 1023 моль−1Для определения постоянной Авогадро были сделаны многочисленные и разнообразные исследования (броуновского движения, явлений электролиза и др.), которые привели к достаточно согласованным результатам и являются ярким свидетельством реальности молекул и молекулярного строения вещества.
Кинетическая теория
Кинетическая теория даёт представление о макроскопических свойствах газов, рассматривая их молекулярное строение и движение молекул. Начиная с определения импульса и кинетической энергии, можно, используя закон сохранения импульса и геометрические зависимости, связать макроскопические свойства системы (температуру и давление) с микроскопическими свойствами (кинетической энергии одной молекулы).
Кинетическая теория объясняет термодинамические явления, исходя из атомистических представлений. Теория постулирует, что тепло является следствием хаотического движения чрезвычайно большого количества микроскопических частиц (атомов и молекул). Теория объясняет, как газовая система реагирует на внешние воздействия. Например, когда газ нагревается от абсолютного нуля, при котором его (классические) частицы абсолютно неподвижны, скорость частиц возрастает с ростом его температуры. Это приводит к большему числу их столкновений со стенками сосуда в единицу времени за счёт более высокой скорости. По мере роста числа столкновений возрастает их воздействие на стенки сосуда, пропорционально которому возрастает давление. Успешное объяснение газовых законов, исходя из положений кинетической теории, стало одним из факторов подтверждения атомарного строения веществ в природе. В современной физике молекулярно-кинетическая теория рассматривается как составная часть статистической механики.
Электрический ток в газах
Газы — очень плохие проводники, но в ионизированном состоянии газ способен проводить электрический ток[6]. Проводимость газа зависит от напряжения нелинейно, поскольку степень ионизации изменяется по сложному закону. Основных способов ионизации газа два: термическая ионизация и ионизация электрическим разрядом. Кроме того, существует так называемый самостоятельный электрический разряд (пример — молния).
Термическая ионизация — придание атомам достаточной кинетической энергии для отрыва электрона от ядра и последующей ионизации вследствие повышения температуры газа и тепловое движение атомов газа, приводящее к столкновениям и превращением их в кинетическую энергию. Температуры, необходимые для ионизации газов, очень высоки (например, для водорода этот показатель составляет 6000 К). Этот тип ионизации газов распространён преимущественно в природе.
При низкой температуре газ также может проводить ток, если мощность его внутреннего электрического поля превышает некоторое пороговое значение. Пороговое значение в данном случае — достижение электроном под действием электрического поля достаточной кинетической энергии, необходимой для ионизации атома. Далее электроны снова разгоняются электрическим полем для ионизации и ионизируют два атома и т. д. — процесс становится цепным. В конечном итоге все свободные электроны достигнут позитивного электрода, позитивные ионы — негативного электрода. Данный тип ионизации распространён преимущественно в промышленности.
При нагревании катода электрическим разрядом с большой силой тока происходит его нагрев до степени термоэлектронной эмиссии электронов из него (дуговой разряд).
Процессы переноса
Для газа характерен высокий коэффициент самодиффузии. Газы имеют невысокую теплопроводность, поскольку передача энергии от молекулы к молекуле происходит за счет редких столкновений. Этим объясняются хорошие теплоизоляционные свойства шерсти и ваты, материалов, в которых большинство объёма заполнено воздухом. Но в газах действует другой механизм передачи тепла — конвекция.
Сжимаемость
Сжимаемость z — это отношение удельного объёма газа к удельному объёму идеального газа с такой же молярной массой. Как правило, это число чуть меньше единицы, при этом наиболее значительно отклоняется от неё вблизи линии насыщения и для достаточно сложных органических газов, например, для метана при стандартных условиях z=0,9981{\displaystyle z=0,9981}[7].
Рассчитать коэффициент сжимаемости можно несколькими способами:
- модифицированным методом NX19 мод;
- модифицированным уравнением состояния GERG-91 мод;
- уравнением состояния AGA8-92DC;
- уравнением состояния ВНИЦ СМВ.
Теплоёмкость
Теплоёмкость газа сильно зависит от характера процесса, который с ним протекает. Наиболее часто используются изобарная теплоёмкость cp{\displaystyle c_{p}} и изохорная cv{\displaystyle c_{v}}; для идеального газа cp=cv+R{\displaystyle c_{p}=c_{v}+R}.
Теплопроводность
Теплопроводность газов — явление направленного переноса тепловой энергии за счёт столкновения частиц газа без переноса вещества.
Вязкость
В отличие от жидкостей, кинематическая вязкость газов с ростом температуры растёт, хотя для динамической вязкости зависимость менее выражена. Также вязкость растёт с давлением.
Число Прандтля
Число Прандтля (отношение кинематической вязкости к температуропроводности) Pr=νa=μcpλ{\displaystyle \mathrm {Pr} ={\nu \over a}={\mu c_{p} \over \lambda }} для газов обычно немного меньше единицы.
Упрощённые модели газа
Под уравнением состояния (для газов) подразумевают математическую модель, которая используется для приближённого описания или моделирования свойств газа. В настоящее время не существует единого уравнения состояния, которое бы точно прогнозировало свойства всех газов при любых условиях. Поэтому было разработано большое число точных уравнений состояния для конкретных газов в диапазоне определённых температур и давлений. Математические модели газа, наиболее часто используемые — это модели «идеального газа» и «реального газа».
Идеальный газ
Идеальный газ — это газ, в котором молекулы можно считать материальными точками, а силами притяжения и отталкивания между молекулами можно пренебречь. В природе такого газа не существует, но близкими по свойствам к идеальному газу являются реальные разреженные газы при давлениях, не превышающих 200 атмосфер, и не очень низких температурах, поскольку при таких условиях расстояние между молекулами намного превышает их размеры. С точки зрения феноменологической термодинамики идеальным газом (по определению) называется гипотетический, не существующий в природе, газ, в точности подчиняющийся уравнению газового состояния Клапейрона — Менделеева: PV=νRT{\displaystyle PV=\nu \,RT} Различают три типа идеального газа:
- Классический идеальный газ или газ Максвелла — Больцмана.
- Идеальный квантовый газ Бозе (состоит из бозонов).
- Идеальный квантовый газ Ферми (состоит из фермионов).
Внутренняя энергия идеального газа описывается следующим уравнением:
U=c^VnRT=c^VNkT,{\displaystyle U={\hat {c}}_{V}nRT={\hat {c}}_{V}NkT,}где
c^V{\displaystyle {\hat {c}}_{V}} является константой (равной, например, 3/2 для одноатомного газа), U{\displaystyle U} — внутренняя энергия (Дж), P{\displaystyle P} — давление (Па), V{\displaystyle V} — объём (м3), n{\displaystyle n} — количество вещества (моль), R{\displaystyle R} — универсальная газовая постоянная (Дж/(моль·К)), T{\displaystyle T} — абсолютная температура (К), N{\displaystyle N} — количество молекул, k{\displaystyle k} — постоянная Больцмана (Дж/К).Реальный газ
Реальный газ — это газ, между молекулами которого действуют силы межмолекулярного взаимодействия. Опыт показал, что законы идеальных газов с высокой степенью точности справедливы для реальных газов лишь при температурах, превышающих критическую. При повышении давления и понижении температуры ниже критической обнаруживаются значительные отклонения в поведении всех реальных газов. Реальный газ имеет сжимаемость от внешних сил значительно меньшую, чем идеальный. Реальные газы конденсируются, а уравнение состояния идеального газа не может объяснить переход вещества из газообразного состояния в жидкое[8]. Силы межмолекулярного взаимодействия — короткодействующие, то есть проявляются на расстояниях R ≤ 10−9 м и быстро уменьшаются с увеличением расстояния. Силы межмолекулярного взаимодействия в зависимости от расстояния между молекулами могут быть силами притяжения или силами отталкивания. Молекулярные силы притяжения называют силами Ван-дер-Ваальса. Из рисунка видно, что для больших расстояний между молекулами, когда плотность газа мала, силы Ван-дер-Ваальса правильно передают характер взаимодействия между молекулами. Части кривой, соответствующей межмолекулярному отталкиванию, в модели Ван-дер-Ваальса соответствует положительная часть кривой. На этом участке U (r) → ∞ при r ≤ d, то есть центры молекул не могут приблизиться на расстояние r < d (d — диаметр молекулы). В общем, изображена пунктиром кривая представляет потенциальную энергию парного взаимодействия молекул, между которыми действуют силы притяжения, а силы отталкивания проявляются лишь в случае столкновения согласно модели твердых шариков.
В 1873 году Ван-дер-Ваальс, проанализировав причины отклонения свойств реальных газов от закона Бойля-Мариотта, вывел уравнение состояния реального газа, в котором были учтены собственный объём молекул и силы взаимодействия между ними. Аналитическое выражение уравнение Ван-дер-Ваальса для одного моля газа имеет вид:
(p+aVμ2)(Vμ−b)=RT{\displaystyle \left(p+{\frac {a}{V_{\mu }^{2}}}\right)\left(V_{\mu }-b\right)=RT},где коэффициенты a{\displaystyle a} и b{\displaystyle b} называют постоянными Ван дер Ваальса, которые зависят от химической природы вещества, температуры и давления. Уравнение Ван дер Ваальса для произвольного количества газа массой m{\displaystyle m} имеет вид:
(p+m2μ2aV2)(V−mμb)=mμRT{\displaystyle \left(p+{\frac {m^{2}}{\mu ^{2}}}{\frac {a}{V^{2}}}\right)\left(V-{\frac {m}{\mu }}b\right)={\frac {m}{\mu }}RT}Уравнение Ван-дер-Ваальса является приближенным уравнением состояния реального газа, причем степень его приближения различна для разных газов. Записано большое количество эмпирических и полуэмпирических уравнений состояния реальных газов (уравнение: Бертло, Клаузиуса — Клапейрона, Дитеричи, Редлиха — Квонг, Камерлинг-Оннес т. п.). За счет увеличения числа констант в этих уравнениях можно достичь лучшего согласования с практикой, по сравнению с уравнением Ван-дер-Ваальса. Однако уравнение Ван-дер-Ваальса, благодаря своей простоте и физическому содержанию постоянных a{\displaystyle a} и b{\displaystyle b} входящих в него, является самым распространённым для анализа качественной поведения реальных газов.
Интересные факты
- Чтобы испарить жидкость, вовсе необязательно её нагревать. Можно уменьшить атмосферное давление поднятием на высоту, либо вакуумированием.
См. также
Примечания
- ↑ Физическая Энциклопедия т. 1, 1988, с. 375.
- ↑ Белоконь Н. И., Основные принципы термодинамики, 1968, с. 78.
- ↑ Кириллин В. А. , Техническая термодинамика, 1983, с. 165.
- ↑ Перельман Я. И. ,Занимательная физика, 1994, с. 109.
- ↑ Физическая Энциклопедия т. 1, 1988, с. 123.
- ↑ Элементарный учебник ;физики / Под ред. Ландсберг Г. С.. — Изд. 8-е. — М.: Наука, 1972. — Т. 2. — С. 230—268.
- ↑ ГОСТ 30319.1-96. Газ природный. Методы расчета физических свойств. Определение физических свойств природного газа, его компонентов и продуктов его переработки.
- ↑ Вукалович М. П., Техническая термодинамика, 1968, с. 190—192.
Литература
- Физическая Энциклопедия / Гл. ред. А. М. Прохоров. — М.: Советская Энциклопедия, 1988. — Т. 1. — 704 с.
- Белоконь Н. И. Основные принципы термодинамики. — М.: Недра, 1968. — 112 с.
- Вукалович М. П. Техническая термодинамика. — М.: Энергия, 1968. — 496 с.
- Перельман Я. И. Занимательная физика. — Чебоксары: ТОО Арта, 1994. — Т. 2. — 272 с..
- Кириллин В. А. Техническая термодинамика. — 4-е. — М.: Энергоатомиздат, 1983. — 416 с.
wikiredia.ru
Газ (агрегатное состояние)
Газ (газообразное состояние) (от греч. χάος — хаос) — агрегатное состояние вещества, характеризующееся очень слабыми связями между, составляющими его, частицами (молекулами, атомами или ионами), а также их большей подвижностью.
Подобно жидкостям, газы обладают текучестью и не сопротивляются деформации. В отличие от жидкостей, газы не имеют фиксированного объёма, а стремятся заполнить весь доступный объём (например, сосуда).
Некоторые частные случаи
- Идеальный газ — газ, в котором взаимодействие между молекулами полностью отсутствует. Идеальный газ является простейшим модельным объектом молекулярной физики.
- Реальный газ — газ, в котором учитывается взаимодействие между молекулами. Уравнение состояния реального газа часто строится методами теории возмущений, при этом отличие от уравнения состояния идеального газа описывается набором вириальных коэффициентов.
- Газ ван-дер-Ваальса — частный случай реального газа с достаточно простым модельным уравнением состояния. Важнейшим свойством газа ван-дер-Ваальса является существование в такой простой модели фазового перехода газ-жидкость.
- Частично или полностью ионизованный газ называется плазма.
Также газом часто кратко называют природный газ.
Этимология
Слово «газ» (голл. gas) было придумано в начале XVII века голландским естествоиспытателем Я. Б. ван Гельмонтом (Jean Baptiste van Helmont), для обозначения полученного им «мёртвого воздуха» (углекислого газа). Согласно, Я. И. Перельману, Гельмонт писал: «Такой пар я назвал газ, потому что он почти не отличается от хаоса древних».
Согласно В. Вундту, звуковой строй этого слова целиком определяется смысловыми отголосками тех терминов и выражений, которые для учёного сознания того времени обозначали родственные идеи и образы. По мнению Вундта, прежде всего Гельмонт думал, что открытый им газ напоминает первобытный хаос. Кроме того, на Гельмонта действовало представление слова blas (ср. немецкое blasen), которое он употреблял для обозначения холодного воздуха, исходящего из звёзд. Наконец, сюда же примешивалась мысль о слове Geist, соответствующем латинскому spiritus, так как газ, под которым Гельмонт подразумевал, главным образом, углекислоту, по латыни передавался через spiritus silvestris («лесной дух»). Некоторые подозревают воздействие немецкого gasen «кипеть».
В России для обозначения газов М. В. Ломоносов употреблял термин «упругие жидкости», но он не прижился.
См. также
mediaknowledge.ru





















