ГАЗЫ ГОРЮЧИЕ. Горючие газы
ГАЗЫ ГОРЮЧИЕ - это... Что такое ГАЗЫ ГОРЮЧИЕ?
газы горючие — Вид топлива, добываемого из недр земли (природные Г.г.), получаемого путём газификации твёрдого топлива в газогенераторах (искусственные Г.г.) или же являющегося побочным продуктом различных производств [Терминологический словарь по строительству … Справочник технического переводчика
Газы горючие — газообразные вещества, способные гореть. В широком смысле слова к Г. г. относятся водород, окись углерода, сероводород, газообразные углеводороды (например, метан, этан, этилен). В технике под Г. г. обычно понимают природные и… … Большая советская энциклопедия
ГАЗЫ ГОРЮЧИЕ — газообразные углеводороды, преим. метан и его гомологи (этан и др.). Природные Г. г. содержат примеси азота, углекислоты, инертных газов, сероводорода и др. Г. г. образуют в осадочных породах земной коры газовые залежи либо присутствуют (преим. в … Большой энциклопедический политехнический словарь
ГОСТ Р 53762-2009: Газы горючие природные. Определение температуры точки росы по углеводородам — Терминология ГОСТ Р 53762 2009: Газы горючие природные. Определение температуры точки росы по углеводородам оригинал документа: 3.3 автоматический конденсационный анализатор ТТРув: Конденсационный анализатор ТТРув, при выполнении измерений… … Словарь-справочник терминов нормативно-технической документации
ГОСТ Р 53763-2009: Газы горючие природные. Определение температуры точки росы по воде — Терминология ГОСТ Р 53763 2009: Газы горючие природные. Определение температуры точки росы по воде оригинал документа: 3.4 автоматический конденсационный гигрометр: Конденсационный гигрометр, при выполнении измерений которым наличие или… … Словарь-справочник терминов нормативно-технической документации
ГАЗЫ — ГАЗЫ, вещества, находящиеся в состоянии, характеризующемся тем, что молекулы вещества удалены на большие расстояния друг от друга и силы взаимодействия между молекулами очень невелики. Экспериментальные исследования вещества в газовом состоянии… … Большая медицинская энциклопедия
Газы в технике — Газы в технике, применяются главным образом в качестве топлива; сырья для химической промышленности: химических агентов при сварке, газовой химико термической обработке металлов, создании инертной или специальной атмосферы, в некоторых… … Большая советская энциклопедия
Газы — I Газы (французское gaz; название предложено голланским учёным Я. Б. Гельмонтом агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь… … Большая советская энциклопедия
Газы природные — (классификация) встречаются и проявляют себя в разл. геол. и геохим. условиях, весьма разнообразны по хим. сост. и физ. свойствам. Известны классификации Г. п.: Вернадского (1912, 1934), Соколова (1930), Хлопина и Черепенникова (1935), Белоусова… … Геологическая энциклопедия
Газы природные горючие — (a. combustible natural gases; н. naturliche Brenngase; ф. gaz naturels combustibles; и. gases combustibles naturales) смеси углеводородов метанового ряда и неуглеводородных компонентов, встречающиеся в осадочном чехле земной коры в виде… … Геологическая энциклопедия
ГАЗЫ ГОРЮЧИЕ - это... Что такое ГАЗЫ ГОРЮЧИЕ?
газы горючие — Вид топлива, добываемого из недр земли (природные Г.г.), получаемого путём газификации твёрдого топлива в газогенераторах (искусственные Г.г.) или же являющегося побочным продуктом различных производств [Терминологический словарь по строительству … Справочник технического переводчика
Газы горючие — газообразные вещества, способные гореть. В широком смысле слова к Г. г. относятся водород, окись углерода, сероводород, газообразные углеводороды (например, метан, этан, этилен). В технике под Г. г. обычно понимают природные и… … Большая советская энциклопедия
ГАЗЫ ГОРЮЧИЕ — вид топлива, добываемого из недр земли (природные Г.г.), получаемого путём газификации твёрдого топлива в газогенераторах (искусственные Г.г.) или же являющегося побочным продуктом различных производств (Болгарский язык; Български) горивни газове … Строительный словарь
ГОСТ Р 53762-2009: Газы горючие природные. Определение температуры точки росы по углеводородам — Терминология ГОСТ Р 53762 2009: Газы горючие природные. Определение температуры точки росы по углеводородам оригинал документа: 3.3 автоматический конденсационный анализатор ТТРув: Конденсационный анализатор ТТРув, при выполнении измерений… … Словарь-справочник терминов нормативно-технической документации
ГОСТ Р 53763-2009: Газы горючие природные. Определение температуры точки росы по воде — Терминология ГОСТ Р 53763 2009: Газы горючие природные. Определение температуры точки росы по воде оригинал документа: 3.4 автоматический конденсационный гигрометр: Конденсационный гигрометр, при выполнении измерений которым наличие или… … Словарь-справочник терминов нормативно-технической документации
ГАЗЫ — ГАЗЫ, вещества, находящиеся в состоянии, характеризующемся тем, что молекулы вещества удалены на большие расстояния друг от друга и силы взаимодействия между молекулами очень невелики. Экспериментальные исследования вещества в газовом состоянии… … Большая медицинская энциклопедия
Газы в технике — Газы в технике, применяются главным образом в качестве топлива; сырья для химической промышленности: химических агентов при сварке, газовой химико термической обработке металлов, создании инертной или специальной атмосферы, в некоторых… … Большая советская энциклопедия
Газы — I Газы (французское gaz; название предложено голланским учёным Я. Б. Гельмонтом агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь… … Большая советская энциклопедия
Газы природные — (классификация) встречаются и проявляют себя в разл. геол. и геохим. условиях, весьма разнообразны по хим. сост. и физ. свойствам. Известны классификации Г. п.: Вернадского (1912, 1934), Соколова (1930), Хлопина и Черепенникова (1935), Белоусова… … Геологическая энциклопедия
Газы природные горючие — (a. combustible natural gases; н. naturliche Brenngase; ф. gaz naturels combustibles; и. gases combustibles naturales) смеси углеводородов метанового ряда и неуглеводородных компонентов, встречающиеся в осадочном чехле земной коры в виде… … Геологическая энциклопедия
dic.academic.ru
Горючие газы и жидкости - Газовая резка
Горючие газы и жидкости
К горючим газам относят ацетилен, газы — заменители ацетилена (природный газ, пропан-бутановая смесь и др.), пары жидких горючих (керосин, бензин).
Ацетилен (С2#2) —один из основных горючих газов, применяемых при резке металлов, температура его пламени при сгорании в технически чистом кислороде достигает 3150 °С.
Технический ацетилен (ГОСТ 5457—75) получают, в основном, из карбида кальция в стационарных генераторах. Он выпускается промышленностью двух видов: растворенный и газообразный.
Растворенный ацетилен представляет собой находящийся под давлением в баллоне раствор ацетилена в ацетоне, равномерно распределенный в пористой массе?- При давлении 0,101 МПа (1,01 кгс/см2) и температуре 20°С в 1 кг ацетона растворяется 27,9 кг ацетилена, или в 1 л ацетона растворяется 20 л ацетилена.
Растворимость ацетилена в ацетоне возрастает примерно прямо пропорционально давлению. С понижением температуры растворимость увеличивается.
Газообразный ацетилен — бесцветный газ с резким специфическим запахом, вследствие наличия в нем фосфористого водорода и сероводорода. Его плотность при температуре 0°С и давлении 0,101 МПа равна 1,173 кг/м3.
При нормальном давлении (0,101 МПа) и температуре от —82,4 до —83,6°С ацетилен переходит в жидкое состояние, а при температуре —85°С и ниже — в твердое.
В жидком и твердом состоянии ацетилен легко взрывается от трения и удара, при взрыве происходит резкое повышение его давления и температуры, что может вызвать большие разрушения и тяжелые несчастные случаи.
Смеси ацетилена с воздухом и кислородом взрывоопасны. Нижний предел взрываемости с кислородом — 2,3% {ацетилена по объему), нижний предел взрываемости с воздухом — 2,2% (ацетилена по объему).
Наиболее взрывоопасны смеси, содержащие 7—13% ацетилена.
Ацетилен обладает способностью самовоспламеняться в чистом виде и в смеси с воздухом. Температура самовоспламенения ацетилена 335°С. Он легко реагирует с солями серебра, меди, ртути, образуя при этом нестойкие взрывчатые ацетилениды. Поэтому в аппаратуре, трубопроводах и приборах, работающих в среде ацетилена, не допускается применять детали из меди или медных сплавов, содержащих более 70% меди.
Торючие газы — заменители ацетилена. Широкое применение газы-заменители находят при кислородной резке металлов, где температура подогревающего пламени не влияет на характер протекания процесса, а лишь сказывается на длительности начального подогрева металла перед резкой. Поэтому для резки можно использовать газы-заменители, у которых температура газокислородного пламени не ниже 1800—2000°С, а теплотворная способность не ниже 10 000 кДж/м3.
Для определения потребного количества газа — заменителя ацетилена — пользуются коэффициентом замены (отношение низшей теплотворности ацетилена к низшей теплотворности газа, заменяющего ацетилен).
Таблица 1. Основные физико-химические свойства горючих газов и жидкостей, применяемых для кислородной резки
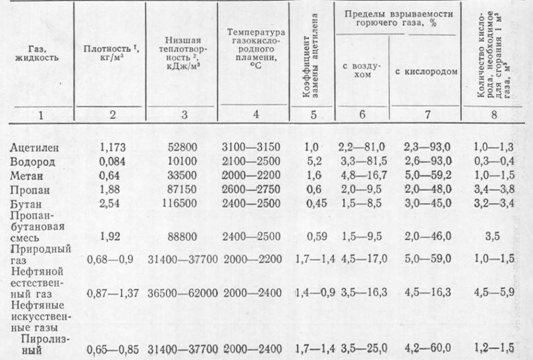
По физико-химическим свойствам (табл. 1) наиболее пригодными заменителями ацетилена являются природные и сжиженные газы. Искусственные горючие газы опасны в работе из-за высокой токсичности, особенно при содержании в них большого количества окиси углерода.
Сжиженные газы — это смеси углеводородов, которые при нормальных условиях находятся в газообразном состоянии, а при пониженной температуре или повышенном давлении — в жидком состоянии.
Для газопламенной обработки металла сжиженный газ состоит, в основном, из смеси пропана и бутана. Потребителям его доставляют в баллонах (ГОСТ 15860—70), вмещающих от 1 до 34 кг газа.
Ввиду того, что жидкие пропан и бутан обладают значительным коэффициентом объемного расширения (соответственно 306-Ю-5 и 212-Ю-5), баллоны после наполнения должны иметь необходимый объем паровой подушки, достаточный для принятия жидкости, расширившейся при повышении температуры. Предприятиям, потребляющим большое количество сжиженного газа, целесообразно применять пропановые рампы.
Сжиженные газы имеют низкие пределы взрываемости в смеси с воздухом. Они почти без запаха, поэтому с целью обнаружения утечки к ним обычно добавляют вещество с резким неприятным запахом. Концентрацию этого вещества выбирают с таким расчетом, чтобы в случае утечки запах газа был обнаружен гораздо раньше, чем его концентрация достигнет нижнего предела взрываемости.
При длительном пребывании рабочего в загазованном помещении сжиженные газы вызывают головокружение, а иногда — удушье.
Углеводородные газы обладают свойством переходить в жидкое состояние при обычной температуре и невысоком давлении. В этом случае объем всех углеводородов уменьшается более чем в 200 раз. Это позволяет транспортировать в небольших сосудах значительное количество сжиженного топлива.
Следует иметь в виду, что факел пламени сжиженных газов больше, чем ацетилено-кислородного пламени, а это приводит к получению менее концентрированного пламени. Кроме того, при термическом распаде сжиженных газов происходит поглощение тепла, а не выделение его, как у ацетилена. Максимальная температура сжиженных газов в смеси с кислородом меньше, чем у ацетилено-кислородного пламени. Все это ограничивает возможность применения сжиженных газов для некоторых процессов при газопламенной обработке металлов. Однако сравнительно высокая температура пламени пропан-бутановой смеси дает возможность применять его в качестве горючего газа при кислородной резке металлов.
Природные газы добывают на газовых месторождениях. К месту работы их транспортируют по трубопроводам, реже в баллонах под давлением до 15 МПа (150 кгс/см2). Природные газы в своем составе содержат в основном метан (до 98%) и небольшое количество различных примесей.
Одно из главных требований, предъявляемых к природным газам,—.минимальное содержание вредных примесей и отсутствие сероводорода.
Природные газы бесцветны и, как правило, без запаха. Для обнаружения утечек к ним добавляют одорант — вещество с резким неприятным запахом.
Благодаря высоким теплотворности и температуре газокислородного пламени, природные газы являются наиболее распространенным горючим, применяемым для газовой резки металлов.
Температура метано-кислородного пламени на 1000°С ниже ацетилено-кислородного. Максимальная температура пламени находится на расстоянии 10 мм от конца ядра.
Поэтому при резке деталей природным газом, особенно в тех случаях, когда рез начинают с середины, на подогрев металла до температуры воспламенения затрачивается примерно в 1,5—2 раза больше времени, чем при ацетилено-кислородной резке, что сказывается на производительности процесса.
Следует также иметь в виду, что при использовании природного газа вместо ацетилена расход подогревающего кислорода увеличивается примерно в два раза. Но, несмотря на это, общая стоимость работ при использовании природного газа вместо ацетилена ниже примерно на 10—15%. Кроме того, при применении природного газа отпадает необходимость в специальном хранении карбида кальция и обслуживании генератора, что повышает культуру производства.
Керосин и бензин — продукты переработки нефти и представляют собой легко испаряющиеся прозрачные жидкости. При газопламенной обработке они применяются в виде паров, для этого резаки снабжаются специальными испарителями или распылителями.
Жидкие горючие подаются в резак из специальных бачков с насосом, создающим давление в бачке до 0,2—0,3 МПа (2— 3 кгс/см2).
Для керосино-кислородной резки используют осветительный керосин (ГОСТ 4753—68) марок КО-ЗО, КО-25, КО-22 и КО-;20.
Перед заливкой в бачок керосин рекомендуется профильтровать через слой войлока и кускового едкого натра для очистки от примесей.
Бензин можно применять любого сорта, кроме этилированного, обладающего сильной токсичностью.
Читать далее:Эксплуатация газосварочной и газорезательной аппаратуры и оборудованияЭксплуатация переносных ацетиленовых генераторовКачество сварных соединенийТехнология резкиМеханизированная резкаРучная резкаCварочные деформации и напряженияCварка чугунаCварка цветных металлов и сплавовСварка низкоуглеродистой стали
Газы горючие — с русского
газы горючие — Вид топлива, добываемого из недр земли (природные Г.г.), получаемого путём газификации твёрдого топлива в газогенераторах (искусственные Г.г.) или же являющегося побочным продуктом различных производств [Терминологический словарь по строительству … Справочник технического переводчика
Газы горючие — газообразные вещества, способные гореть. В широком смысле слова к Г. г. относятся водород, окись углерода, сероводород, газообразные углеводороды (например, метан, этан, этилен). В технике под Г. г. обычно понимают природные и… … Большая советская энциклопедия
ГАЗЫ ГОРЮЧИЕ — газообразные углеводороды, преим. метан и его гомологи (этан и др.). Природные Г. г. содержат примеси азота, углекислоты, инертных газов, сероводорода и др. Г. г. образуют в осадочных породах земной коры газовые залежи либо присутствуют (преим. в … Большой энциклопедический политехнический словарь
ГАЗЫ ГОРЮЧИЕ — вид топлива, добываемого из недр земли (природные Г.г.), получаемого путём газификации твёрдого топлива в газогенераторах (искусственные Г.г.) или же являющегося побочным продуктом различных производств (Болгарский язык; Български) горивни газове … Строительный словарь
ГОСТ Р 53762-2009: Газы горючие природные. Определение температуры точки росы по углеводородам — Терминология ГОСТ Р 53762 2009: Газы горючие природные. Определение температуры точки росы по углеводородам оригинал документа: 3.3 автоматический конденсационный анализатор ТТРув: Конденсационный анализатор ТТРув, при выполнении измерений… … Словарь-справочник терминов нормативно-технической документации
ГОСТ Р 53763-2009: Газы горючие природные. Определение температуры точки росы по воде — Терминология ГОСТ Р 53763 2009: Газы горючие природные. Определение температуры точки росы по воде оригинал документа: 3.4 автоматический конденсационный гигрометр: Конденсационный гигрометр, при выполнении измерений которым наличие или… … Словарь-справочник терминов нормативно-технической документации
ГАЗЫ — ГАЗЫ, вещества, находящиеся в состоянии, характеризующемся тем, что молекулы вещества удалены на большие расстояния друг от друга и силы взаимодействия между молекулами очень невелики. Экспериментальные исследования вещества в газовом состоянии… … Большая медицинская энциклопедия
Газы в технике — Газы в технике, применяются главным образом в качестве топлива; сырья для химической промышленности: химических агентов при сварке, газовой химико термической обработке металлов, создании инертной или специальной атмосферы, в некоторых… … Большая советская энциклопедия
Газы — I Газы (французское gaz; название предложено голланским учёным Я. Б. Гельмонтом агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь… … Большая советская энциклопедия
Газы природные — (классификация) встречаются и проявляют себя в разл. геол. и геохим. условиях, весьма разнообразны по хим. сост. и физ. свойствам. Известны классификации Г. п.: Вернадского (1912, 1934), Соколова (1930), Хлопина и Черепенникова (1935), Белоусова… … Геологическая энциклопедия
Газы природные горючие — (a. combustible natural gases; н. naturliche Brenngase; ф. gaz naturels combustibles; и. gases combustibles naturales) смеси углеводородов метанового ряда и неуглеводородных компонентов, встречающиеся в осадочном чехле земной коры в виде… … Геологическая энциклопедия
translate.academic.ru
Горючие газы и их свойства. Сжигание газов
Основные понятия
- Давление — это сила, действующая на единицу площади:
- P=F/S (Ньютон/m2= Кгм/сек2м2=кг/сек2м=Па), где
- Р — давление (Па — Паскаль),
- F — сила, F = ma (Кгм/сек2, Н — Ньютон),
- S — площадь (м2).
За единицу измерения давления принимается техническая атмосфера, равная давлению в I кгс/см2. Техническая атмосфера измеряется в ат, или кгс/см2.
Давление в I ат способно уравновесить столб воды высотой 10 м, т. е. 10000 мм или столб ртути высотой 735 мм, т. к. ртуть тяжелее воды в 13,6 раза.
I кгс/см2 = 10 м вод.ст = 10000 мм вод.cт = 735,6 мм рт.ст.
- Соотношение единиц измерения давления (в системе СИ):
- 1кгс/см2 =9,8 . 1O4Па =105 Па = 0,1 мПа
- 1 мм вод.ст = 9,8Па = 10 Па
- 1 мм рт.ст = 133,3 Па
- Кратные единицы:
- Дека (ДА) — 10
- Гекто (Г) — 102
- Кило (К) — 103
- Мега (М) — 106
- Гига (Г) — 109
- Тера (Т) — 1012
- Дольные единицы:
- Деци (Д) — 10-1
- Санти (С) — 10-2
- Милли (М) — 10-3
- Микро (МК) — 10-6
- Нано (Н) — 10-9
- Пико (П) — 10-12
Давления могут быть избыточными и абсолютными. Если в газопроводе имеется газ, то его давление создаваемое внутри трубы будет абсолютным. Снаружи на стенки газопровода давит атмосферный воздух, поэтому газопровод находится под действием избыточного давления, т. е. разности внутреннего и наружного давлений. Величину избыточного давления измеряют манометрами, а для абсолютного давления необходимо к избыточному давлению прибавить атмосферное.
Измерение температуры газа транспортируемого по газопроводам измеряется термометрами, шкала которых имеет две постоянные точки, точку таяния льда (0°) и точку кипения воды (100°С). Расстояние на шкале между этими точками делится на 100 равных частей с ценой деления 1°С. Температура лежащая выше 0°С, обозначается знаком «+», а ниже знаком «-».
Применяется также и другая шкала — шкала «Кельвина». На этой шкале точка «0» соответствует абсолютному нулю, т. е. такой степени охлаждения тела (температура тела), при которой прекращается всякое движение молекул любого вещества. Абсолютный нуль, применяемый за начала отсчета температур в системе СИ, в технической системе равен 273,1б°С (температура, отсчитываемая от — 273,16°, называется абсолютной и обозначается буквой Т и °К)
Т = t0C + 273,2 = 100° + 273,2° = 373,2°К при t= 100°С
Измерение количества, тепла, измеряется (Кал)
Калория — это количество тепла, которое необходимо сообщить I г. чистой воды для повышения её температуры на 1°, или Ккал это количество тепла которое необходимо сообщить I кг дистиллированной воды для повышения её температуры на 1°.
Теплотворной способностью газового топлива называется количество тепла, которое выделяется при полном сгорании I м газа. Теплоту сгорания газообразного топлива измеряют в Ккал на I м3. Для удобства сравнения различных видов топлива введено понятие условного топлива, теплотворная способность которого принимается 7000 Ккал.
Величина, показывающая во сколько раз теплотворная способность данного топлива больше теплотворной способности условного топлива, называется тепловым эквивалентом. Для метана тепловой эквивалент будет равен:
Э = 8558/7000 = 1,22 кг, т.е 1м3 метанаэквивалентен 1,22 кг условного топлива.
Удельный вес горючих газов
Удельным весом горючих газов принято называть вес одного кубического метра газа в килограммах, взятого при температуре 0° и давлении в 760 мм рт.ст. (нм3/кг).
Различные газообразные виды топлива имеют различный вес. Так, например, I нм3 коксового газа весит 0,5 кг, а I нм3 генераторного паровоздушного газа — 1,2 кг. Это объясняется не только тем, что различные газообразные топлива отличаются друг от друга своим составом, но и различным весом составляющих их газов. Водород является самым легким газом, азот тяжелее его в 7 раз, кислород и метан в 8 раз, окись углерода в 14 раз, углекислый газ в 22 раза, некоторые тяжелые углеводороды в 29 раз. Почти все газообразные топлива легче воздуха, I нм3 которого весит 1,29 кг. Отсюда следует, что в помещении, в которое проник горючий газ, он будет стремиться вверх, т. к. плотность будет меньше плотности воздуха.
Указанный выше удельный вес газа называют абсолютным удельным весом, в отличие от относительного удельного веса газа, который выражает собою вес I нм газа в сравнении с весом 1 нм воздуха. Чтобы определить относительный удельный вес газа, нужно его абсолютный удельный вес разделить на удельный вес воздуха. Так, например, относительный удельный вес Ставропольского природного газа будет равен: 0,8/1,29 = 0,62.
Для того, чтобы своевременно обнаружить утечку газа, его подвергают одоризации, т. е. придают резкий специфический запах. В качестве одоранта применяют этилмеркаптан, запах должен ощущаться при содержании газа в воздухе не более 1/5 нижнего предела воспламеняемости. Практически природный газ, имеющий нижний предел взрываемости, равный 5% должен ощущаться в воздухе помещений при 1% концентрации.
К сожалению, при утечке газа из подземного газопровода, одоризованный газ при прохождении через грунт фильтруется, т. е. теряет одорант и его запах в загазованном помещении может не ощущаться. Поэтому утечки газа из подземного газопровода весьма опасны и требует от обслуживающего персонала повышенного внимания.
Состав горючих газов
В состав любого газообразного топлива входят горючая и негорючая части. Чем больше горючая часть, тем выше теплотворная способность топлива.
К горючим компонентам относятся:
Окись углерода (СО). Бесцветный газ, без запаха и вкуса; масса 1 Нm3 составляет 1,25 кг; теплотворная способность Q = = 2413 ккал/кг.
Пребывание в помещении, воздух которого содержит 0,5% СО в течение 5 мин. опасно для жизни. Предельно-допускаемая концентрация (ПДК) при использовании газа в быту составляет 2 мг/м3.
Водород (h3) — бесцветный, нетоксичный газ. Масса 1 Нм3 равна 0,09 кг, он в 14,5 раза легче воздуха. Теплотворная способность Q = 33860 ккал/кг. Отличается высокой реакционной способностью, имеет широкие пределы воспламеняемости, весьма взрывоопасен.
Метан (СН4) — бесцветный нетоксичный газ, без запаха и вкуса. В состав входит 75% углерода и 25% водорода. 1 Нм3 весит 0,717 кг. Теплотворная способность Q = 13200 ккал/кг. Взрывоопасен, пределы взрываемости 5–15.
Азот (N2) — негорючая часть газообразного топлива, без цвета, запаха и вкуса, не реагирует с кислородом, его рассматривают как инертный газ.
Углекислый газ (С02) — бесцветный, тяжелый, малореакционный, имеет слегка кисловатый запах и вкус, масса 1 Нм3 составляет 1,98 кг. При концентрации до 10% в воздухе вызывает сильное отравление.
Кислород (02) — без запаха, цвета и вкуса, масса 1 Нм3 составляет 1,43 кг. Содержание кислорода в газе понижает его теплотворную способность и делает газ взрывоопасным, по ГОСТу не должен превышать в газе не более 1% по объему.
Сероводород (h3S) тяжелый газ с сильным неприятным запахом, 1 Нм3 составляет 1,54 кг, сильно корродирует газопроводы, при сжигании образует сернистый газ (SО2) вредный для здоровья, содержание сероводорода не должно превышать 2 г на 100 м3 газа; к вредным примесям относится синильная кислота НС, содержание которой не должно превышать 5 г на 100 м3 газа.
Влажность газа — согласно действующему ГОСТу влагонасыщаемость газа при поступлении в городские газопроводы д.6. не более максимального насыщения газа при температуре 20°С зимой и 35°С летом (чем выше температура газа, тем больше влаги содержится в единице объема газа).
Состав и каллорийность реального сетевого газа г. Москвы
Таблица № 1
|
Адрес отбора проб с газ.ст. |
Углекислый газ (С02) |
Кислород (02) |
Водород (h3) |
Метан (СН4) |
Этан (С2Н6) |
Пропан (С3Н8) |
каллорийность |
|
Карачаровская |
0,6 |
0,3 |
1,2 |
97,32 |
0,21 |
0,37 |
7883 |
|
Очаковская |
0,6 |
0,2 |
1,2 |
97,60 |
0,25 |
0,15 |
7865 |
|
Головинская |
0,6 |
0,3 |
1,3 |
97,64 |
0,09 |
0,07 |
7829 |
|
Южная |
0,6 |
0,3 |
1,2 |
97,21 |
0,45 |
0,14 |
7861 |
Особенности физико-химических свойств жидкого (сжиженного) газа
Известно, что все вещества (тела) состоят из отдельных частиц (молекул), размещенных в определенном порядке. Чем ближе эти молекулы расположены друг к другу и чем больше взаимодействия их между собой, тем ближе тело по своему состоянию к твердому. Поэтому твердым называется такое состояние вещества, когда расстояния между его молекулами ничтожны, а силы взаимодействия огромны. Характерной особенностью твердых тел является то, что они обладают собственной формой и объемом. Твердыми видами топлива встречающимися в природе, являются например: древесина, уголь, сланцы. Жидкое состояние вещества характеризуется тем, что расстояние в нем между молекулами сравнительно невелики и силы их взаимодействия малы. Особенностью жидких тел является отсутствие у них собственного объема и формы. Все жидкости приобретают форму сосуда, в который они помещены. Жидкими видами топлива являются бензин, керосин, жидкий (сжиженный) газ и др.
Газообразным (парообразным) называется такое состояние вещества, когда расстояния между молекулами в нем огромны, а силы их взаимодействия ничтожны. Газы, также как и жидкости не имеют собственного объема и формы. Среди большого разнообразия видов твердого, жидкого и газообразного топлива особое место занимает жидкий газ.
Жидким называется такой газ, который при нормальной температуре (+20°С) и атмосферном давлении (760 мм рт.ст) находится в газообразном состоянии, обладая способностью при незначительном повышении давления превращаться в жидкость и, обратно, при снижении давления — быстро испаряться. Под жидкими газами, используемыми в быту, следует понимать смесь пропана и бутана с небольшим содержанием этана, пентана, бутилена и некоторых других газов.
Основным сырьем для получения жидкого газа являются нефть, природные газы и каменный уголь.
При использовании жидкого газа в быту приходиться иметь дело с его жидкой и газообразной фазами. Удельный вес жидкой фазы определяется по отношению к удельному весу воды, равному единице, и колеблется в зависимости от состава газа от 0,495 до 0,570 кг/л. Удельный вес газообразной (парообразной) фазы берется по отношению к удельному весу воздуха, принимаемому равным единице, и в зависимости от состава газа, колеблется от 1,9 до 2,6 кг/м3, т. е. пары жидкого газа используемые в бытовых газовых приборах примерно в два раза тяжелее воздуха.
Физико-химические свойства основных: жидких у глеводородных газов
Таблица № 2
|
Наименование показателей |
Пропан |
Бутан |
Этан |
Этилен |
Пропилен |
Бутилен |
|
Химическая формула |
С3Н8 |
С4Н9 |
С2Н6 |
С2Н4 |
С3Н6 |
С4Н8 |
|
Удельный вес газа_при 760 мм рт.ст. и 0°С, кг/м3 |
1,967 |
2,598 |
1,344 |
1,260 |
1,876 |
2,503 |
|
Удельный объем газа при 760 мм рт.ст. и 0°С, М3/КГ |
0,510 |
0,385 |
0,746 |
0,566 |
0,609 |
0,636 |
|
Отношение объема газа к объему жидкости |
272,6 |
229,3 |
294,3 |
340,2 |
287,8 |
258,2 |
|
Теплотворная способность ккал ; низшая/высшая |
22359 24320 |
29510 32010 |
I5370 16820 |
14320 15290 |
21070 22540 |
10831 11500 |
|
Пределы взрываемости смеси паров газа с воздухом % нижний/верхний |
2,1/9,5 |
1,5/8,5 |
3,0/14,0 |
3,0/16,0 |
2,2/9,7 |
1,7/9,0 |
Примечание:Зная отношение объема газа к объему жидкости (таб.2, п.4) можно определить объем испарившегося газа (м3), наполненной жидким газом емкости.
Давление и упругость паров жидкого газа
Известно, что над поверхностью различных водоемов (рек, озер, морей и т. д.) всегда имеются пары воды. Чем выше температура воздуха окружающего водоемы, тем больше паров над их поверхностью. Такое же явление наблюдается, если в какой-либо сосуд поместить керосин, бензин или жидкий газ, — пары жидкости всегда будут находиться над её поверхностью, причем их будет тем больше, чем выше температура
и чем больше поверхность (зеркало) испарения жидкости. Естественно, что если поместить жидкий газ в какой-либо сосуд и закрыть его, то пары этого газа начнут оказывать на стенки сосуда определенное давление.
Избыточное давление которое способно создать пары жидкого газа в закрытом сосуде, называется упругостью паров этого газа.
Приближенные значения упругости паров некоторых углеводородных газов в абсолютных атмосферах, в зависимости от температуры.
Таблица № 3
|
Температура, °С |
Пропан С3Н8 |
Бутан С4Н9 |
Этан С2Н6 |
Этилен С2Н4 |
Пропилен С3Н6 |
Бутилен С4Н8 |
|
-30 |
1,8 |
0,28 |
9,8 |
17,5 |
2,0 |
0,27 |
|
-20 |
2,7 |
0,45 |
13,0 |
23,2 |
3,0 |
0,41 |
|
-10 |
3,7 |
0,68 |
17,0 |
30,0 |
4,1 |
0,64 |
|
0 |
4,8 |
0,96 |
23,6 |
40,0 |
5,8 |
0,92 |
|
10 |
6,4 |
1, О |
30,0 |
50,7 |
7,6 |
1,4 |
|
20 |
8,5 |
2,1 |
38,0 |
64,0 |
10,3 |
2,0 |
|
30 |
11,0 |
2,9 |
48,0 |
78,0 |
13,3 |
3,16 |
Из таб.3 видно, что основные газы, входящие в состав жидкого газа, используемого в быту, — пропан и бутан — имеют резко отличную упругость паров даже при одинаковой температуре. Поэтому в холодное время года (зимой) используется газ, обладающий наибольшей упругостью паров, а именно газ содержащий 70–85% пропана. Применение в это время года газа с низкой упругостью паров, т. е. с повышенным содержанием бутана, может вызвать перерыв в работе газовых приборов, вследствии его плохой испаряемости.
- Примечание:
- Наличие в жидких газах этана и этилена является нежелателен, т. к. они обладая высокой упругостью паров, приводят к излишним давлениям в баллонах и др. емкостях.
- Жидкий газ обладает большим коэффициентом объемного расширения. Это означает, что с повышением температуры объем его в сосуде увеличивается, а следовательно емкости для транспорта и хранения заполняют не более чем на 84–90%, в противном случае при повышении температуры может произойти разрыв этих сосудов.
- (При хранении переполненных баллонов имели место случаи их разрыва, которые становились причиной крупных аварий с человеческими жертвами).
- Пары жидкого газа в смеси с воздухом в зоне между верхними и нижними пределами взрываемости образуют гремучие взрывоопасные смеси (табл.2).
Сжигание газов и газогорелочные устройства
Возникновение горения и его протекание возможны только при определенных условиях. Подвод к очагу горения горючего газа, его тщательное перемешивание с необходимым количеством воздуха, а также достижение определенного температурного уровня. Для нормального горения необходимо на 1 часть газа 10 частей воздуха. В результате сгорания 1 м3 метана получается I м3 углекислого газа, 2 м3 водяных паров и 7,52 м3 азота. Чем больше в продуктах сгорания С0о, тем меньше в них окиси углерода СО, т. е. тем полнее сгорание и меньше несгоревшего водорода (Hg). (СО + Н^. -самое выгодное горение.когда стрелка на нуле. Горение газа сопровождается пламенем, т. е. зоной в которой протекают реакции горения, Существует два типа распространения пламени: медленное и детонационное. Медленное называется нормальным — нормальной скоростью распространения пламени. Величина скорости распространения пламени имеет очень важное значение для правильной организации процесса сжигания газов.
Если скорость распространения пламени газовоздушной смеси, выходящей из горелки, будет меньше скорости движения этой смеси, то произойдет отрыв пламени.
Проскок пламени происходит в том случае, если скорость распространения пламени будет больше скорости движения газовоздушной смеси. Проскок может сопровождаться горением газа внутри самой горелки.
Детонация (взрыв) — это тип распространения пламени, при котором скорость распространения является наивысшей — несколько тыс. метров в сек. При детонации возникают наибольшие взрывные давления (20 атм и выше), приводящие к сильным разрушениям.
Способы сжигания газа
Газ можно сжигать светящимся и несветящимся пламенем, а также беспламенным горением. Способы сжигания газа зависит от способа перемешивания газа с воздухом происходит благодаря свойством частиц газа и воздуха проникать друг в друга. Такое явление называется диффузией, а горелки работающие по этому принципу называются диффузионными — светящимся пламенем.
Диффузионно-кинетическое горение — несветящееся пламя — инжекционные с первичным и вторичным поступлением воздуха из окружающей среда.
Кинетическое горение (пламени почти нет) — предварительное 100% смешение газа с воздухом, сгорание в окружении раскаленных огнеупоров и называется беспламенным сжиганием газа.
ingenerov.net
Горючие газы
Во многих городах нашей страны газ широко вошел в быт людей.
Кислород играет решающую роль при его горении. Прикройте на минутку воздушную заслонку у горелки газовой плиты. Пламя газовой горелки станет белым, коптящим и недостаточно горячим. Это потому, что газ сгорает не полностью, ему не хватает того кислорода, который он встречает в воздухе при выходе из горелки.
Чтобы полнее использовать теплотворную способность газа, горелка устроена так, что при входе в нее газ подсасывает воздух и, смешиваясь с ним, подходит к пламени с таким количеством кислорода, которого достаточно для его полного сгорания. Пламя при этом получается синеватое, короткое и очень горячее. Прикрывая кран газовой горелки, вы уменьшаете приток газа и тем самым уменьшаете подсос воздуха.
Газ, которым пользуются в быту, чаще всего добывается из недр земли и называется природным газом.
Большинство природных газов — это смесь органических соединений, главным образом углеводородов, то есть соединений, в состав которых входят углерод и водород. Оба эти элемента при соединении с кислородом выделяют огромное количество тепла.
В настоящее время открыто очень много крупных месторождений природного газа. Особенно богата природными газами Саратовская область.
По специальному газопроводу Саратов — Москва газ поступает в столицу нашей Родины, где широко используется в промышленности и для бытовых нужд населения.
Преимущества газообразного топлива перед твердым огромны. К ним прежде всего относятся удобства потребления, легкость подачи топлива в топку или газовую горелку, чрезвычайная простота управления пламенем и большая гигиеничность.
Но самым важным преимуществом газообразного топлива является его высокая теплотворная способность. Температура пламени горящего газа значительно выше температуры пламени твердого топлива и в некоторых случаях достигает 3000°.
Как же проходит процесс горения твердого и газообразного топлива?
При горении твердое топливо вначале подсушивается, а затем наступает так называемая сухая перегонка. Образуются газообразные вещества, содержащие углерод. Углерод этих горючих веществ соединяется с кислородом воздуха.
Сгорая, углерод образует углекислый газ (СO2). При этом выделяется тепло. Часть этого тепла расходуется на осушку и перегонку новых частей твердого топлива; часть тепла забирает азот, который поступает в топку вместе с кислородом.
Нагреваясь до высокой температуры, азот покидает топку, бесцельно унося с собой тепло в атмосферу. Кроме того, из-за плохого «перемешивания» воздуха с твердым топливом не весь кислород, поступающий в топку, участвует в горении; часть его, нагреваясь вместе с азотом, также уходит в атмосферу. Большое количество тепла уходит бесполезно, и вместе с ним уносится много мелких частиц угля в виде дыма.
При использовании газообразного топлива часть этик недостатков устраняется. Горючий газ еще до подхода к пламени хорошо перемешивается с кислородом воздуха. Подачу воздуха в топку можно отрегулировать так, чтобы его было достаточно для полного сгорания газа и не было лишней потери тепла.
При подаче в топку подогретого газа и горячего воздуха потери тепла почти полностью устраняются. На подогревание воздуха и газа обычно используется тепло газов, выходящих из топки. Газообразное топливо экономичнее и удобнее твердого.
Газообразное топливо можно получить и искусственным путем. Для этой цели служат так называемые газогенераторные установки.
В высокую колонку, снабженную внизу колосниковой решеткой, загружают уголь. Загрузка угля производится через верхнее загрузочное отверстие. Когда колонка заполнена, отверстие закрывают, оставляя только узкий выход для газов. Снизу колонки под решетку подают воздух с определенным содержанием кислорода и поджигают уголь. Нижние слои угля, сгорая в присутствии кислорода, образуют углекислый газ и выделяют тепло. Это тепло поднимается вверх по колонке и накаляет верхние слои угля. Углекислый газ, полученный при горении нижних слоев, проходит через раскаленные до 700° верхние слои угля, отдает им часть своего кислорода и образует окись углерода. Окись углерода вместе с азотом воздуха проходит через выходное отверстие и собирается в газохранилищах.
Газ, получаемый в генераторных установках, называют генераторным газом.
Если в генератор вместе с воздухом пустить водяной пар, то одновременно с окисью углерода образуется и водород. Смесь этих газов носит название водяного газа и также используется как газообразное топливо. При горении водяного газа окись углерода соединяется с кислородом и образует углекислый газ. А водород, соединяясь с кислородом, дает воду.
Как генераторный, так и водяной газ содержит окись углерода. Окись углерода — бесцветный газ, не имеющий запаха, немного легче воздуха. Она ядовита и вызывает угар, откуда и происходит другое ее название — угарный газ. В общежитии мы часто подразумеваем под «угаром» запах несгоревшего топлива. Однако запах этот принадлежит не окиси углерода, а другим продуктам горения, также содержащим углерод.
Если продолжительное время (3—4 часа) находиться в помещении, где на каждые 100 тысяч частей воздуха приходится только одна часть окиси углерода, можно угореть. Примесь одной части окиси углерода к 800 частям воздуха уже крайне опасна для жизни человека и за полчаса может вызвать смерть.
Лучшим средством для пострадавшего является чистый воздух, а при сильном отравлении — чистый кислород.
Окись углерода обладает большой калорийностью. При сгорании 1 граммолекулы окиси углерода (28 граммов) выделяется 67 500 калорий; это на 29 500 калорий меньше тепла, выделяемого при сгорании 1 грамматома углерода (12 граммов):
(С + O2 = СO2 + 97 000 кал.)
(СО + V2O2 = СO2 + 67 500 кал.)
Казалось бы, что при таком соотношении тепловых эффектов нецелесообразно уголь переводить в окись углерода, с тем чтобы, в конечном итоге, при сжигании ее получить меньше тепла. В действительности же это не так. Если подсчитать все потери тепла при сгорании твердого топлива, в том числе и потери на золу, которая составляет 5—30 процентов, то использование генераторного газа окажется выгодным.
Еще более целесообразным является получение окиси углерода на месте залегания угля без добычи его на поверхность. Такой способ получения газообразного топлива носит название подземной газификации угля.
Идея подземной газификации угля впервые родилась у великого русского химика Менделеева. В 80-х годах прошлого столетия он писал: «Настанет, вероятно, со временем даже такая эпоха, что угля из земли вынимать не будут, а там, в земле, сумеют превращать в горючие газы и их по трубам будут распределять на далекие расстояния».
Эта смелая для того времени мысль была подхвачена многими учеными. Начало осуществления идеи подземной газификации было оценено В. И. Лениным в статье «Одна из величайших побед в технике», опубликованной в «Правде» в 1913 году. В. И. Ленин охарактеризовал подземную газификацию как переворот в промышленности, равносильный гигантской технической революции едва ли не самой важной отрасли производства.
Однако в условиях царской России не удалось развить подземную газификацию. Это стало возможным только при советской власти.
В 1931 году Центральный Комитет Всесоюзной Коммунистической партии принял решение по реализации проблем подземной газификации угля. С тех пор в нашей стране идет непрерывная работа по широкому внедрению этого передового метода добычи топлива из недр земли.
Преимущества этого метода огромны.
Подземная газификация значительно упрощает и удешевляет разработку каменноугольных месторождений и облегчает труд горняков. Транспорт освобождается от перевозок большого количества твердого топлива.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
www.activestudy.info
НЕГОРЮЧИЕ ГАЗЫ | Газогенераторы МСД
Содержание инертных газов N2 и СОг в газообразном топливе в зиа’и: тельной степени определяет его свойства и области применения.
Увеличение содержания балластирующих горючий газ примесей Ii.3 и С02 понижает теплоту сгорания газа и удорожает его транспорт. Газ с высоким содержанием балласта и соответственно пониженной теплотой сгорания не экономично использовать для дальнего газоснабжения.
Важнейшая теплотехническая характеристика — жаропроизводитель — ность — не определяется однозначно теплотой сгорания. Так, жаропроизио- дительность окиси углерода и водорода выше жаропроизводительности метана, несмотря па значительно более высокую теплоту сгорания последнего. Однако снижение теплоты сгорания вследствие увеличения содержания балласта без изменения состава горючих компонентов сопровождается понижением не только теплоты сгорания, но и жаропроизводительности газа, так как при этом увеличивается объем продуктов сгорания за счет азота и двуокиси углерода, содержащихся в сжигаемом газе, и соответственно понижается количество тепла, приходящееся на единицу объема продуктов сгорания. Вследствие этого газы с высоким содержанием балласта характеризуются пониженной жаронроизводительностью и их применение в высокотемпературных процессах малоэффективно. Наличие балласта в газе сильно сказывается также на скорости распространения пламени.
Следует отметить, что теплота сгорания газа понижается вследствие содержания в нем балласта в одинаковой степени независимо от того, чем забалластирован газ — азотом или двуокисью углерода.
В отличие от этого жаропроизводительность газа, зависящая от теплосодержания продуктов сгорания и, следовательно, от их теплоемкости, снижается в большей степени при балластировании двуокисью углерода, так как объемная теплоемкость С02 значительно превышает объемную теплоемкость N2. Степень снижения скорости распространения пламени также зависит не только от процента балласта, но и от его состава.
Аоот N2. Двухатомный бесцветный газ без запаха и вкуса. Молекулярный вес азота 28,016. Вес 1 нм3 азота 1,25 кг. Вес 1 нм3 атмосферного азота (включая аргон) 1,26 кг.
Атомы азота соединены между собой в молекуле тройной связью N=N, на разрыв которой расходуется 225 тыс. ккал/молъ.
Теплота разрыва связей между атомами в молекуле азота очень велика, и взаимодействие молекулярного азота и кислорода с образованием закиси азота сопровождается затратой большого количества тепла.
Эндотермический процесс окгеления молекулярного азота осуществляет — ся лишь при весьма еысокой температуре. Незначительное количество окислов азота образуется при высокотемпературном сжигании газа, в особенности с применением обогащенного кислородом дутья. Поскольку азот практически не реагирует с кислородом, за исключением области весьма высоких температур, его рассматривают при расчетах процесса горения как инертный газ.
Содержание азота в различных видах газообразного топлива колеблется в пределах от 0 до 75%. В нефтезаводских газах, получаемых в процессе крекинга и пиролиза, ог практически отсутствует.
В большинстве прпр; лных и нефтепромысловых газов содержание азота весьма невелико (и ишимбаевском газе около0,5%, в дашавском—около 1%, в саратовском — 3%). Однако в некоторых природных и нефтепромысловых газах ого содержится значительно больше (в ухтинском около 10%, бугу — руслапском — 10—15%, прикамском — 30%).
15 водяном газе, производимом в генераторах периодического действия, содержится около 5% азота в результате смешения в начале периода парового дутья газа с продуктами горения, образующимися при разогреве слоя топлива и период воздушного дутья.
В каменноугольном коксовом газе содержится 8—10% азота, попадающего в газ С продуктами горения, проникающими через кладку в камеры коксовых печей.
В полукоксовом газе содержание азота колеблется в больших пределах в зависимости от метода полукоксования. При полукоксовании топлива в печах с внутренним обогревом в результате смешения газа с продуктами горения, используемыми в качестве теплоносителя, содержание азота в газе сильно возрастает.
Высоким содержанием азота и соответственно пониженной теплотой сгорания И жаропроизводительностью характеризуются газы, получаемые путем газификации топлива на воздушном или паровоздушном дутье. Содержание азота в генераторных газах из торфа и древесины, смешанных со швельгазом, равно — 54%.
В генераторных газах, производимых путем газификации каменных углей, аитрацита и кокса, содержится около 50% азота, а в доменных газах и газе подземной газификации — около 60%.
В газах, образующихся в процессе плавления чугуна в вагранках, при воздушном дутье в генераторах водяного газа, при производстве сажи из природного газа и жидкого топлива, содержание азота достигает 74—76%, т. е. приближается к содержанию азота в воздухе (79% по объему).
Высокое содержание балласта в этих газах обусловливает их низкую теплоту сгорания и жаропроизводительность и заставляет стремиться при их сжигании к использованию физического тепла и высокотемпературному подогреву воздуха.
Двуокись углерода (углекислый га!) СОа. Бесцветный тяжелый мало- реакционноспособный при низких и умеренных температурах газ со слегка кисловатым запахом и вкусом. С02 обладает кислотными свойствами. Способность С02 образовывать соли с основаниями используется в газовом анализе при определении содержания С02, а также при очистке газа от С02.
Малые концентрации С02 в воздухе (до — 1%) не оказывают токсического воздействия на организм. При концентрации 4—5% отмечается сильное раздражение органов дыхания. Концентрация около 10% СОа вызывает
Сильное отравление.
Молекулярный вес С02 — 44,09. Вес 1 нм3 газа 1,98 кг. Двуокись углерода в 1,53 раза тяжелее воздуха.
При температуре 20° и давлении 58,5 ата С02 сжижается. Жидкую С02 перевозят в стальных баллонах. При сильном охлаждении С02 застывает в белую снегообразную массу, возгоняющуюся при давлении 1 ата при—78,5°. Твердую С0.2 — «сухой лед» — используют для хранения скоропортящихся продуктов и других целей.
Содержание С02 в генераторных газах колеблется обычно от 5 до 8%. В газе подземной газификации содержится около 10% С02, в доменном газе — 10—12%.
В процессе термического разложения горючей массы твердого топлива с высоким содержанием кислорода выделяется значительное количество С02, большая часть которой образуется при сравнительно низких температурах, порядка 200—300° (процесс бертинирования). Поэтому газ, получаемый при низких температурах в процессе термической переработки топлива, содержит весьма высокий процент С02. При более высокотемпературном процессе сухой перегонки топлива содержание С02 в газе понижается вследствие интенсивного выделения горючих газов — углеводородов и водоро; а. Так, газы, получаемые при температуре около 550° в процессе полукоксования древесины, торфа и бурых углей с высоким содержанием кислорода в горючей массе, примерно на 50% состоят из С02. Напротив, в коксовом газе, получаемом при нагревании без доступа воздуха до температуры около 1000° каменных углей со сравнительно малым содержанием кислорода в горючей массе, содержится всего лишь 2—3% С02.
В нефтезаводских газах, получаемых при переработке не содержащего кислород углеводородного топлива, а также в нефтепромысловых газах С02 практически не содержится. В большинстве природных газов С02 также не содержится или содержится лишь в долях процента.
Ценность технических газов как топлива резко уменьшается при увеличении в них С02, поскольку теплота сгорания газа понижается, а транспорт газа на дальние расстояния становится неэкономичным. Кроме того, снижается жаропроизводительность газа и притом в большей степени, чем при балластировании его азотом, вследствие более высокой объемной теплоемкости С02.
Скорость распространения пламени газовоздушных смесей, забалластированных С02, также резко уменьшается. При этом несколько возрастает содержание в уходящих газах СО, что существенно при сжигании газа в бытовых плитах с выпуском продуктов горения в помещение.
Проф. У Бехером, исследовавшим влияние добавок СОг на полноту сгорания коксового газа, установлено, что с увеличением концентрации в газе С02 в результате снижения полноты сгорапия содержание окиси углерода в уходящих газах возрастало в 10 раз и достигало 0,05%. Поэтому при высоком содержании С02 в газе концентрация СО в воздухе легко может превысить предел, допустимый при использовании газа для коммунально-бытового потребления, особенно при отсутствии отвода продуктов горения в трубу.
В отличие от двухатомных газов и углеводородов, СОг, как и другие газы, обладающие кислотными свойствами, хорошо растворяется в воде. В 1 Ж3 воды при 10° и нормальном давлении растворяется около 1,2 мэ С02, т. е. в 40 раз больше, чем СО, и в 60 раз больше, чем Н2 и N3. С повышением давления до 20 атпа в 1 ле8 воды растворяется около 10 м3 СОг.
Теплотехническую ценность газов с высоким содержанием С02 можно повысить путем промывки газов водой под давлением около 20 ата. Растворенная в воде С02 выделяется при снижении давления до нормального и может быть использована для производства жидкой баллонной углекислоты и сухого льда.
Кислород Ог. Бесцветный газ без запаха и вкуса. Молекулярный вес 32. Вое 1 нм3 газа — 1,34 кг. Содержание его в газе, обусловленное примесью воздуха или содержащих кислород дымовых газов, понижает теплоту сгорания газа. Вместе с тем наличие кислорода снижает расход воздуха на горение газа и повышает его жаропроизводительность. Однако поскольку с кислородом, попадающим из воздуха или продуктов сгорания, в газ поступает соответствующий объем азота, жаропроизводительность газа не повышается.
Примесь кислорода делает газ взрывоопасным. Поэтому содержание кислорода в горючем газе жестко ограничивается техническими условиями.
| Границы (пределы) воспламенения газов и паров в смеси с воздухом при
|
Комментирование на данный момент запрещено, но Вы можете оставить
на Ваш сайт.
gazogenerator.com