Популярная химия. Формула гелия
Формула гелия в химии
Определение и формула гелия
По физическим свойствам гелий наиболее близок к молекулярному водороду. Вследствие ничтожной поляризуемости атомов гелия у него самые низкие температуры кипения (-269oC) и плавления (-271oC при 2,5×106 Па).
Гелий по сравнению с другими элементами обладает наибольшей энергией ионизации атома (24,59 эВ). Особая устойчивость электронной структуры атома отличает гелий от остальных элементов Периодической системы Д.И. Менделеева.
Гелий хуже других газов растворяется в воде и других растворителях. В 1 л воды, например, растворяется при 0oC менее 10 мл гелия, т.е. в два с лишним раза меньше, чем молекул водорода (h3), и в 51000 раз меньше, чем молекул хлороводорода (HCl).
Химическая формула гелия
Химическое обозначение гелия – He от латинского слова «helium». Этот химический элемент расположен в первом периоде в VIIIA группе Его внешний энергетический уровень заполнен, из-за чего он наименее химически активен, чем другие химические элементы (входит в группу элементов под названием инертные газы). Относительная атомная масса гелия равна 4,0026 а.е.м.
Электронная формула гелия
Ядро атома гелия содержит два протона и два нейтрона (массовое число гелия равно 4-м). Как и в атоме водорода, у гелия есть всего один энергетический уровень, на котором находятся два электрона (рис. 1).
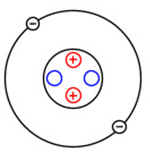
Рис. 1. Строение атома гелия.
Электронная формула атома гелия в основном состоянии выглядит следующим образом:
1s2
Примеры решения задач

| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Гелий, Вступление | |
| Символ | He |
| Латинское название | Helium |
| Тип вещества | простой химический элемент |
| Первооткрыватель | Ж. Жансен, Дж.Н. Локьер, Э. Франкланд |
| Год открытия | 1895 |
Основные параметры гелия по таблице Менделеева | |
| Атомный номер Z | 2 |
| Атомная масса | 4.002602 |
| Группа | 18 |
| Период | 1 |
| Принадлежность к группе | инертные благородные газы |
Механические свойства гелия | |
| Плотность газообразных веществ (при 0°C и 760мм.рт.ст) | 0.179 (Килограмм / Метр3) |
| Скорость звука | 970 (Метр / Секунда) |
Термодинамические свойства гелия | |
| Агрегатное состояние при нормальных условиях | газ |
| Точка кипения по Кельвину | 4.22 (Кельвин) |
| Точка кипения по Цельсию | -268.93 (°C) |
| Показатель адиабаты | 1.666 |
| Газовая постоянная | 2078 (Джоуль / (Килограмм · Кельвин)) |
| Коэффициент объемного расширения газов в интервале температур (0..100°C) при давлении 101.3 кПа | 3.66 · 10 − 3 (1 / Кельвин) |
Магнитные свойства гелия | |
| Тип магнитной проницаемости | диамагнетик |
Оптические свойства гелия | |
| Цвет | бесцветный |
| Коэффициент преломления | 1.000035 |
Спектр излучения гелия | |
Спектр поглощения гелия | |
Свойства атома гелия | |
| Конфигурация электронного облака | 1s2 |
| Радиус ядра | 2.2223615 · 10 − 15 (Метр) |
| Радиус атома | 31 · 10 − 12 (Метр) |
| Число протонов p | 2 |
| Число нейтронов n | 2 |
| Число электронов e | 2 |
| Массовое число A | 4 |
| Атомная структура гелия | 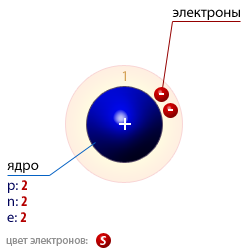 |
Радиоактивные свойства гелия | |
| Стабильность | элемент стабильный |
Химические свойства гелия | |
| Валентность | 0 |
Распространенность гелия | |
| Вселенная состоит из гелия на | 23% |
| Солнце состоит из гелия на | 23% |
| Мировой океан состоит из гелия на | 7.2×10-10% |
Вселенная | |
| Вселенная состоит из гелия на | 23% |
www.fxyz.ru
Газ гелий - Популярная химия

Гелий – химический элемент с атомным номером 2 в периодической системе химических элементов Д.И. Менделеева. Химическая формула Не. Гелий – инертный газ без цвета и запаха.
Гелий очень распространён во Вселенной. Он занимает второе место после водорода. Но на Земле гелия мало.
Гелий не вступает в реакцию ни с одним химическим элементом. Его атомы не соединяются даже между собой. Гелий не горит.
Открытие гелия

Открыли гелий в 1868 г. во время солнечного затмения. Причём, сделано это открытие одновременно двумя астрономами – французом Пьером Жюлем Жансеном и англичанином Джозефом Норманом Локьером. В спектре солнечной короны оба независимо друг от друга обнаружили жёлтую линию, которая не принадлежала ни одному их известных в то время элементов. Локьер в 1871 г. предположил, что на Солнце присутствует новый химический элемент. А в 1895 г. шотландский химик Уильям Рамзай впервые выделил газ из радиоактивного минерала клевеита. В спектре этого газа присутствовала точно такая же жёлтая линия. Новому элементу дали имя Helios – солнце.
Получение гелия

Гелий получают из природных гелионосных газов методом глубокого охлаждения. Выделение гелия осуществляется в два этапа. Первый этап – получение гелиевого концентрата конденсацией при низкой температуре. И второй этап – очистка гелиевого концентрата от метана, водорода, азота, неона, аргона.
Все основные мировые запасы гелия находятся в Алжире, Катаре, США и России. Крупнейший производитель гелия – США. В России гелия добывается немного, так как основные его месторождения расположены в малоосвоенных месторождениях Дальнего Востока и Восточной Сибири.
Применение гелия

Гелий обладает высокой электропроводностью и теплопроводностью. Кроме того, у него очень низкая температура кипения, минус 268,94оС.
Область применения гелия очень широка.
Смесь газообразного гелия с кислородом применяют для снятия приступов астмы. Гелий гораздо хуже растворяется в крови, чем азот. Поэтому его используют в дыхательных смесях, подаваемых водолазам при глубоководных погружениях, для создания искусственной атмосферы космических кораблей и станций.
Многие технологические процессы в производстве невозможно проводить в воздушной среде из-за возможности вступления в реакцию с газами воздуха исходного сырья или получаемого продукта. И здесь на помощь приходит газообразный гелий, с помощью которого создают специальные защитные среды.
Отдельные стадии получения ядерного топлива проходят в гелиевой защитной среде. Тепловыделяющие элементы ядерных реакторов также транспортируют и хранят в контейнерах, заполненных гелем. Гелий применяется для выявления возможностей утечки в атомных реакторах. Используют гелий в газовых термометрах, переключателях высокого напряжения, в счётчиках нейтронов, для газовой смазки подшипников.
Как инертная среда гелий используется при дуговой сварке.
Гелием наполняют дирижабли и воздушные шарики.
Гелий не токсичен. И вдыхание небольшого количества гелия вместе с воздухом безвредно.
ximik.biz
Гелий - это... Что такое Гелий?
ГЕ́ЛИЙ -я; м. [от греч. hēlios - солнце]. Химический элемент (He), не имеющий запаха химически инертный газ, самый лёгкий после водорода.
◁ Ге́лиевый, -ая, -ое. Г-ое ядро.
ГЕ́ЛИЙ (лат. Helium), He (читается «гелий»), химический элемент с атомным номером 2, атомная масса 4,002602. Относится к группе инертных, или благородных, газов (группа VIIIA периодической системы), находится в 1-м периоде. Природный гелий состоит из двух стабильных нуклидов: 3Не (0,00013% по объему) и 4Не. Почти полное преобладание гелия-4 связано с образованием ядер этого нуклида при -радиоактивном распаде урана, тория, радия и других атомов, происходившем в течение длительной истории Земли. Радиус нейтрального атома гелия 0,122 нм. Электронная конфигурация нейтрального невозбужденного атома 1s2. Энергии последовательной ионизации нейтрального атома равны, соответственно, 24,587 и 54,416 эВ (у атома гелия самая высокая среди нейтральных атомов всех элементов энергия отрыва первого электрона). Простое вещество гелий — легкий одноатомный газ без цвета, вкуса, запаха. История открытия Открытие гелия началось с 1868, когда при наблюдении солнечного затмения астрономы француз П. Ж. Жансен (см. ЖАНСЕН Пьер Жюль Сезар) и англичанин Д. Н. Локьер (см. ЛОКЬЕР Джозеф Норман) независимо друг от друга обнаружили в спектре солнечной короны (см. СОЛНЕЧНАЯ КОРОНА) желтую линию (она получила название D3-линии), которую нельзя было приписать ни одному из известных в то время элементов. В 1871 Локьер объяснил ее происхождение присутствием на Солнце нового элемента. В 1895 англичанин У. Рамзай (см. РАМЗАЙ Уильям) выделил из природной радиоактивной руды клевеита газ, в спектре которого присутствовала та же D3-линия. Новому элементу Локьер дал имя, отражающее историю его открытия (греч. Helios—солнце). Поскольку Локьер полагал, что обнаруженный элемент — металл, он использовал в латинском названии элемента окончание «lim» (соответствует русскому окончанию «ий»), которое обычно употребляется в названии металлов. Таким образом, гелий задолго до своего открытия на Земле получил имя, которое окончанием отличает его от названий остальных инертных газов. Нахождение в природе В атмосферном воздухе содержание гелия очень мало и составляет около 5,27·10-4% по объему. В земной коре его 0,8·10-6%, в морской воде — 4·10-10 %. Источником гелия служат нефти и гелионосные природные газы, в которых содержание гелия достигает 2—3%, а в редких случаях и 8—10% по объему. Зато в космосе гелий — второй по распространенности элемент (после водорода): на его долю приходится 23% космической массы. Получение Технология получения гелия очень сложна: его выделяют из природных гелионосных газов, пользуясь методом глубокого охлаждения. Месторождения таких газов имеются в России, США, Канаде и ЮАР. Гелий содержится также в некоторых минералах (монаците, торианите и других), при этом из 1 кг минерала при нагревании можно выделить до 10 л гелия. Физические свойства Гелий — легкий негорючий газ, плотность газообразного гелия при нормальных условиях 0,178 кг/м3 (меньше только у газа водорода). Температура кипения гелия (при нормальном давлении) около 4,2К (или –268,93 °C, это — самая низкая температура кипения). При нормальном давлении жидкий гелий не удается превратить в твердое вещество даже при температурах, близких к абсолютному нулю (0К). При давлении около 3,76 МПа температура плавления гелия 2,0К. Наименьшее давление, при котором наблюдается переход жидкого гелия в твердое состояние — 2,5МПа (25 ат), температура плавления гелия при этом около 1,1 К (–272,1 °C). В 100 мл воды при 20 °C растворяется 0,86 мл гелия, в органических растворителях его растворимость еще меньше. Легкие молекулы гелия хорошо проходят (диффундируют) через различные материалы (пластмассы, стекло, некоторые металлы). Для жидкого гелия-4, охлажденного ниже –270,97 °C, наблюдается ряд необычных эффектов, что дает основание рассматривать эту жидкость как особую, так называемую квантовую, жидкость. Эту жидкость обычно обозначают как гелий-II в отличие от жидкого гелия-I — жидкости, существующей при чуть более высоких температурах. График изменения теплоемкости жидкого гелия с изменением температуры напоминает греческую букву лямбда (l). Температура перехода гелия-I в гелий-II 2,186 К. Эту температуру часто называют l-точкой. Жидкий гелий-II способен быстро проникать через мельчайшие отверстия и капилляры, не обнаруживая при этом вязкости (так называемая сверхтекучесть (см. СВЕРХТЕКУЧЕСТЬ) жидкого гелия-II). Кроме того, пленки гелия-II быстро перемещаются по поверхности твердых тел, в результате чего жидкость быстро покидает тот сосуд, в который она была помещена. Это свойство гелия-II называют сверхползучестью. Сверхтекучесть гелия-II открыта в 1938 советским физиком П. Л. Капицей (см. КАПИЦА Петр Леонидович) (Нобелевская премия по физике, 1978). Объяснение уникальным свойствам гелия-II дано другим советским физиком Л. Д. Ландау (см. ЛАНДАУ Лев Давидович) в 1941—1944 (Нобелевская премия по физике, 1962). Никаких химических соединений гелий не образует. Правда, в разреженном ионизированном гелии удается обнаружить достаточно устойчивые двухатомные ионы Не2+. Применение Гелий используют для создания инертной и защитной атмосферы при сварке, резке и плавке металлов, при перекачивании ракетного топлива, для заполнения дирижаблей и аэростатов, как компонент среды гелиевых лазеров. Жидкий гелий, самая холодная жидкость на Земле, — уникальный хладагент в экспериментальной физике, позволяющий использовать сверхнизкие температуры в научных исследованиях (например, при изучении электрической сверхпроводимости (см. СВЕРХПРОВОДИМОСТЬ)). Благодаря тому, что гелий очень плохо растворим в крови, его используют как составную часть искусственного воздуха, подаваемого для дыхания водолазам. Замена азота на гелий предотвращает кессонную болезнь (см. КЕССОННАЯ БОЛЕЗНЬ) (при вдыхании обычного воздуха азот под повышенным давлением растворяется в крови, а затем выделяется из нее в виде пузырьков, закупоривающих мелкие сосуды).Популярная библиотека химических элементов. Раритетные издания. Наука и техника
Гелий
Гелий – подлинно благородный газ. Заставить его вступить в какие-либо реакции пока не удалось. Молекула гелия одноатомна.
По легкости этот газ уступает только водороду, воздух в 7,25 раза тяжелее гелия.
Гелий почти нерастворим в воде и других жидкостях. И точно так же в жидком гелии заметно не растворяется ни одно вещество.
Твердый гелий нельзя получить ни при каких температурах, если не повышать давление.
В истории открытия, исследования и применения этого элемента встречаются имена многих крупных физиков и химиков разных стран. Гелием интересовались, с гелием работали: Жансен (Франция), Локьер, Рамзай, Крукс, Резерфорд (Англия), Пальмиери (Италия), Кеезом, Камерлинг-Оннес (Голландия), Фейнман, Онсагер (США), Капица, Кикоин, Ландау (Советский Союз) и многие другие крупные ученые.
Неповторимость облика атома гелия определяется сочетанием в нем двух удивительных природных конструкций – абсолютных чемпионов по компактности и прочности. В ядре гелия, гелия-4, насыщены обе внутриядерные оболочки – и протонная, и нейтронная. Электронный дублет, обрамляющий это ядро, тоже насыщенный. В этих конструкциях – ключ к пониманию свойств гелия. Отсюда проистекают и его феноменальная химическая инертность и рекордно малые размеры его атома.
Огромна роль ядра атома гелия – альфа частицы в истории становления и развития ядерной физики. Если помните, именно изучение рассеяния альфа частиц привело Резерфорда к открытию атомного ядра. При бомбардировке азота альфа частицами было впервые осуществлено взаимопревращение элементов – то, о чем веками мечтали многие поколения алхимиков. Правда, в этой реакции не ртуть превратилась в золото, а азот в кислород, но это сделать почти так же трудно. Те же альфа частицы оказались причастны к открытию нейтрона и получению первого искусственного изотопа. Позже с помощью альфа частиц были синтезированы кюрий, берклий, калифорний, менделевий.
Мы перечислили эти факты лишь с одной целью – показать, что элемент №2 – элемент весьма необычный.
Земной гелий
Гелий – элемент необычный, и история его необычна. Он был открыт в атмосфере Солнца на 13 лет раньше, чем на Земле. Точнее говоря, в спектре солнечной короны была открыта ярко-желтая линия D, а что за ней скрывалось, стало достоверно известно лишь после того, как гелий извлекли из земных минералов, содержащих радиоактивные элементы.
Гелий на Солнце открыли француз Ж. Жансен, проводивший свои наблюдения в Индии 19 августа 1868 г., и англичанин Дж.H. Локьер – 20 октября того же года. Письма обоих ученых пришли в Париж в один день и были зачитаны на заседании Парижской Академии наук 26 октября с интервалом в несколько минут. Академики, пораженные столь странным совпадением, приняли постановление выбить в честь этого события золотую медаль.
В 1881 г. об открытии гелия в вулканических газах сообщил итальянский ученый Пальмиери. Однако его сообщение, впоследствии подтвержденное, мало кто из ученых принял всерьез. Вторично земной гелий был открыт Рамзаем в 1895 г.
В земной коре насчитывается 29 изотопов, при радиоактивном распаде которых образуются альфа частицы – высокоактивные, обладающие большой энергией ядра атомов гелия.
В основном земной гелий образуется при радиоактивном распаде урана-238, урана-235, тория и нестабильных продуктов их распада. Несравнимо меньшие количества гелия дает медленный распад самария-147 и висмута. Все эти элементы порождают только тяжелый изотоп гелия – 4Не, чьи атомы можно рассматривать как останки альфа частиц, захороненные в оболочке из двух спаренных электронов – в электронном дублете. В ранние геологические периоды, вероятно, существовали и другие, уже исчезнувшие с лица Земли естественно радиоактивные ряды элементов, насыщавшие планету гелием. Одним из них был ныне искусственно воссозданный нептуниевый ряд.
По количеству гелия, замкнутого в горной породе или минерале, можно судить об их абсолютном возрасте. В основе этих измерений лежат законы радиоактивного распада: так, половина урана-238 за 4,52 млрд лет превращается в гелий и свинец.
Гелий в земной коре накапливается медленно. Одна тонна гранита, содержащая 2 г урана и 10 г тория, за миллион лет продуцирует всего 0,09 мг гелия – половину кубического сантиметра. В очень немногих богатых ураном и торием минералах содержание гелия довольно велико – несколько кубических сантиметров гелия на грамм. Однако доля этих минералов в естественном производстве гелия близка к нулю, так как они очень редки.
Природные соединения, в составе которых есть альфа активные изотопы, – это только первоисточник, но не сырье для промышленного получения гелия. Правда, некоторые минералы, обладающие плотной структурой – самородные металлы, магнетит, гранат, апатит, циркон и другие, – прочно удерживают заключенный в них гелий. Однако большинство минералов с течением времени подвергаются процессам выветривания, перекристаллизации и т.д., и гелий из них уходит.
Высвободившиеся из кристаллических структур гелиевые пузырьки отправляются в путешествие по земной коре. Очень незначительная часть их растворяется в подземных водах. Для образования более или менее концентрированных растворов гелия нужны особые условия, прежде всего большие давления. Другая часть кочующего гелия через поры и трещины минералов выходит в атмосферу. Остальные молекулы газа попадают в подземные ловушки, в которых скапливаются в течение десятков, сотен миллионов лет. Ловушками служат пласты рыхлых пород, пустоты которых заполняются газом. Ложем для таких газовых коллекторов обычно служат вода и нефть, а сверху их перекрывают газонепроницаемые толщи плотных пород.
Так как в земной коре странствуют и другие газы (главным образом метан, азот, углекислота), и притом в гораздо больших количествах, то чисто гелиевых скоплений не существует. Гелий в природных газах присутствует как незначительная примесь. Содержание его не превышает тысячных, сотых, редко – десятых долей процента. Большая (1,5...10%) гелиеносность метано-азотных месторождений – явление крайне редкое.
Природные газы оказались практически единственным источником сырья для промышленного получения гелия. Для отделения от прочих газов используют исключительную летучесть гелия, связанную с его низкой температурой сжижения. После того как все прочие компоненты природного газа сконденсируются при глубоком охлаждении, газообразный гелий откачивают. Затем его очищают от примесей. Чистота заводского гелия достигает 99,995%.
Запасы гелия на Земле оцениваются в 5·1014 м3; судя же по вычислениям, его образовалось в земной коре за 2 млрд лет в десятки раз больше. Такое расхождение теории с практикой вполне объяснимо. Гелий – легкий газ и, подобно водороду (хотя и медленнее), не улетучивается из атмосферы в мировое пространство. Вероятно, за время существования Земли гелий нашей планеты неоднократно обновлялся – старый улетучивался в космос, а вместо него в атмосферу поступал свежий – «выдыхаемый» Землей.
В литосфере гелия по меньшей мере в 200 тыс. раз больше, чем в атмосфере; еще больше потенциального гелия хранится в «утробе» Земли – в альфа активных элементах. Но общее содержание этого элемента в Земле и атмосфере невелико. Гелий – редкий и рассеянный газ. На 1 кг земного материала приходится всего 0,003 мг гелия, а содержание его в воздухе – 0,00052 объемного процента. Столь малая концентрация не позволяет пока экономично извлекать гелий из воздуха.
Гелий во Вселенной
Недра и атмосфера нашей планеты бедны гелием. Но это не значит, что его мало повсюду во Вселенной. По современным подсчетам 76% космической массы приходится на водород и 23% на гелий; на все прочие элементы остается только 1%! Таким образом, мировую материю можно назвать водородно-гелиевой. Эти два элемента главенствуют в звездах, планетарных туманностях и межзвездном газе.
Рис. 1. Кривые распространенности элементов на Земле (вверху) и в космосе.«Космическая» кривая отражает исключительную роль водорода и гелия в мироздании и особое значение гелиевой группировки в строении атомного ядра. Наибольшую относительную распространенность имеют те элементы и те их изотопы, массовое число которых делится на четыре: 16О, 20Ne, 24Mg и т.д.
Вероятно, все планеты солнечной системы содержат радиогенный (образовавшийся при альфа распаде) гелий, а крупные – и реликтовый гелий из космоса. Гелий обильно представлен в атмосфере Юпитера: по одним данным его там 33%, по другим – 17%. Это открытие легло в основу сюжета одного из рассказов известного ученого и писателя-фантаста А. Азимова. В центре повествования – план (возможно, осуществимый в будущем) доставки гелия с Юпитера, а то и заброски на ближайший спутник этой планеты – Юпитер V – армады кибернетических машин на криотронах (о них – ниже). Погрузившись в жидкий гелий атмосферы Юпитера (сверхнизкие температуры и сверхпроводимость – необходимые условия для работы криотронов), эти машины превратят Юпитер V в мозговой центр солнечной системы...
Происхождение звездного гелия было объяснено в 1938 г. немецкими физиками Бете и Вейцзекером. Позже их теория получила экспериментальное подтверждение и уточнение с помощью ускорителей элементарных частиц. Суть ее в следующем.
Ядра гелия синтезируются при звездных температурах из протонов в результате термоядерных процессов, высвобождающих 175 млн киловатт-часов энергии на каждый килограмм гелия.
Разные циклы реакций могут привести к синтезу гелия.
В условиях не очень горячих звезд, таких, как наше Солнце, преобладает, по-видимому, протонно-протонный цикл. Он складывается из трех последовательно сменяющихся превращений. Вначале соединяются на огромных скоростях два протона с образованием дейтрона – конструкции из протона и нейтрона; при этом отделяются позитрон и нейтрино. Далее соединяются дейтрон с протоном в легкий гелий с испусканием гамма кванта. Наконец, реагируют два ядра 3Не, преобразуясь в альфа частицу и два протона. Альфа-частица, обзаведясь двумя электронами, станет потом атомом гелия.
Тот же конечный результат дает более быстрый углеродно-азотный цикл, значение которого в условиях Солнца не очень велико, но на более горячих, чем Солнце, звездах роль этого цикла усиливается. Он складывается из шести ступеней – реакций. Углерод играет здесь роль катализатора процесса слияния протонов. Энергия, выделяемая в ходе этих превращений, такая же, как и при протонно-протонном цикле – 26,7 МэВ на один атом гелия.
Реакция синтеза гелия – основа энергетической деятельности звезд, их свечения. Следовательно, синтез гелия можно считать праотцом всех реакций в природе, первопричиной жизни, света, тепла и метеорологических явлений на Земле.
Гелий не всегда бывает конечным продуктом звездных синтезов. По теории профессора Д.А. Франк-Каменецкого, при последовательном слиянии ядер гелия образуются 3Be, 12C, 16O, 20Ne, 24Mg, а захват этими ядрами протонов приводит к возникновению других ядер. Для синтеза ядер тяжелых элементов вплоть до трансурановых требуются исключительные сверхвысокие температуры, которые развиваются на неустойчивых «новых» и «сверхновых» звездах.
Известный советский химик А.Ф. Капустинский называл водород и гелий протоэлементами – элементами первичной материи. Не в этой ли первичности скрыто объяснение особого положения водорода и гелия в периодической системе элементов, в частности того факта, что первый период по существу лишен периодичности, характерной для прочих периодов?
Самый, самый...
Атом гелия (он же молекула) – прочнейшая из молекулярных конструкций. Орбиты двух его электронов совершенно одинаковы и проходят предельно близко от ядра. Чтобы оголить ядро гелия, нужно затратить рекордно большую энергию – 78,61 МэВ. Отсюда – феноменальная химическая пассивность гелия.
За последние 15 лет химикам удалось получить более 150 химических соединений тяжелых благородных газов (о соединениях тяжелых благородных газов будет рассказано в статьях «Криптон» и «Ксенон»). Однако инертность гелия остается, как и прежде, вне подозрений.
Вычисления показывают, что если бы и был найден путь получения, скажем фторида или окисла гелия, то при образовании они поглотили бы так много энергии, что получившиеся молекулы были бы «взорваны» этой энергией изнутри.
Молекулы гелия неполярны. Силы межмолекулярного взаимодействия между ними крайне невелики – меньше, чем в любом другом веществе. Отсюда – самые низкие значения критических величин, наинизшая температура кипения, наименьшие теплоты испарения и плавления. Что касается температуры плавления гелия, то при нормальном давлении ее вообще нет. Жидкий гелий при сколь угодно близкой к абсолютному нулю температуре не затвердевает, если, помимо температуры, на него но действует давление в 25 или больше атмосфер. Второго такого вещества в природе нет.
Нет также другого газа, столь ничтожно растворимого в жидкостях, особенно полярных, и так мало склонного к адсорбции, как гелий. Это наилучший среди газов проводник электричества и второй, после водорода, проводник тепла. Его теплоемкость очень велика, а вязкость мала.
Поразительно быстро проникает гелий сквозь тонкие перегородки из некоторых органических полимеров, фарфора, кварцевого и боросиликатного стекла. Любопытно, что сквозь мягкое стекло гелий диффундирует в 100 раз медленнее, чем сквозь боросиликатное. Гелий может проникать и через многие металлы. Полностью непроницаемы для него лишь железо и металлы платиновой группы, даже раскаленные.
На принципе избирательной проницаемости основан новый метод извлечения чистого гелия из природного газа.
Исключительный интерес проявляют ученые к жидкому гелию. Во-первых, это самая холодная жидкость, в которой к тому же не растворяется заметно ни одно вещество. Во-вторых, это самая легкая из жидкостей с минимальной величиной поверхностного натяжения.
При температуре 2,172°К происходит скачкообразное изменение свойств жидкого гелия. Образующаяся разновидность условно названа гелием II. Гелий II кипит совсем не так, как прочие жидкости, он не бурлит при кипении, поверхность его остается совершенно спокойной. Гелий II проводит тепло в 300 млн раз лучше, чем обычный жидкий гелий (гелий I). Вязкость гелия II практически равна нулю, она в тысячу раз меньше вязкости жидкого водорода. Поэтому гелий II обладает сверхтекучестью – способностью вытекать без трения через капилляры сколь угодно малого диаметра.
Другой стабильный изотоп гелия 3Не переходит в сверхтекучее состояние при температуре, отстоящей от абсолютного пуля всего на сотые доли градусов. Сверхтекучие гелий-4 и гелий-3 называют квантовыми жидкостями: в них проявляются квантово-механические эффекты еще до их отвердевания. Этим объясняется весьма детальная изученность жидкого гелия. Да и производят его ныне немало – сотни тысяч литров в год. А вот твердый гелий почти не изучен: велики экспериментальные трудности исследования этого самого холодного тела. Бесспорно, пробел этот будет заполнен, так как физики ждут много нового от познания свойств твердого гелия: ведь он тоже квантовое тело.
Инертный, но очень нужный
В конце прошлого века английский журнал «Панч» поместил карикатуру, на которой гелий был изображен хитро подмигивающим человечком – жителем Солнца. Текст под рисунком гласил: «Наконец-то меня изловили и на Земле! Это длилось достаточно долго! Интересно знать, сколько времени пройдет, пока они догадаются, что делать со мной?»
Действительно, прошло 34 года со дня открытия земного гелия (первое сообщение об этом было опубликовано в 1881 г.), прежде чем он нашел практическое применение. Определенную роль здесь сыграли оригинальные физико-технические, электрические и в меньшей мере химические свойства гелия, потребовавшие длительного изучения. Главными же препятствиями были рассеянность и высокая стоимость элемента №2.
Первыми гелий применили немцы. В 1915 г. они стали наполнять им свои дирижабли, бомбившие Лондон. Вскоре легкий, но негорючий гелий стал незаменимым наполнителем воздухоплавательных аппаратов. Начавшийся в середине 30-х годов упадок дирижаблестроения повлек некоторый спад в производстве гелия, но лишь на короткое время. Этот газ все больше привлекал к себе внимание химиков, металлургов и машиностроителей.
Многие технологические процессы и операции нельзя вести в воздушной среде. Чтобы избежать взаимодействия получаемого вещества (или исходного сырья) с газами воздуха, создают специальные защитные среды; и нет для этих целей более подходящего газа, чем гелий.
Инертный, легкий, подвижный, хорошо проводящий тепло гелий – идеальное средство для передавливания из одной емкости в другую легко воспламеняемых жидкостей и порошков; именно эти функции выполняет он в ракетах и управляемых снарядах. В гелиевой защитной среде проходят отдельные стадии получения ядерного горючего. В контейнерах, заполненных гелием, хранят и транспортируют тепловыделяющие элементы ядерных реакторов.
С помощью особых течеискателей, действие которых основано на исключительной диффузионной способности гелия, выявляют малейшие возможности утечки в атомных реакторах и других системах, находящихся под давлением или вакуумом.
Последние годы ознаменованы повторным подъемом дирижаблестроения, теперь на более высокой научно-технической основе. В ряде стран построены и строятся дирижабли с гелиевым наполнением грузоподъемностью от 100 до 3000 т. Они экономичны, надежны и удобны для транспортировки крупногабаритных грузов, таких, как плети газопроводов, нефтеочистительные установки, опоры линий электропередач и т.п. Наполнение из 85% гелия и 15% водорода огнебезопасно и только на 7% снижает подъемную силу в сравнении с водородным наполнением.
Начали действовать высокотемпературные ядерные реакторы нового типа, в которых теплоносителем служит гелий.
В научных исследованиях и в технике широко применяется жидкий гелий. Сверхнизкие температуры благоприятствуют углубленному познанию вещества и его строения – при более высоких температурах тонкие детали энергетических спектров маскируются тепловым движением атомов.
Уже существуют сверхпроводящие соленоиды из особых сплавов, создающие при температуре жидкого гелия сильные магнитные поля (до 300 тыс. эрстед) при ничтожных затратах энергии.
При температуре жидкого гелия многие металлы и сплавы становятся сверхпроводниками. Сверхпроводниковые реле – криотроны все шире применяются в конструкциях электронно-вычислительных машин. Они просты, надежны, очень компактны. Сверхпроводники, а с ними и жидкий гелий становятся необходимыми для электроники. Они входят в конструкции детекторов инфракрасного излучения, молекулярных усилителей (мазеров), оптических квантовых генераторов (лазеров), приборов для измерения сверхвысоких частот.
Конечно, этими примерами не исчерпывается роль гелия в современной технике. Но если бы не ограниченность природных ресурсов, не крайняя рассеянность гелия, он нашел бы еще множество применений. Известно, например, что при консервировании в среде гелия пищевые продукты сохраняют свой первоначальный вкус и аромат. Но «гелиевые» консервы пока остаются «вещью в себе», потому что гелия не хватает и применяют его лишь в самых важных отраслях промышленности и там, где без него никак не обойтись. Поэтому особенно обидно сознавать, что с горючим природным газом через аппараты химического синтеза, топки и печи проходят и уходят в атмосферу намного большие количества гелия, чем те, что добываются из гелиеносных источников.
Сейчас считается выгодным выделять гелий только в тех случаях, если его содержание в природном газе не меньше 0,05%. Запасы такого газа все время убывают, и не исключено, что они будут исчерпаны еще до конца нашего века. Однако, проблема «гелиевой недостаточности» к этому времени, вероятно, будет решена – частично за счет создания новых, более совершенных методов разделения газов, извлечения из них наиболее ценных, хотя и незначительных по объему фракций, и частично благодаря управляемому термоядерному синтезу. Гелий станет важным, хотя и побочным, продуктом деятельности «искусственных солнц».
Изотопы гелия
В природе существуют два стабильных изотопа гелия: гелий-3 и гелий-4. Легкий изотоп распространен на Земле в миллион раз меньше, чем тяжелый. Это самый редкий из стабильных изотопов, существующих на нашей планете. Искусственным путем получены еще три изотопа гелия. Все они радиоактивны. Период полураспада гелия-5 – 2,4·10–21 секунды, гелия-6 – 0,83 секунды, гелия-8 – 0,18 секунды. Самый тяжелый изотоп, интересный тем, что в его ядрах на один протон приходится три нейтрона, впервые подучен в Дубне в 60-х годах. Попытки получить гелий-10 пока были неудачны.
Последний твердый газ
В жидкое и твердое состояние гелий был переведен самым последним из всех газов. Особые сложности сжижения и отверждения гелия объясняются строением его атома и некоторыми особенностями физических свойств. В частности, гелий, как и водород, при температуре выше – 250°C, расширяясь, не охлаждается, а нагревается. С другой стороны, критическая температура гелия крайне низка. Именно поэтому жидкий гелий впервые удалось получить лишь в 1908, а твердый – в 1926 г.
Гелиевый воздух
Воздух, в котором весь азот или большая его часть заменена гелием, сегодня уже не новость. Его широко используют на земле, под землей и под водой.
Гелиевый воздух втрое легче и намного подвижнее обычного воздуха. Он активнее ведет себя в легких – быстро подводит кислород и быстро эвакуирует углекислый газ. Вот почему гелиевый воздух дают больным при расстройствах дыхания и некоторых операциях. Он снимает удушья, лечит бронхиальную астму и заболевания гортани.
Дыхание гелиевым воздухом практически исключает азотную эмболию (кессонную болезнь), которой при переходе от повышенного давления к нормальному подвержены водолазы и специалисты других профессий, работа которых проходит в условиях повышенного давления. Причина этой болезни – довольно значительная, особенно при повышенном давлении, растворимость азота в крови. По мере уменьшения давления он выделяется в виде газовых пузырьков, которые могут закупорить кровеносные сосуды, повредить нервные узлы... В отличие от азота, гелий практически нерастворим в жидкостях организма, поэтому он не может быть причиной кессонной болезни. К тому же гелиевый воздух исключает возникновение «азотного наркоза», внешне сходного с алкогольным опьянением.
Рано или поздно человечеству придется научиться подолгу жить и работать на морском дне, чтобы всерьез воспользоваться минеральными и пищевыми ресурсами шельфа. А на больших глубинах, как показали опыты советских, французских и американских исследователей, гелиевый воздух пока незаменим. Биологи доказали, что длительное дыхание гелиевым воздухом не вызывает отрицательных сдвигов в человеческом организме и не грозит изменениями в генетическом аппарате: гелиевая атмосфера не влияет на развитие клеток и частоту мутаций. Известны работы, авторы которых считают гелиевый воздух оптимальной воздушной средой для космических кораблей, совершающих длительные полеты во Вселенную. Но пока за пределы земной атмосферы искусственный гелиевый воздух еще не поднимался.
• Литий
• Оглавление
Дата публикации:
8 февраля 2002 года
n-t.ru
Данное оборудование указано в следующих разделах каталога:
Технические характеристики
Физические свойства
Требования и нормы к физико-химическим показателям гелия газообразногоГелий газообразный (сжатый) технический ТУ 0271-005-45905715-06Гелий газообразный (сжатый) очищенный ТУ 51-940-80 или ТУ 0271-135-31323949-2005 с изм.1
*Объемная доля гелия дана в пересчете на сухое вещество **Или суммарная объемная доля кислорода + аргона, не более 0,007% ***Или суммарная объемная доля кислорода + аргона, не более 0,0006% Гелий газообразный высокой чистоты ТУ 0271-001-45905715-02 с изм.1
*Объемная доля гелия дана в пересчете на сухое вещество Гелий газообразный перевозят в стальных баллонах (ГОСТ 949-73) коричневого цвета, с вентилями КВБ-53М или аналогичными, и специализированных контейнерах, предназначенных для перевозки гелия, всеми видами транспорта в соответствии с правилами перевозок грузов, действующими на данном виде транспорта. Жидкий гелий перевозят в специальных транспортных сосудах типа СТГ-25 и СТГ-40 светло-серого цвета объемом 25 и 40 литров соответственно. Сосуды с жидким гелием должны транспортироваться и храниться в вертикальном положении. Могут перевозиться железнодорожным, автомобильным и другими видами транспорта в соответствии с правилами перевозок грузов, действующими на данном виде транспорта. | ||||
granat-e.ru
Гелий
Ге́лий — второй порядковый элемент периодической системы химических элементов Д. И. Менделеева, с атомным номером 2. Расположен в главной подгруппе восьмой группы, первом периоде периодической системы. Возглавляет группу инертных газов в периодической таблице. Обозначается символом He (лат. Helium). Простое вещество гелий (CAS-номер: 7440-59-7) — инертный одноатомный газ без цвета, вкуса и запаха. Гелий — один из наиболее распространённых элементов во Вселенной, он занимает второе место после водорода. Также гелий является вторым по лёгкости (после водорода) химическим элементом. Гелий добывается из природного газа процессом низкотемпературного разделения — так называемой фракционной перегонкой
18 августа 1868 года французский учёный Пьер Жансен, находясь во время полного солнечного затмения в индийском городе Гунтур, впервые исследовал хромосферу Солнца. Жансену удалось настроить спектроскоп таким образом, чтобы спектр короны Солнца можно было наблюдать не только при затмении, но и в обычные дни. На следующий же день спектроскопия солнечных протуберанцев наряду с линиями водорода — синей, зелено-голубой и красной — выявила очень яркую жёлтую линию, первоначально принятую Жансеном и другими наблюдавшими её астрономами за линию D натрия. Жансен немедленно написал об этом во Французскую Академию наук. Впоследствии было установлено, что ярко-жёлтая линия в солнечном спектре не совпадает с линией натрия и не принадлежит ни одному из ранее известных химических элементов.
Спустя два месяца 20 октября английский астроном Норман Локьер, не зная о разработках французского коллеги, также провёл исследования солнечного спектра. Обнаружив неизвестную жёлтую линию с длиной волны 588 нм (более точно 587,56 нм), он обозначил её D3, так как она была очень близко расположена к Фраунгоферовым линиям D1 (589,59 нм) и D2 (588,99 нм) натрия. Спустя два года Локьер, совместно с английским химиком Эдвардом Франкландом, в сотрудничестве с которым он работал, предложил дать новому элементу название «гелий» (от др.-греч. ἥλιος — «солнце»).
Интересно, что письма Жансена и Локьера пришли во Французскую Академию наук в один день — 24 октября 1868 года, однако письмо Локьера, написанное им четырьмя днями ранее, пришло на несколько часов раньше. На следующий день оба письма были зачитаны на заседании Академии. В честь нового метода исследования протуберанцев Французская академия решила отчеканить медаль. На одной стороне медали были выбиты портреты Жансена и Локьера над скрещенными ветвями лавра, а на другой — изображение мифического бога Солнца Аполлона, правящего в колеснице четверкой коней, скачущей во весь опор.
В 1881 году итальянец Луиджи Пальмиери опубликовал сообщение об открытии им гелия в вулканических газах (фумаролах). Он исследовал светло-желтое маслянистое вещество, оседавшее из газовых струй на краях кратера Везувия. Пальмиери прокаливал этот вулканический продукт в пламени бунзеновской горелки и наблюдал спектр выделявшихся при этом газов. Ученые круги встретили это сообщение с недоверием, так как свой опыт Пальмиери описал неясно. Спустя многие годы в составе фумарол действительно были найдены небольшие количества гелия и аргона.
Только через 27 лет после своего первоначального открытия гелий был обнаружен на Земле — в 1895 году шотландский химик Уильям Рамзай, исследуя образец газа, полученного при разложении минерала клевеита, обнаружил в его спектре ту же ярко-жёлтую линию, найденную ранее в солнечном спектре. Образец был направлен для дополнительного исследования известному английскому ученому-спектроскописту Уильяму Круксу, который подтвердил, что наблюдаемая в спектре образца жёлтая линия совпадает с линией D3 гелия. 23 марта 1895 года Рамзай отправил сообщение об открытии им гелия на Земле в Лондонское королевское общество, а также во Французскую академию через известного химика Марселена Бертло.
В 1896 году Генрих Кайзер, Зигберт Фридлендер, а еще через два года Эдвард Бэли окончательно доказали присутствие гелия в атмосфере.
Еще до Рамзая гелий выделил также американский химик Фрэнсис Хиллебранд, однако он ошибочно полагал, что получил азот[6] и в письме Рамзаю признал за ним приоритет открытия. Исследуя различные вещества и минералы, Рамзай обнаружил, что гелий в них сопутствует урану и торию. Но только значительно позже, в 1906 году, Резерфорд и Ройдс установили, что альфа-частицы радиоактивных элементов представляют собой ядра гелия. Эти исследования положили начало современной теории строения атома.
Только в 1908 году нидерландскому физику Хейке Камерлинг-Оннесу удалось получить жидкий гелий дросселированием (см. Эффект Джоуля — Томсона), после того как газ был предварительно охлажден в кипевшем под вакуумом жидком водороде. Попытки получить твёрдый гелий еще долго оставались безуспешными даже при температуре в 0,71 K, которых достиг ученик Камерлинг-Оннеса — немецкий физик Виллем Хендрик Кеезом. Лишь в 1926 году, применив давление выше 35 атм и охладив сжатый гелий в кипящем под разрежением жидком гелии, ему удалось выделить кристаллы.
Только в 1908 году нидерландскому физику Хейке Камерлинг-Оннесу удалось получить жидкий гелий дросселированием (см. Эффект Джоуля — Томсона), после того как газ был предварительно охлажден в кипевшем под вакуумом жидком водороде. Попытки получить твёрдый гелий еще долго оставались безуспешными даже при температуре в 0,71 K, которых достиг ученик Камерлинг-Оннеса — немецкий физик Виллем Хендрик Кеезом. Лишь в 1926 году, применив давление выше 35 атм и охладив сжатый гелий в кипящем под разрежением жидком гелии, ему удалось выделить кристаллы.
В 1932 году Кеезом исследовал характер изменения теплоёмкости жидкого гелия с температурой. Он обнаружил, что около 2,19 K медленный и плавный подъём теплоёмкости сменяется резким падением и кривая теплоёмкости приобретает форму греческой буквы λ (лямбда). Отсюда температуре, при которой происходит скачок теплоёмкости, присвоено условное название «λ-точка». Более точное значение температуры в этой точке, установленное позднее — 2,172 K. В λ-точке происходят глубокие и скачкообразные изменения фундаментальных свойств жидкого гелия — одна фаза жидкого гелия сменяется в этой точке на другую, причем без выделения скрытой теплоты; имеет место фазовый переход II рода. Выше температуры λ-точки существует так называемый гелий-I, а ниже её — гелий-II.
В 1938 году советский физик Пётр Леонидович Капица открыл явление сверхтекучести жидкого гелия-II, которое заключается в резком снижении коэффициента вязкости, вследствие чего гелий течёт практически без трения. Вот что он писал в одном из своих докладов про открытие этого явления.
Происхождение названия
От греч. ἥλιος — «Солнце» (см. Гелиос). Любопытен тот факт, что в названии элемента было использовано характерное для металлов окончание «-ий» (по лат. «-um» — «Helium»), так как Локьер предполагал, что открытый им элемент является металлом. По аналогии с другими благородными газами логично было бы дать ему имя «гелион» («Helion»). В современной науке название «гелион» закрепилось за ядром лёгкого изотопа гелия — гелия-3.
Распространённость
Во Вселенной Гелий занимает второе место по распространённости во Вселенной после водорода — около 23 % по массе. Однако на Земле гелий редок. Практически весь гелий Вселенной образовался в первые несколько минут после Большого Взрыва, во время первичного нуклеосинтеза. В современной Вселенной почти весь новый гелий образуется в результате термоядерного синтеза из водорода в недрах звёзд (см. протон-протонный цикл, углеродно-азотный цикл). На Земле он образуется в результате альфа-распада тяжёлых элементов (альфа-частицы, излучаемые при альфа-распаде — это ядра гелия-4). Часть гелия, возникшего при альфа-распаде и просачивающегося сквозь породы земной коры, захватывается природным газом, концентрация гелия в котором может достигать 7 % от объёма и выше.. Земная кора В рамках восьмой группы гелий по содержанию в земной коре занимает второе место (после аргона). Содержание гелия в атмосфере (образуется в результате распада Ac, Th, U) — 5,27×10−4 % по объёму, 7,24×10−5 % по массе. Запасы гелия в атмосфере, литосфере и гидросфере оцениваются в 5×1014 м³. Гелионосные природные газы содержат как правило до 2 % гелия по объёму. Исключительно редко встречаются скопления газов, гелиеносность которых достигает 8 — 16 %. Среднее содержание гелия в земном веществе — 3 г/т. Наибольшая концентрация гелия наблюдается в минералах, содержащих уран, торий и самарий: клевеите, фергюсоните, самарските, гадолините, монаците (монацитовые пески в Индии и Бразилии), торианите. Содержание гелия в этих минералах составляет 0,8 — 3,5 л/кг, а в торианите оно достигает 10,5 л/кг
Определение
Качественно гелий определяют с помощью анализа спектров испускания (характеристические линии 587,56 нм и 388,86 нм), количественно — масс-спектрометрическими и хроматографическими методами анализа, а также методами, основанными на измерении физических свойств (плотности, теплопроводности и др.
Химические свойства
Гелий — наименее химически активный элемент восьмой группы таблицы Менделеева (инертные газы). Многие соединения гелия существуют только в газовой фазе в виде так называемых эксимерных молекул, у которых устойчивы возбуждённые электронные состояния и неустойчиво основное состояние. Гелий образует двухатомные молекулы He2+, фторид HeF, хлорид HeCl (эксимерные молекулы образуются при действии электрического разряда или ультрафиолетового излучения на смесь гелия с фтором или хлором). Известно химическое соединение гелия LiHe (возможно, имелось ввиду соединение LiHe7
Получение
В промышленности гелий получают из гелийсодержащих природных газов (в настоящее время эксплуатируются главным образом месторождения, содержащие > 0,1 % гелия). От других газов гелий отделяют методом глубокого охлаждения, используя то, что он сжижается труднее всех остальных газов. Охлаждение производят дросселированием в несколько стадий очищая его от CO2 и углеводородов. В результате получается смесь гелия, неона и водорода. Эту смесь, т. н. сырой гелий, (He — 70-90 % об.) очищают от водорода (4-5 %) с помощью CuO при 650—800 К. Окончательная очистка достигается охлаждением оставшейся смеси кипящим под вакуумом N2 и адсорбцией примесей на активном угле в адсорберах, также охлаждаемых жидким N2. Производят гелий технической чистоты (99,80 % по объёму гелий) и высокой чистоты (99,985 %). В России газообразный гелий получают из природного и нефтяного газов. В настоящее время гелий извлекается на гелиевом заводе ООО «Газпром добыча Оренбург» в Оренбурге из газа с низким содержанием гелия (до 0,055 % об.), поэтому российский гелий имеет высокую себестоимость. Актуальной проблемой является освоение и комплексная переработка природных газов крупных месторождений Восточной Сибири с высоким содержанием гелия (0,15-1 % об.), что позволит намного снизить его себестоимость. По производству гелия лидируют США (140 млн м³ в год), затем — Алжир (16 млн м³). Россия занимает третье место в мире — 6 млн м³ в год. Мировые запасы гелия составляют 45,6 млрд м³.
Источник: Википедия
Другие заметки по химии
edu.glavsprav.ru















