Азот (N): такой важный, такой нужный. Азот n
Азот (N) - это... Что такое Азот (N)?
АЗОТ — (N) химический элемент, газ, без цвета, вкуса и запаха; составляет 4/5 (79 %) воздуха; уд. вес 0,972; атомный вес 14; сгущается в жидкость при 140 °С. и давлении 200 атмосфер; составная часть многих растительных и животных веществ. Словарь… … Словарь иностранных слов русского языка
АЗОТ — АЗОТ, хим. элемент, симв. N (франц. AZ), порядковый номер 7, ат. в. 14,008; точка кипения 195,7°; 1 л А. при 0° и 760 мм давл. весит 1,2508 г [лат. Nitrogenium («порождающий селитру»), нем. Stickstoff («удушающее… … Большая медицинская энциклопедия
АЗОТ — (лат. Nitrogenium) N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067. Название от греческой a отрицательная приставка и zoe жизнь (не поддерживает дыхания и горения). Свободный азот состоит из 2 атомных… … Большой Энциклопедический словарь
азот — а м. azote m. <араб. 1787. Лексис.1. алхим. Первая материя металлов металлическая ртуть. Сл. 18. Пустился он <парацельс> на конец по свету, предлагая всем за весьма умеренную цену свой Лауданум и свой Азот, для изцеления всех возможных… … Исторический словарь галлицизмов русского языка
АЗОТ — (Nitrogenium), N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067; газ, tкип 195,80 шС. Азот основной компонент воздуха (78,09% по объему), входит в состав всех живых организмов (в организме человека… … Современная энциклопедия
Азот — (Nitrogenium), N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067; газ, tкип 195,80 °С. Азот основной компонент воздуха (78,09% по объему), входит в состав всех живых организмов (в организме человека… … Иллюстрированный энциклопедический словарь
Азот — (хим. знак N, атомный вес 14) один из химических элементов;бесцветный газ, не имеющий ни запаха, ни вкуса; очень мало растворим вводе. Удельный вес его 0.972. Пикте в Женеве и Кальете в Париже удалосьсгустить азот, подвергая его высокому давлению … Энциклопедия Брокгауза и Ефрона
Азот — N (лат. Nitrogenium * a. nitrogen; н. Stickstoff; ф. azote, nitrogene; и. nitrogeno), хим. элемент V группы периодич. системы Mенделеева, ат.н. 7, ат. м. 14,0067. Oткрыт в 1772 англ. исследователем Д. Pезерфордом. При обычных условиях A.… … Геологическая энциклопедия
АЗОТ — муж., хим. основание, главная стихия селитры; селитротвор, селитрород, селитряк; он же главная, по количеству, составная часть нашего воздуха (азота 79 объемов, кислорода 21). Азотистый, азотный, азотовый, азот в себе содержащий. Химики различают … Толковый словарь Даля
азот — органоген, нитроген Словарь русских синонимов. азот сущ., кол во синонимов: 8 • газ (55) • неметалл … Словарь синонимов
Азот — это газ, который гасит пламя, так как не горит и не поддерживает горения. Его получают фракционной перегонкой жидкого воздуха, хранят под давлением в стальных баллонах. Азот применяют, в основном, для производства аммиака и цианамида кальция, а… … Официальная терминология
metallurgicheskiy.academic.ru
Азот (N): такой важный, такой нужный
Азот — он же в таблице Менделеева N (он же — первая буква в аббревиатуре NPK на многочисленных упаковках с удобрениями).
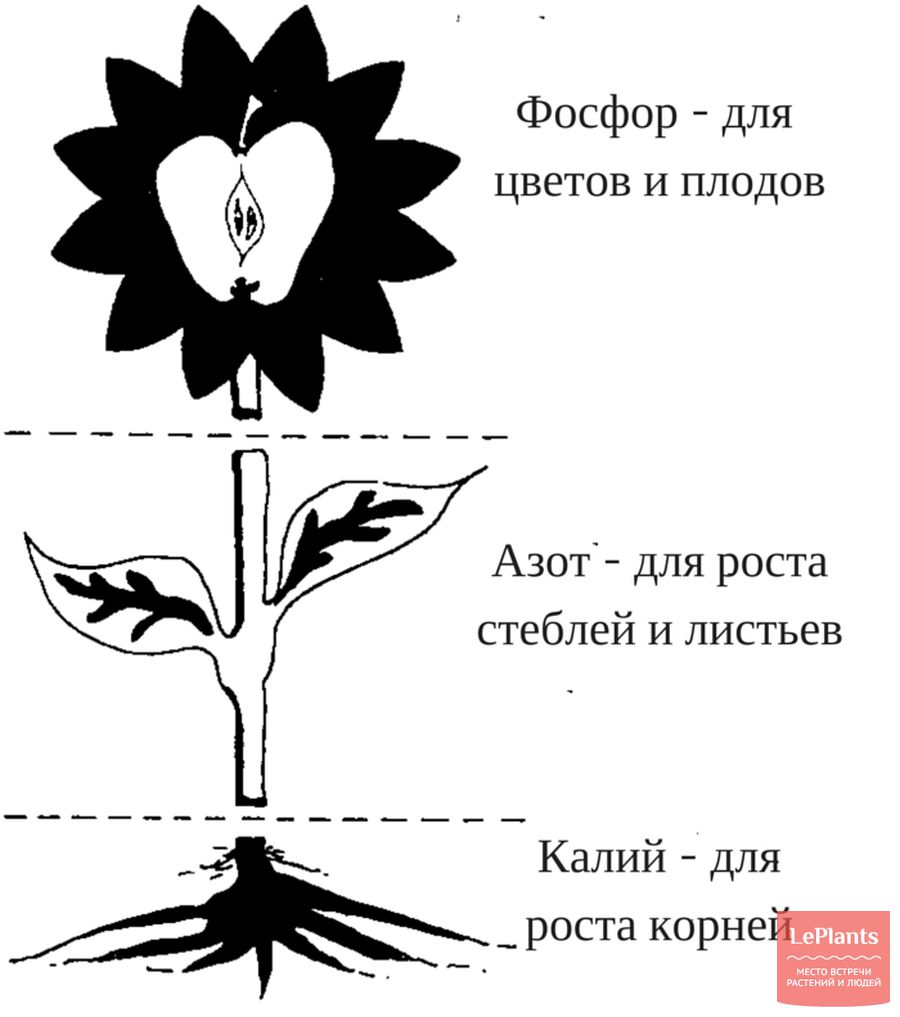 Прежде чем подробно разобрать роль и формы азота в удобрениях, нужно напомнить, что он относится к группе МАКРОэлементов. Это категория жизненно необходимых абсолютно всем растениям элементов, куда помимо азота входит фосфор P и калий K. МИКРОэлементы (железо, сера, цинк, марганец и другие) также играют важную роль, но они необходимы в дозировках в сотни раз меньше, чем макроэлементы (отсюда и название «микро»). Азот как и фосфор и калий напрямую участвуют в формировании основных тканей растения, отвечают за фазы развития (рост, вегетация, цветение, плодоношение) и скорость роста.
Прежде чем подробно разобрать роль и формы азота в удобрениях, нужно напомнить, что он относится к группе МАКРОэлементов. Это категория жизненно необходимых абсолютно всем растениям элементов, куда помимо азота входит фосфор P и калий K. МИКРОэлементы (железо, сера, цинк, марганец и другие) также играют важную роль, но они необходимы в дозировках в сотни раз меньше, чем макроэлементы (отсюда и название «микро»). Азот как и фосфор и калий напрямую участвуют в формировании основных тканей растения, отвечают за фазы развития (рост, вегетация, цветение, плодоношение) и скорость роста.
Зачем растению азот?
Если бы художник захотел нарисовать картинку благоухающего сада из элементов таблицы Менделеева, то вместо зелени листвы, стеблей и молодых побегов была бы буква N — азот. Именно этот летучий газ участвует через различные соединения в формировании хлорофилла — того самого белка, который принимает участие в фотосинтезе и дыхании растения. Если азота достаточно — листва имеет насыщенный изумрудный цвет, который вкупе с хорошим поливом может отливать глянцем. Как только азота становится мало, растение бледнеет вплоть до чахлой желтизны, а новые побеги растут медленно или практически прекращают рост.
Также принято считать, что за плодоношение отвечает фосфор, и именно его присутствие будет влиять на урожай. Это действительно так, но в большей степени в вопросе качества урожая. За количество будет отвечать азот. Чем больше вегетативной массы наберет растение, тем больше цветочных почек появится на стеблях или в пазухах. У некоторых растений азот напрямую влияет на формирование цветочных почек, особенно у двудомных с женскими и мужскими цветками (конопля, ива, лимонник, облепиха и многие другие).
Как понять, что растению не хватает азота?
Первый признак нехватки азота — чахлый, желтушный, вплоть до бледно-желтого, цвет листвы. Пожелтение начинается с краев листа по направлению к центру. При этом листовая пластинка утончается, становится мягкой, даже если соблюдается полив. Очень похожие симптомы наблюдаются при нехватке серы (S), однако в случае с азотом нижние листья желтеют первыми. В запущенных случаях они высыхают и опадают — растение «вытягивает» все питательные вещества из них, чтобы отдать верхним побегам или плодам, если они имеются. При нехватке серы опадения листвы снизу не наблюдается.
Причин нехватки может быть, как правило, две: или растение забыли подкормить (когда и как подкармливать — ниже) или грунт сильно закислен, и кислая реакция среды нарушает всасываемость азота. Также в кислой среде нехватка азота может мимикрировать под хлороз — недостаток железа или магния. Однако в данном случае это непринципиально — грунт требует решительной замены или обновления.
Какой азот продают в магазинах и какой из них лучше?
Для каждого садовода этот вопрос, пожалуй, самый главный. Однако давайте для начала разберемся, а какой в принципе азот бывает? Без этого будет трудно понять, что написано на упаковке.
Аммиачный или аммонийный азот (Nh5)
Этот азот еще называют органическим азотом. Его действительно много в органических остатках разлагающегося вещества будто то навоз или опавшая листва. Растения очень любят аммоний, так как он легко проникает в корни и в них же может превращаться с аминокислоты, которые и будут формировать листья и побеги растения. Однако есть существенный минус: несмотря на все механизмы сопротивления, аммоний может проникать в клетку растения и оказывать на нее токсичный эффект.
В природе передозировка аммонием довольно редка, т.к. он довольно быстро «преобразуется» бактериями до нитратов NO3 (процесс нитрификации) и далее до нитритов (NO2) и вплоть до чистого азота, который быстро улетучивается из почвы. В саду или огороде аммиачный азот также быстро покидает почву, если только владелец участка не применил чистый, свежий навоз в большом количестве. В этом случае и происходит т.н. «сжигание» корней или всего растения. В комнатных условиях органический азот следует использовать по-минимуму, т.к. проконтролировать нужную дозировку довольно сложно.
ВАЖНО: на упаковках удобрений для комнатных растений аммиачный азот крайне редко указывается формулой (Nh5) или формулировкой. Как правило, используется органическая форма: некий экстракт (например, экстракт водорослей) или жидкая форма чистого органического удобрения («биогумус»), или гелеобразная масса («сапропель» — донный ил) и т.д.

Для сада и огорода применяется минеральная форма — сульфат аммония (Nh5)2SO4. Большое преимущество этого удобрения в том, что оно также содержит серу. Вместе с азотом она участвует в синтезе важных аминокислот, включая незаменимые. Сульфат аммония входит в состав популярной сегодня марки удобрения «Акварин» (номера 6 и 7 подходят для сада и огорода). Это удобрение содержит приблизительно 25% аммонийного и 75% нитратного азота.
Нитратный азот (NO3)
Если органический азот растение старается сразу пустить в дело, не затрачивая энергии, то с нитратом картина совершенно противоположная. Практически любая культура жадно запасает нитраты в тканях в количествах порой превышающих допустимые пределы! А всему виной — высокая подвижность азота в биосфере. Сегодня коровка плюхнула лепешку, на нее тут же набрасываются бактерии (а чуть позже и насекомые), которые переводят азот из органической в минеральную форму NO3. Но и эта форма долго не задерживается: то, что не успели забрать растения, уже другие бактерии доводят до нитритной NO2 формы, а потом и до азота. Плюс нитрата — безвредность для растения. Минус — необходимость света и тепла, благодаря которым нитрат в листьях восстанавливается до аммония (точнее различных аминов Nh3) и далее — до аминокислот и белков. Как итог: в неблагоприятных условиях растение будет стремиться накапливать нитраты, чтобы использовать их, когда ситуация наладится.
В комнатных условиях нитратный азот — настоящее решение. Он указывается формулой на упаковке NO3 и сопровождается соответствующим текстом. Дозировки рассчитаны заранее для периодов покоя и активного роста. Ошибиться невозможно.
 В саду и огороде нитратный азот используется сразу после начала сокодвижения (что соответствует температуре почвы около +15°С). Важно не упустить этот момент и обеспечить растение элементом, из которого уже в самые ближайшие дни начнут строиться новые побеги и листья. Заканчивают применение азотных удобрений в июле, а точнее — сразу после завершения периода вегетации (деревья и кустарники замедляют рост, начинается плодоношение). В зиму сад отправляют без азотной подкормки или делают это поздней осенью, перед заморозками и органической формой, которая задержится в почве подольше. Также не забываем, что зимы в последнее время теплеют, что не лучшим образом сказывается на удержании азота в почве.
В саду и огороде нитратный азот используется сразу после начала сокодвижения (что соответствует температуре почвы около +15°С). Важно не упустить этот момент и обеспечить растение элементом, из которого уже в самые ближайшие дни начнут строиться новые побеги и листья. Заканчивают применение азотных удобрений в июле, а точнее — сразу после завершения периода вегетации (деревья и кустарники замедляют рост, начинается плодоношение). В зиму сад отправляют без азотной подкормки или делают это поздней осенью, перед заморозками и органической формой, которая задержится в почве подольше. Также не забываем, что зимы в последнее время теплеют, что не лучшим образом сказывается на удержании азота в почве.
В обиходе нитратный азот известен как селитра, из которой наиболее популярна в России — калийная (или «калиевая») селитра. Эта форма нитратного азота подходит как для садовых, так и для комнатных растений. Обеспечивает легкоусвояемым азотом и калием.
Амидный азот CO(Nh3)2, карбамид или просто мочевина
Богатое, биогенное (то есть полученное в том числе органическим путем) удобрение, которое может содержать до 46% азота. Для использования в грунте в последнее время используется редко, т.к. вездесущие «уреазные» бактерии быстро переводят драгоценную мочевину в карбонат аммония более известный в пищевой промышленности как разрыхлитель теста. Вот таким «разрыхлителем» в советские годы «удобряли» поля, пока не осознали потери азота. Сегодня мочевина используется в растворах для опрыскивания. Разумеется, лучшее ее применение – на полях и в больших садах. В частной практике применяется редко, поэтому и на полках обычных магазинов практически не встречается.
Мочевина — прекрасное средство против парши и некоторых других патогенных грибков.
Подробнее об использовании мочевины в качестве фунгицида читайте в нашей статье "Октябрь — пора приводить сад в порядок"
Подведем итог
- Азот — один из важнейших элементов, который постоянно необходим растению для здорового роста и развития.
- В комнатной культуре азотные удобрения добавляют в период активного роста. За месяц-полтора до покоя азотное питание прекращают, чтобы не вызвать избыточный рост и нарушение периода покоя.
- В садовой и огородной культуре азот добавляют весной, как только температура прогреется до +15°С (корни начинают впитывать влагу). Конец периода применения: середина лета; начало августа — только в случае холодной весны/лета.
- В комнатной культуре необходимо использовать нитратный азот: на упаковке будет написано NO3, возможно встретится только слово «нитрат».
- В садовой культуре, как правило, используются готовые марки удобрений, в которых смешаны нитратные и аммонийные формы азота. Оба указываются на упаковке формулами сульфата аммония и нитрата калия (чаще всего).
- Если вам попадется мочевина (карбамид), то используйте ее для опрыскивания растений. Период использования аналогичен другим формам азота.
leplants.ru
Азот N в Таблице Менделеева
Азот — это бесцветный газ, один из самых распространенных химических элементов на нашей планете, в таблице Менделеева обозначается символом N от лат. Nitrogenum, что означает безжизненный (azoos по-гречески). Еще в школе мы узнаем, что газообразный азот составляет 78 процентов земной атмосферы. Если положить его на одну чашу воображаемых весов, то на другую их чашу пришлось бы для равновесия взгромоздить 4 х 1015 тонн гирь.
Азот в виде его соединений играет колоссальную роль в жизни человечества. Земледельцы ежегодно вносят в почву огромное количество азотных удобрений. Содержащие азот соединения находят всевозрастающий спрос в промышленности — это красители, различные виды топлива, полимеры. Казалось бы, потребность легко удовлетворить за счет безбрежного океана атмосферы. Однако каждому школьнику хорошо известна инертность этого вещества: двухатомные молекулы, из которых состоит газообразный азот, при обычных условиях не реагируют практически ни с какими другими веществами.
Вместе с тем давно известно обстоятельство, которое заставляет химиков упорно искать новые пути. Это впервые установленная русским ученым С. Виноградским еще в 90-х годах XIX столетия биологическая фиксация азота некоторыми микроорганизмами, а также водорослями. Выходит, химическая инертность не мешает усвоению азота живыми организмами? Ведь они не могут при этом пользоваться высокими температурами и давлением. Значит, среди ферментов — биологических катализаторов, содержащихся в теле бактерий, — есть такие, которые позволяют превратить азот в белки при обычных температурах и давлениях в присутствии воды и кислорода.
Поразительным оказалось то, что активные к азоту системы не были уникальными. Со многими из них химики работали раньше и даже применяли в промышленных процессах.
Вслед за этим было сделано и другое открытие, рушившее психологический барьер в отношении азота. Ученые получили в итоге своеобразный комплекс рутения и азота: молекула газа в нем была прочно привязана к атому металла. Такие комплексы других молекул с соединениями металлов были известны ранее и широко изучались. Однако никто не ожидал, что с ионом металла могла так прочно связаться молекула «инертного» азота.
Ученым не удалось выяснить условий связывания свободного азота. Однако было установлено, что и свободный азот способен образовывать комплексы с соединениями рутения, причем иногда в присутствии воды и кислорода. Затем в разных странах мира начались интенсивные поиски, и выяснилось, что азот связывается в комплексы с рядом различных металлов.
Здесь оставалось снова только удивляться, почему ни комплексы азота, ни его реакции в растворах не были открыты ранее.
Тем временем ученые продвинулись дальше. Во-первых, удалось показать, что процесс можно ускорить — с помощью катализаторов связывать большие количества молекулярного азота. Во-вторых, открыли, что под действием соединений тех же переходных металлов свободный азот способен вступать в реакции с некоторыми органическими соединениями. Так был найден перспективный путь получения ценных химических веществ из молекулярного азота.
Теперь предстояло связать воедино два наметившихся направления — химию комплексов молекулярного азота и изучение реакции его восстановления. Ведь именно комплексообразование (как это было ранее найдено для других молекул) в принципе должно было «активировать» инертные молекулы газа. Однако в известных комплексах он оставался инертным. Длительная теоретическая и экспериментальная работа дала ответ на вопрос, какими должны быть комплексы, чтобы азот в них был химически активным. Естественно, здесь невозможно дать детальное описание разработанной теории. Но из нее, в частности, следует, что активные по отношению к дальнейшим реакциям комплексы могут наблюдаться не при обычных, а при пониженных температурах. Ученые стали выделять из растворов целый набор комплексов, в которых молекула азота активирована к дальнейшим реакциям.
Ободренные успехами исследователи попытались связать азот непосредственно в водном растворе, используя сравнительно слабые восстановители, — так, как это делают бактерии и водоросли. В поисках недостающих данных пришлось прибегнуть к помощи живой природы.
Уже было известно, что в ферментативных системах бактерий молекула азота активирует молибден и этот металл нельзя заменить никаким другим, кроме ванадия. Исследователи сосредоточили свое внимание на соединениях именно этих металлов, считая, что природа не случайно остановила на них свой выбор.
В 1970 году наконец получили результат, к которому исследователи стремились многие годы. Удалось открыть системы, которые фиксируют азот в присутствии соединений молибдена и ванадия в водных и водно-спиртовых средах. Основным конечным пунктом реакции, как оказалось, был почти исключительно гидразин. В несколько измененных условиях удавалось наблюдать и преимущественное образование аммиака.
Итак, еще одним парадоксом в химии стало меньше. Опровергнуто представление об инертности азота, открыты новые пути превращения огромных атмосферных «залежей» этого газа в продукты, нужные человеку.
www.alto-lab.ru
Популярная библиотека химических элементов. Раритетные издания. Наука и техника
Азот
| 7 | |
N |
5 2 |
| АЗОТ | |
| 14,0067 | |
| 2s22p3 | |
Всем известно: азот инертен. Часто мы сетуем за это на элемент №7, что естественно: слишком дорогой ценой приходится расплачиваться за его относительную инертность, слишком много энергии, сил и средств приходится тратить на его превращение в жизненно необходимые соединения.
Но, с другой стороны, не будь азот так инертен, в атмосфере произошли бы реакции азота с кислородом, и жизнь на пашей планете в тех формах, в которых она существует, стала бы невозможной. Растения, животные, мы с вами буквально захлебывались бы в потоках неприемлемых жизнью окислов и кислот. И «при всем при том» именно в окислы и азотную кислоту мы стремимся превратить возможно большую часть атмосферного азота. Это один из парадоксов элемента №7. (Здесь автор рискует быть обвиненным в тривиальности, ибо парадоксальность азота, вернее его свойств, стала притчей во языцех. И все же...)
Азот – элемент необыкновенный. Порою кажется, что чем больше мы о нем узнаем, тем непонятнее он становится. Противоречивость свойств элемента №7 отразилась даже в его названии, ибо ввела в заблуждение даже такого блистательного химика, как Антуан Лоран Лавуазье. Это Лавуазье предложил назвать азот азотом после того, как не первым и не последним получил и исследовал не поддерживающую дыхания и горения часть воздуха. Согласно Лавуазье, «азот» означает «безжизненный», и слово это произведено от греческого «а» – отрицание и «зоэ» – жизнь.
Термин «азот» бытовал еще в лексиконе алхимиков, откуда и заимствовал его французский ученый. Означал он некое «философское начало», своего рода кабалистическое заклинание. Знатоки утверждают, что ключом к расшифровке слова «азот» служит заключительная фраза из Апокалипсиса: «Я есть альфа и омега, начало и конец, первый и последний...» В средние века особо почитались три языка: латинский, греческий и древнееврейский. И слово «азот» алхимики составили из первой буквы «а» (а, альфа, алеф) и последних букв: «зет», «омега» и «тов» этих трех алфавитов. Таким образом, это таинственное синтетическое слово означало «начало и конец всех начал».
Современник и соотечественник Лавуазье Ж. Шапталь, не мудрствуя лукаво, предложил назвать элемент №7 гибридным латино-греческим именем «нитрогениум», что значит «селитру рождающий». Селитры – азотнокислые соли, вещества, известные с древнейших времен. (О них речь впереди.) Надо сказать, что термин «азот» укоренился только в русском и французском языках. По-английски элемент №7 – «Nitrogen», по-немецки – «Stockton» (удушающее вещество). Химический же символ N – дань шапталевскому нитрогениуму.
Кем открыт азот
Открытие азота приписывают ученику замечательного шотландского ученого Джозефа Блэка Даниелю Резерфорду, который в 1772 г. опубликовал диссертацию «О так называемом фиксируемом и мефитическом воздухе». Блэк прославился своими опытами с «фиксируемым воздухом» – углекислым газом. Он обнаружил, что после фиксирования углекислоты (связывания ее щелочью) остается еще какой-то «не фиксируемый воздух», который был назван «мефитическим» – испорченным – за то, что не поддерживал горения и дыхания. Исследование этого «воздуха» Блэк и предложил Резерфорду в качестве диссертационной работы.
Примерно в то же время азот был получен К. Шееле, Дж. Пристли, Г. Кавендишем, причем последний, как следовало из его лабораторных записей, изучал этот газ раньше Резерфорда, но, как всегда, не спешил с публикацией результатов своих трудов. Однако все эти выдающиеся ученые имели весьма смутное представление о природе открытого ими вещества. Они были убежденными сторонниками теории флогистона и связывали свойства «мефитического воздуха» с этой мнимой субстанцией. Только Лавуазье, ведя наступление на флогистон, убедился сам и убедил других, что газ, который он назвал «безжизненным», – простое вещество, как и кислород...
Вселенский катализатор?
Можно лишь догадываться, что означает «начало и конец всех начал» в алхимическом «азоте». Но об одном из «начал», связанных с элементом №7, можно говорить всерьез. Азот и жизнь – понятия неотделимые. По крайней мере, всякий раз, когда биологи, химики, астрофизики пытаются постичь «начало начал» жизни, то непременно сталкиваются с азотом.
Атомы земных химических элементов рождены в недрах звезд. Именно оттуда, от ночных светил и дневного светила, начинаются истоки нашей земной жизни. Это обстоятельство и имел в виду английский астрофизик У. Фаулер, говоря, что «все мы... являемся частичкой звездного праха»...
Звездный «прах» азота возникает в сложнейшей цепи термоядерных процессов, начальная стадия которых – превращение водорода в гелий. Это многостадийная реакция, идущая, как предполагают, двумя путями. Один из них, получивший название углеродно-азотного цикла, имеет самое непосредственное отношение к элементу №7. Этот цикл начинается, когда в звездном веществе, помимо ядер водорода – протонов, уже есть и углерод. Ядро углерода-12, присоединив еще один протон, превращается в ядро нестабильного азота-13:
126C + 11H → 137N + γ.
Но, испустив позитрон, азот снова становится углеродом – образуется более тяжелый изотоп 13С:
137N → 136C + е+ + γ.
Такое ядро, приняв лишний протон, превращается в ядро самого распространенного в земной атмосфере изотопа -14N.
136C + 11H → 147N + γ.
Увы, лишь часть этого азота отправляется в путешествие по Вселенной. Под действием протонов азот-14 превращается в кислород-15, а тот, в свою очередь, испустив позитрон и гамма-квант, превращается в другой земной изотоп азота – 15N:
147N + 11H → 158O + γ;
158O → 157N + е+ + γ.
Земной азот-15 стабилен, но и он в недрах звезды подвержен ядерному распаду; после того, как ядро 15N примет еще один протон, произойдет не только образование кислорода 16О, но и другая ядерная реакция:
157N + 11H → 126С + 42He.
В этой цепи превращений азот – один из промежуточных продуктов. Известный английский астрофизик Р.Дж. Тейлер пишет: «14N – изотоп, который нелегко построить. В углеродно-азотном цикле образуется азот, и, хотя впоследствии он снова превращается в углерод, все же если процесс протекает стационарно, то азота в веществе оказывается больше, чем углерода. Это, по-видимому, основной источник 14N»...
В умеренно сложном углеродно-азотном цикле прослеживаются любопытные закономерности. Углерод 12С играет в нем роль своеобразного катализатора. Судите сами, в конечном счете не происходит изменения количества ядер 12С. Азот же, появляясь в начале процесса, исчезает в конце... И если углерод в этом цикле – катализатор, то азот явно – аутокатализатор, т.е. продукт реакции, катализирующий ее дальнейшие промежуточные стадии.
Мы не случайно завели здесь речь о каталитических свойствах элемента №7. Но сохранил ли эту особенность звездный азот и в живом веществе? Катализаторы жизненных процессов – ферменты, и все они, равно как и большинство гормонов и витаминов, содержат азот.
Азот в атмосфере Земли
Жизнь многим обязана азоту, но и азот, по крайней мере атмосферный, своим происхождением обязан не столько Солнцу, сколько жизненным процессам. Поразительно несоответствие между содержанием элемента №7 в литосфере (0,01%) и в атмосфере (75,6% по массе или 78,09% по объему). В общем-то, мы обитаем в азотной атмосфере, умеренно обогащенной кислородом.
Между тем ни на других планетах солнечной системы, ни в составе комет или каких-либо других холодных космических объектов свободный азот не обнаружен. Есть его соединения и радикалы – CN*, NH*, NH*2, NH*3, а вот азота нет. Правда, в атмосфере Венеры зафиксировано около 2% азота, но эта цифра еще требует подтверждения. Полагают, что и в первичной атмосфере Земли элемента №7 не было. Откуда же тогда он в воздухе?
По-видимому, атмосфера нашей планеты состояла вначале из летучих веществ, образовавшихся в земных недрах: Н2, Н2О, СО2, СН4, Nh4. Свободный азот если и выходил наружу как продукт вулканической деятельности, то превращался в аммиак. Условия для этого были самые подходящие: избыток водорода, повышенные температуры – поверхность Земли еще не остыла. Так что же, значит, сначала азот присутствовал в атмосфере в виде аммиака? Видимо, так. Запомним это обстоятельство.
Но вот возникла жизнь... Владимир Иванович Вернадский утверждал, что «земная газовая оболочка, наш воздух, есть создание жизни». Именно жизнь запустила удивительнейший механизм фотосинтеза. Один из конечных продуктов этого процесса – свободный кислород стал активно соединяться с аммиаком, высвобождая молекулярный азот:
CO2 + 2Н2О → фотосинтез → НСОН + Н2О + О2;
4Nh4 + 3O2 → 2N2 + 6Н2О.
Кислород и азот, как известно, в обычных условиях между собой не реагируют, что и позволило земному воздуху сохранить «статус кво» состава. Заметим, что значительная часть аммиака могла раствориться в воде при образовании гидросферы.
В наше время основной источник поступления N2 в атмосферу – вулканические газы.
Если разорвать тройную связь...
Разрушив неисчерпаемые запасы связанного активного азота, живая природа поставила себя перед проблемой: как связать азот. В свободном, молекулярном состоянии он, как мы знаем, оказался весьма инертным. Виной тому – тройная химическая связь его молекулы: N≡N.
Обычно связи такой кратности малоустойчивы. Вспомним классический пример ацетилена: НС = СН. Тройная связь его молекулы очень непрочна, чем и объясняется невероятная химическая активность этого газа. А вот у азота здесь явная аномалия: его тройная связь образует самую стабильную из всех известных двухатомных молекул. Нужно приложить колоссальные усилия, чтобы разрушить эту связь. К примеру, промышленный синтез аммиака требует давления более 200 атм. и температуры свыше 500°C, да еще обязательного присутствия катализаторов... Решая проблему связывания азота, природе пришлось наладить непрерывное производство соединений азота методом гроз.
Статистика утверждает, что в атмосфере нашей планеты ежегодно вспыхивают три с лишним миллиарда молний. Мощность отдельных разрядов достигает 200 млн киловатт, а воздух при этом разогревается (локально, разумеется) до 20 тыс. градусов. При такой чудовищной температуре молекулы кислорода и азота распадаются на атомы, которые, легко реагируя друг с другом, образуют непрочную окись азота:
N2 + O2 → 2NО.
Благодаря быстрому охлаждению (разряд молнии длится десятитысячную долю секунды) окись азота не распадается и беспрепятственно окисляется кислородом воздуха до более стабильной двуокиси:
2NO + О2 → 2NO2.
В присутствии атмосферной влаги и капель дождя двуокись азота превращается в азотную кислоту:
3NO2 + h3O → 2HNO3 + NO.
Так, попав под свежий грозовой дождик, мы получаем возможность искупаться в слабом растворе азотной кислоты. Проникая в почву, атмосферная азотная кислота образует с ее веществами разнообразные естественные удобрения. Азот фиксируется в атмосфере и фотохимическим путем: поглотив квант света, молекула N2 переходит в возбужденное, активированное состояние и становится способной соединяться с кислородом...
Бактерии и азот
Из почвы соединения азота попадают в растения. Далее: «лошади кушают овес», а хищники – травоядных животных. По пищевой цепи идет круговорот вещества, в том числе и элемента №7. При этом форма существования азота меняется, он входит в состав все более сложных и нередко весьма активных соединений. Но не только «грозорожденный» азот путешествует по пищевым цепям..
Еще в древности было замечено, что некоторые растения, в частности бобовые, способны повышать плодородие почвы.
«...Или, как сменится год, золотые засеивай злакиТам, где с поля собрал урожай, стручками шумящий,Или где вика росла мелкоплодная с горьким лупином...»
Вчитайтесь: это же травопольная система земледелия! Строки эти взяты из поэмы Вергилия, написанной около двух тысяч лет назад.
Пожалуй, первым, кто задумался над тем, почему бобовые дают прибавки урожая зерновых, был французский агрохимик Ж. Буссенго. В 1838 г. он установил, что бобовые обогащают почву азотом. Зерновые же (и еще многие другие растения) истощают землю, забирая, в частности, все тот же азот. Буссенго предположил, что листья бобовых усваивают азот из воздуха, но это было заблуждением. В то время немыслимо было предположить, что дело не в самих растениях, а в особых микроорганизмах, вызывающих образование клубеньков на их корнях. В симбиозе с бобовыми эти организмы и фиксируют азот атмосферы. Сейчас это прописная истина...
В наше время известно довольно много различных азотфиксаторов: бактерии, актиномицеты, дрожжевые и плесневые грибки, сине-зеленые водоросли. И все они поставляют азот растениям. Но вот вопрос: каким образом без особых энергетических затрат расщепляют инертную молекулу N2 микроорганизмы? И почему одни из них обладают этой полезнейшей для всего живого способностью, а другие нет? Долгое время это оставалось загадкой. Тихий, без громов и молний механизм биологической фиксации элемента №7 был раскрыт лишь недавно. Доказано, что путь элементарного азота в живое вещество стал возможен благодаря восстановительным процессам, в ходе которых азот превращается в аммиак. Решающую роль при этом играет фермент нитрогеназа. Его центры, содержащие соединения железа и молибдена, активируют азот для «стыковки» с водородом, который предварительно активируется другим ферментом. Так из инертного азота получается весьма активный аммиак – первый стабильный продукт биологической азотфиксации.
Вот ведь как получается! Сначала процессы жизнедеятельности перевели аммиак первичной атмосферы в азот, а затем жизнь снова превратила азот в аммиак. Стоило ли природе на этом «ломать копья»? Безусловно, потому что именно так и возник круговорот элемента №7.
Залежи селитры и рост народонаселения
Природная фиксация азота молниями и почвенными бактериями ежегодно дает около 150 млн т. соединений этого элемента. Однако не весь связанный азот участвует в круговороте. Часть его выводится из процесса и отлагается в виде залежей селитры. Богатейшей такой кладовой оказалась чилийская пустыня Атакама в предгорьях Кордильер. Здесь годами не бывает дождей. Но изредка на склоны гор обрушиваются сильные ливни, вымывающие почвенные соединения. Потоки воды в течение тысячелетий выносили вниз растворенные соли, среди которых больше всего было селитры. Вода испарялась, соли оставались... Так возникло крупнейшее в мире месторождение азотных соединений.
Еще знаменитый немецкий химик Иоганн Рудольф Глаубер, живший в XVII в., отметил исключительную важность азотных солей для развития растений. В своих сочинениях, размышляя о круговороте азотистых веществ в природе, он употреблял такие выражения, как «нитрозные соки почвы» и «селитра – соль плодородия».
Но природную селитру в качестве удобрения стали применять лишь в начале прошлого века, когда стали разрабатывать чилийские залежи. В то время это был единственный значительный источник связанного азота, от которого, казалось, зависит благополучие человечества. Об азотной же промышленности тогда не могло быть и речи.
В 1824 г. английский священник Томас Мальтус провозгласил свою печально известную доктрину о том, что народонаселение растет гораздо быстрее, чем производство продуктов питания. В это время вывоз чилийской селитры составлял всего около 1000 т в год. В 1887 г. соотечественник Мальтуса, известный ученый Томас Гексли предсказал скорый конец цивилизации из-за «азотного голода», который должен наступить после выработки месторождений чилийской селитры (ее добыча к этому времени составляла уже более 500 тыс. т в год).
Через 11 лет еще один знаменитый ученый сэр Уильям Крукс заявил в Британском обществе содействия наукам, что не пройдет и полувека, как наступит продовольственный крах, если численность народонаселения не сократится. Он также аргументировал свой печальный прогноз тем, что «в скором времени предстоит полное истощение залежей чилийской селитры» со всеми отсюда вытекающими последствиями.
Пророчества эти не оправдались – человечество не погибло, а освоило искусственную фиксацию элемента №7. Более того, сегодня доля природной селитры – лишь 1,5% от мирового производства азотсодержащих веществ.
Как связывали азот
Соединения азота люди умели получать давно. Ту же селитру приготовляли в особых сараях – селитряницах, но очень уж примитивным был этот способ. «Выделывают селитру из куч навоза, золы, помета, оскребков кож, крови, картофельной ботвы. Кучи эти два года поливают мочою и переворачивают, после чего на них образуется налет селитры», – такое описание селитряного производства есть в одной старинной книге.
Источником соединений азота может служить и каменный уголь, в котором до 3% азота. Связанного азота! Этот азот стали выделять при коксовании углей, улавливая аммиачную фракцию и пропуская ее через серную кислоту.
Конечный продукт – сульфат аммония. Но и это, в общем-то, крохи. Трудно даже представить, какими путями развивалась бы наша цивилизация, не реши она вовремя проблему промышленно приемлемой фиксации атмосферного азота.
Впервые атмосферный азот связал еще Шееле. В 1775 г. он получил цианистый натрий, нагревая в атмосфере азота соду с углем:
Na2CO3 + 4С + N2 → 2NaCN + 3СО.
В 1780 г. Пристли установил, что объем воздуха, заключенный в сосуде, перевернутом над водой, уменьшается, если через него пропускать электрическую искру, а вода приобретает свойства слабой кислоты. Этот эксперимент был, как мы знаем (Пристли этого не знал), моделью природного механизма фиксации азота. Четыре года спустя Кавендиш, пропуская электрический разряд через воздух, заключенный в стеклянной трубке со щелочью, обнаружил там селитру.
И хотя все эти эксперименты не могли в то время выйти за пределы лабораторий, в них виден прообраз промышленных способов фиксации азота – цианамидного и дугового, появившихся на рубеже XIX...XX вв.
Цианамидный способ был запатентован в 1895 г. немецкими исследователями А. Франком и Н. Каро. По этому способу азот при нагревании с карбидом кальция связывался в цианамид кальция:
CaC2 + N2 → Ca(CN)2.
В 1901 г. сын Франка, подав идею о том, что цианамид кальция может служить хорошим удобрением, по существу, положил начало производству этого вещества. Росту индустрии связанного азота способствовало появление дешевой электроэнергии. Наиболее перспективным способом фиксации атмосферного азота в конце XIX в. считался дуговой, при помощи электрического разряда. Вскоре после строительства Ниагарской электростанции американцы неподалеку пустили (в 1902 г.) первый дуговой завод. Через три года в Норвегии вступила в строй дуговая установка, разработанная теоретиком и специалистом по изучению северного сияния X. Биркеландом и инженером-практиком С. Эйде. Заводы подобного типа получили широкое распространение; селитру, которую они выпускали, называли норвежской. Однако расход электроэнергии при этом процессе был чрезвычайно велик и составлял до 70 тыс. киловатт/час на тонну связанного азота, причем только 3% этой энергии использовалось непосредственно на фиксацию.
Через аммиак
Перечисленные выше способы фиксации азота были лишь подходами к методу, появившемуся незадолго до первой мировой войны. Это о нем американский популяризатор науки Э. Слоссон весьма остроумно заметил: «Всегда говорилось, что англичане господствуют на море, а французы – на суше, немцам же остается только воздух. К этой шутке немцы отнеслись как будто бы серьезно и принялись использовать воздушное царство для нападения на англичан и французов... Кайзер... обладал целым флотом цеппелинов и таким способом фиксации азота, который не был известен никакой другой нации. Цеппелины разрывались, как мешки с воздухом, но заводы, фиксирующие азот, продолжали работать и сделали Германию независимой от Чили не только в годы войны, но и в мирное время»... Речь идет о синтезе аммиака – основном процессе современной индустрии связанного азота.
Слоссон был не совсем прав, говоря о том, что способ фиксации азота в аммиак не был известен нигде, кроме Германии. Теоретические основы этого процесса были заложены французскими и английскими учеными. Еще в 1784 г. знаменитый К. Бертолле установил состав аммиака и высказал мысль о химическом равновесии реакций синтеза и разложения этого вещества. Через пять лет англичанином У. Остином была предпринята первая попытка синтеза Nh4 из азота и водорода. И, наконец, французский химик А. Ле Шателье, отчетливо сформулировав принцип подвижного равновесия, первым синтезировал аммиак. При этом он применил высокое давление и катализаторы – губчатую платину и железо. В 1901 г. Ле Шателье запатентовал этот способ.
Исследования по синтезу аммиака в начале века проводили также Э. Перман и Г. Аткинс в Англии. В своих экспериментах эти исследователи в качестве катализаторов применяли различные металлы, в частности медь, никель и кобальт...
Но наладить синтез аммиака из водорода и азота в промышленных масштабах впервые удалось, действительно, в Германии. В этом заслуга известного химика Фрица Габера. В 1918 г. он был удостоен Нобелевской премии по химии.
Технология производства Nh4, разработанная немецким ученым, очень сильно отличалась от других производств того времени. Здесь впервые был применен принцип замкнутого цикла с непрерывно действующей аппаратурой и утилизацией энергии. Окончательную разработку технологии синтеза аммиака завершил коллега и друг Габера К. Бош, который в 1931 г. также был удостоен Нобелевской премии – за развитие методов химического синтеза при высоких давлениях.
По пути природы
Синтез аммиака стал еще одной моделью природной фиксации элемента №7. Напомним, что микроорганизмы связывают азот именно в Nh4. При всех достоинствах процесса Габера – Боша он выглядит несовершенным и громоздким по сравнению с природным!
«Биологическая фиксация атмосферного азота... была неким парадоксом, постоянным вызовом для химиков, своего рода демонстрацией недостаточности наших знаний». Эти слова принадлежат советским химикам М.Е. Вольпину и А.Е. Шилову, которые предприняли попытку фиксации молекулярного азота в мягких условиях.
Сначала были неудачи. Но в 1964 г. в Институте элементоорганических соединении АН СССР, в лаборатории Вольпина, было сделано открытие: в присутствии соединений переходных металлов – титана, ванадия, хрома, молибдена и железа – элемент №7 активируется и при обычных условиях образует комплексные соединения, разлагаемые водой до аммиака. Именно эти металлы служат и центрами фиксации азота в ферментах азотфиксаторов, и прекрасными катализаторами в производстве аммиака.
Вскоре после этого канадские ученые А. Аллен и К. Зеноф, исследуя реакцию гидразина N2h3 с треххлористым рутением, получили химический комплекс, в котором, опять же в мягких условиях, азот оказался связанным. Этот результат настолько противоречил обычным представлениям, что редакция журнала, куда исследователи послали свою статью с сенсационным сообщением, отказалась ее печатать. В дальнейшем советским ученым удалось в мягких условиях получить и азотсодержащие органические вещества. Пока еще рано говорить о промышленных способах мягкой химической фиксации атмосферного азота, однако, достигнутые успехи позволяют предвидеть надвигающуюся революцию в технологии связывания элемента №7.
Современной наукой не забыты и старые способы получения азотных соединений через окислы. Здесь главные усилия направлены на разработку технологических процессов, ускоряющих расщепление молекулы N2 на атомы. Наиболее перспективными направлениями окисления азота считают сжигание воздуха в специальных печах, применение плазмотронов, использование для этих целей пучка ускоренных электронов.
Чего бояться?
Сегодня нет оснований опасаться, что человечество когда-либо будет испытывать недостаток в соединениях азота. Промышленная фиксация элемента №7 прогрессирует невероятными темпами. Если в конце 60-х годов мировое производство связанного азота составляло 30 млн т., то к началу будущего века оно, по всей вероятности, достигнет миллиарда тонн!
Такие успехи не только радуют, но и вызывают опасения. Дело в том, что искусственная фиксация N2 и внесение в почву огромного количества азотсодержащих веществ – самое грубое и значительное вмешательство человека в естественный круговорот веществ. В наше время азотные удобрения не только вещества плодородия, но и загрязнители окружающей среды. Они вымываются из почвы в реки и озера, вызывают вредное цветение водоемов, разносятся воздушными потоками на дальние расстояния...
В подземные воды уходит до 13% азота, содержащегося в минеральных удобрениях. Азотные соединения, особенно нитраты, вредны для людей и могут быть причиной отравлений. Вот вам и кормилец-азот!
Всемирная организация здравоохранения (ВОЗ) приняла предельно допустимую концентрацию нитратов в питьевой воде: 22 мг/л для умеренных широт и 10 мг/л для тропиков. В СССР санитарные нормы регламентируют содержание нитратов в воде водоемов по «тропическим» меркам – не более 10 мг/л. Выходит, что нитраты средство «обоюдоострое»...
4 октября 1957 г. человечество еще раз вмешалось в круговорот элемента №7, запустив в космос «шарик», заполненный азотом, – первый искусственный спутник...
Менделеев об азоте
«Хотя деятельнейшую, т.е. наиболее легко и часто химически действующую часть окружающего нас воздуха, составляет кислород, но наибольшую массу его, судя как по объему, так и по весу, образует азот; а именно газообразный азот составляет более 3/4, хотя и менее 4/5 объема воздуха. А так как азот лишь немногим легче кислорода, то весовое содержание азота в воздухе составляет около 3/4 всей его массы. Входя в таком значительном количестве в состав воздуха, азот, по-видимому, не играет особо видной роли в атмосфере, химическое действие которой определяется преимущественно содержанием в ней кислорода. Но правильное представление об азоте получается только тогда, когда узнаем, что в чистом кислороде животные не могут долго жить, даже умирают, и что азот воздуха, хотя лишь медленно и мало-помалу, образует разнообразные соединения, часть которых играет важнейшую роль в природе, особенно в жизни организмов».
Где применяют азот
Азот – самый дешевый из всех газов, химически инертных в обычных условиях. Его широко применяют в химической технологии для создания неокислительных сред. В лабораториях в атмосфере азота хранят легко окисляющиеся соединения. Выдающиеся произведения живописи иногда (в хранилищах или при транспортировке) помещают в герметические футляры, заполненные азотом, – чтобы предохранить краски от влаги и химически активных компонентов воздуха.
Значительной бывает роль азота в металлургии и при металлообработке. Различные металлы в расплавленном состоянии реагируют на присутствие азота по-разному. Медь, например, абсолютно инертна по отношению к азоту, поэтому изделия из меди часто сваривают в струе этого газа. Магний, напротив, при горении на воздухе дает соединения не только с кислородом, но и с азотом. Так что для работы с изделиями из магния при высоких температурах азотная среда неприменима. Насыщение азотом поверхности титана придает металлу большую прочность и износостойкость – на ней образуется очень прочный и химически инертный нитрид титана. Эта реакция идет лишь при высоких температурах.
При обыкновенной температуре азот активно реагирует только с одним металлом – литием.
Наибольшее количество азота идет на производство аммиака.
Азотный наркоз
Распространенное мнение о физиологической инертности азота не совсем правильно. Азот физиологически инертен при обычных условиях.
При повышенном давлении, например при погружении водолазов, растет концентрация растворенного азота в белковых и особенно жировых тканях организма. Это приводит к так называемому азотному наркозу. Водолаз словно пьянеет: нарушается координация движений, мутится сознание. В том, что причина этого – азот, ученые окончательно убедились после проведения экспериментов, в которых вместо обычного воздуха в скафандр водолаза подавалась гелио-кислородная смесь. При этом симптомы наркоза исчезли.
Космический аммиак
Большие планеты солнечной системы Сатурн и Юпитер состоят, как полагают астрономы, частично из твердого аммиака. Аммиак замерзает при –78°C, а на поверхности Юпитера, например, средняя температура – 138°C.
Аммиак и аммоний
В большой семье азота есть странное соединение – аммоний Nh5. В свободном виде он нигде не встречается, а в солях играет роль щелочного металла. Название «аммоний» предложил в 1808 г. знаменитый английский химик Хэмфри Дэви. Латинское слово ammonium когда-то означало: соль из Аммонии. Аммония – область в Ливии. Там находился храм египетского бога Аммона, по имени которого и называли всю область. В Аммонии издавна получали аммонийные соли (в первую очередь нашатырь), сжигая верблюжий навоз. При распаде солей получался газ, который сейчас называют аммиаком.
С 1787 г. (в том самом году, когда был принят термин «азот») комиссия по химической номенклатуре дала этому газу имя ammoniaque (аммониак). Русскому химику Я.Д. Захарову это название показалось слишком длинным, и в 1801 г. он исключил из него две буквы. Так получился аммиак.
Веселящий газ
Из пяти окислов азота два – окись (NO) и двуокись (NO2) – нашли широкое промышленное применение. Два других – азотистый ангидрид (N2O3) и азотный ангидрид (N2O5) – не часто встретишь и в лабораториях. Пятый – закись азота (N2O). Она обладает весьма своеобразным физиологическим действием, за которое ее часто называют веселящим газом.
Выдающийся английский химик Хэмфри Дэви с помощью этого газа устраивал специальные сеансы. Вот как описывал действие закиси азота один из современников Дэви: «Одни джентльмены прыгали по столам и стульям, у других развязались языки, третьи обнаружили чрезвычайную склонность к потасовке».
Свифт смеялся напрасно
Выдающийся писатель-сатирик Джонатан Свифт охотно издевался над бесплодием современной ему науки. В «Путешествиях Гулливера», в описании академии Лагадо, есть такое место: «В его распоряжении были две большие комнаты, загроможденные самыми удивительными диковинами; пятьдесят помощников работали под его руководством. Одни сгущали воздух в сухое плотное вещество, извлекая из него селитру...»
Сейчас селитра из воздуха – вещь абсолютно реальная. Аммиачную селитру Nh5NO3 действительно делают из воздуха и воды.
Бактерии связывают азот
Идею о том, что некоторые микроорганизмы могут связывать азот воздуха, первым высказал русский физик П. Коссович. Русскому биохимику С.Н. Виноградскому первому удалось выделить из почвы один вид бактерий, связывающих азот.
Растения разборчивы
Дмитрий Николаевич Прянишников установил, что растение, если ему предоставлена возможность выбора, предпочитает аммиачный азот нитратному. (Нитраты – соли азотной кислоты).
Важный окислитель
Азотная кислота HNO3 – один из самых важных окислителей, применяемых в химической промышленности. Первым ее приготовил, действуя серной кислотой на селитру, один из крупнейших химиков XVII в. Иоганн Рудольф Глаубер.
Среди соединений, получаемых сейчас с помощью азотной кислоты, многие совершенно необходимые вещества: удобрения, красители, полимерные материалы, взрывчатые вещества.
Двойная роль
Некоторые азотсодержащие соединения, применяемые в агрохимии, выполняют двоякие функции. Например, цианамид кальция хлопкоробы применяют как дефолиант – вещество, вызывающее опадение листьев перед уборкой урожая. Но это соединение одновременно служит и удобрением.
Азот в ядохимикатах
Далеко не все вещества, в состав которых входит азот, способствуют развитию любых растений. Аминные соли феноксиуксусной и трихлорфеноксиуксусной кислот – гербициды. Первая подавляет рост сорняков на полях злаковых культур, вторая применяется для очистки земель под пашни – уничтожает мелкие деревья и кустарники.
Полимеры: от биологических до неорганических
Атомы азота входят в состав многих природных и синтетических полимеров – от белка до капрона. Кроме того, азот – важнейший элемент безуглеродных, неорганических полимеров. Молекулы неорганического каучука – полифосфонитрилхлорида – это замкнутые циклы, составленные из чередующихся атомов азота и фосфора, в окружении ионов хлора. К неорганическим полимерам относятся и нитриды некоторых металлов, в том числе и самое твердое из всех веществ – боразон.
• Кислород
• Оглавление
Дата публикации:
17 февраля 2002 года
n-t.ru
АЗОТ - это... Что такое АЗОТ?
АЗОТ — (N) химический элемент, газ, без цвета, вкуса и запаха; составляет 4/5 (79 %) воздуха; уд. вес 0,972; атомный вес 14; сгущается в жидкость при 140 °С. и давлении 200 атмосфер; составная часть многих растительных и животных веществ. Словарь… … Словарь иностранных слов русского языка
АЗОТ — АЗОТ, хим. элемент, симв. N (франц. AZ), порядковый номер 7, ат. в. 14,008; точка кипения 195,7°; 1 л А. при 0° и 760 мм давл. весит 1,2508 г [лат. Nitrogenium («порождающий селитру»), нем. Stickstoff («удушающее… … Большая медицинская энциклопедия
АЗОТ — (лат. Nitrogenium) N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067. Название от греческой a отрицательная приставка и zoe жизнь (не поддерживает дыхания и горения). Свободный азот состоит из 2 атомных… … Большой Энциклопедический словарь
азот — а м. azote m. <араб. 1787. Лексис.1. алхим. Первая материя металлов металлическая ртуть. Сл. 18. Пустился он <парацельс> на конец по свету, предлагая всем за весьма умеренную цену свой Лауданум и свой Азот, для изцеления всех возможных… … Исторический словарь галлицизмов русского языка
Азот — (Nitrogenium), N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067; газ, tкип 195,80 °С. Азот основной компонент воздуха (78,09% по объему), входит в состав всех живых организмов (в организме человека… … Иллюстрированный энциклопедический словарь
Азот — (хим. знак N, атомный вес 14) один из химических элементов;бесцветный газ, не имеющий ни запаха, ни вкуса; очень мало растворим вводе. Удельный вес его 0.972. Пикте в Женеве и Кальете в Париже удалосьсгустить азот, подвергая его высокому давлению … Энциклопедия Брокгауза и Ефрона
Азот — N (лат. Nitrogenium * a. nitrogen; н. Stickstoff; ф. azote, nitrogene; и. nitrogeno), хим. элемент V группы периодич. системы Mенделеева, ат.н. 7, ат. м. 14,0067. Oткрыт в 1772 англ. исследователем Д. Pезерфордом. При обычных условиях A.… … Геологическая энциклопедия
АЗОТ — муж., хим. основание, главная стихия селитры; селитротвор, селитрород, селитряк; он же главная, по количеству, составная часть нашего воздуха (азота 79 объемов, кислорода 21). Азотистый, азотный, азотовый, азот в себе содержащий. Химики различают … Толковый словарь Даля
азот — органоген, нитроген Словарь русских синонимов. азот сущ., кол во синонимов: 8 • газ (55) • неметалл … Словарь синонимов
Азот — это газ, который гасит пламя, так как не горит и не поддерживает горения. Его получают фракционной перегонкой жидкого воздуха, хранят под давлением в стальных баллонах. Азот применяют, в основном, для производства аммиака и цианамида кальция, а… … Официальная терминология
dic.academic.ru