Оксиды углерода: химия, 8 класс. Химическая формула углекислого газа
Содержание углекислого газа в атмосфере, химическая формула и влияние на состояние человека
Деятельность человека достигла уже таких масштабов, что общее содержание углекислого газа в атмосфере Земли достигло предельно допустимых значений. Природные системы – суша, атмосфера, океан, находятся под разрушительным воздействием.
Важные факты
Содержание углекислого газа в атмосфере Земли за последнее столетие постоянно увеличивается. Помимо СО2 туда поступают и другие газы, которые не относятся с естественным компонентам глобальной экологической системы.
Например, к ним относятся фторхлоруглеводороды. Эти примеси газов излучают и поглощают солнечную радиацию, что отражается на климате планеты. В совокупности СО2, иные газообразные соединения, оказывающиеся в атмосфере, называют парниковыми газами.

Историческая справка
Каково содержание углекислого газа в атмосфере? Над этим вопросом задумывался в свое время еще Сванте Аррениус. Ему удалось доказать зависимость между выбросами диоксида углерода и изменениями климата. Ученый указал на то, что при сжигании полезных ископаемых содержание углекислого газа в атмосфере резко возрастает.
Он предупреждал о том, что увеличение объемов сжигаемого топлива может привести к нарушению радиационного баланса Земли.
Современные реалии
Сегодня большее количество диоксида углерода в атмосферу поступает при сжигании топлива, а также в связи с теми изменениями, что происходят в природе из-за вырубки лесных угодий, увеличения площадей сельскохозяйственных угодий.

Механизм воздействия диоксида углерода на живую природу
Повышение содержания углекислого газа в атмосфере вызывает парниковый эффект. Если при коротковолновой солнечной радиации оксид углерода (IV) прозрачен, то длинноволновую радиацию он поглощает, излучая энергию по всем направлениям. В результате содержание углекислого газа в атмосфере существенно увеличивается, нагревается поверхность Земли, горячими становятся нижние слои атмосферы. При последующем увеличении количества диоксида углерода возможно глобальное изменение климата.
Именно поэтому важно прогнозировать общее содержание углекислого газа в атмосфере Земли.
Источники попадания в атмосферу
Среди них можно выделить промышленные выбросы. Содержание углекислого газа в атмосфере возрастанием в связи с антропогенными выбросами. Экономический рост напрямую зависит от количества сжигаемых природных ископаемых, так как многие производства являются энергозатратными предприятиями.
Результаты статистических исследований свидетельствуют о том, что с конца прошлого века во многих странах происходит снижение удельных затрат энергии при существенном росте цен на электроэнергию.
Эффективное ее использование достигается благодаря модернизации технологического процесса, транспортных средств, использованию новых технологий в строительстве производственных цехов. Некоторые развитые промышленные страны перешли от развития перерабатывающей и сырьевой отрасли к развитию тех направлений, которые занимаются изготовлением конечного продукта.
Содержание углекислого газа в атмосфере в процентах не является постоянной величиной. При минимальном развитии производственной базы, наличии густого лесного массива, оно имеет минимальные показатели.
В крупных мегаполисах, обладающих серьезной производственной базой, выбросы диоксида углерода в атмосферу существенно выше, поскольку СО2 часто является побочным продуктом отраслей, деятельность которых удовлетворяет запросы образования, медицины.
В развивающихся странах существенный рост использования высококачественного топлива на 1 жителя, считается серьезным фактором для перехода на более высокий уровень жизни. В настоящее время выдвигается идея, согласно которой продолжение экономического роста и повышение уровня жизни возможно без увеличения количества сжигаемого топлива.
В зависимости от региона содержание углекислого газа в атмосфере составляет от 10 до 35 %.

Связь между потребляемой энергией и выбросами СО2
Начнем с того, что энергия не производится только ради ее получения. В развитых промышленных странах большая ее часть используется в промышленности, для обогрева и охлаждения зданий, для транспорта. Исследования, проводимые крупными научными центрами, показали, что при использовании энергосберегающих технологий можно получить существенное снижение выбросов диоксида углерода в земную атмосферу.
Например, ученым удалось посчитать, что если бы США перешли на менее энергоемкие технологии при производстве товаров народного потребления, это бы позволило снизить количество углекислого газа, попадающего в атмосферу, на 25 %. В масштабах земного шара это позволило бы снизить проблему парникового эффекта на 7 %.
Углерод в природе
Анализируя проблему, касающуюся выбросов диоксида углерода в атмосферу Земли, отметим, что углерод, который входит в его состав, является жизненно важным для существования биологических организмов. Его способность образовывать сложные углеродные цепочки (ковалентные связи) приводит к появлению белковых молекул, необходимых для жизни. Биогенный цикл углерода является сложным процессом, поскольку в него входит не просто функционированием живых существ, но и перенос неорганических соединений между разными резервуарами углерода, а также внутри них.
К ним относится атмосфера, континентальная масса, в том числе почвы, а также гидросфера, литосфера. На протяжении двух последних столетий в системе биофера-атмосфера-гидросфера наблюдаются изменения потоков углерода, который по своей интенсивности существенно превышают скорость протекания геологических процессов переноса данного элемента. Именно поэтому нужно ограничиваться рассмотрением взаимоотношений внутри системы, включая и почву.
Серьезные исследования, касающиеся определения количественного содержания углекислого газа в земной атмосфере, стали проводиться с середины прошлого века. Первопроходцем в таких вычислениях стал Киллинг, работающий в известной обсерватории Мауна-Лоа.
Анализ наблюдений показал, что на изменения концентрации диоксида углерода в атмосфере влияет цикл фотосинтеза, деструкция растений на суше, а также годовое изменение температуры в Мировом океане. В ходе экспериментов удалось выяснить, что количественное содержание углекислого газ в северном полушарии существенно выше. Ученые предположили, что это связно с тем, что большая часть антропогенного поступления приходится именно на это земное полушарие.
Для проведения анализа были взяты пробы воздуха без специальных методик, кроме того не учитывалась относительная и абсолютная погрешность вычислений. Благодаря анализу пузырьков воздуха, которые содержались в ледниковых кернах, исследователям удалось установить данные по содержанию в земной атмосфере углекислого газа в диапазоне 1750-1960 гг.

Заключение
На протяжении последних столетий произошли существенные изменения в континентальных экосистемах, причиной стало увеличение антропогенного воздействия. При повышении количественного содержания углекислого газа в атмосфере нашей планеты, возрастает парниковый эффект, что негативно отражается на существовании живых организмов. Именно поэтому важно переходить на энергосберегающие технологии, которые позволяют снижать поступление СО2 в атмосферу.
fb.ru
химия, 8 класс :: SYL.ru
Все, что нас окружает, состоит из соединений различных химических элементов. Мы дышим не просто воздухом, а сложным органическим соединением, имеющим в своем составе кислород, азот, водород, двуокись углерода и другие необходимые составляющие. Влияние множества этих элементов на организм человека в частности и на жизнь на Земле в целом еще не изучено до конца. Для того чтобы понимать процессы взаимодействия элементов, газов, солей и других образований друг с другом, в школьный курс и был введен предмет «Химия». 8 класс – это старт уроков химии по утвержденной общеобразовательной программе.
Одним из самых распространенных соединений, содержащихся как в земной коре, так и в атмосфере, является оксид. Оксидом называется соединение любого химического элемента с атомом кислорода. Даже источник всего живого на Земле – вода, является оксидом водорода. Но в данной статье речь пойдет не об оксидах в общем, а об одном из самых часто встречаемых соединений – оксиде углерода. Данные соединения получаются путем слияния атомов кислорода и углерода. Эти соединения могут иметь в своем составе различные количества атомов углерода и кислорода, однако следует выделить два основных соединения углерода с кислородом: угарный газ и углекислый газ.
Химическая формула и способ получения угарного газа
Какова же его формула? Оксид углерода довольно легко запомнить – CO. Молекула угарного газа образуется тройной связью, в связи с чем обладает довольно высокой прочностью соединения и имеет очень небольшое межъядерное расстояние (0,1128 нм). Энергия разрыва данного химического соединения составляет 1076 кДж/Моль. Тройная связь возникает вследствие того, что элемент углерод имеет в своей структуре атома p-орбиталь, не занятую электронами. Это обстоятельство создает для атома углерода возможность стать акцептором электронной пары. А атом кислорода, наоборот, имеет на одной из p-орбиталей неразделенную пару электронов, а значит имеет электронно-донорные возможности. При соединении этих двух атомов кроме двух ковалентных связей появляется еще и третья – донорно-акцепторная ковалентная связь.
Существуют различные способы получения CO. Одним из самых простейших является пропускание углекислого газа над раскаленным углем. В лабораторных условиях угарный газ получают при помощи следующей реакции: муравьиную кислоту нагревают с серной кислотой, которая разделяет муравьиную кислоту на воду и угарный газ.
Также CO выделяется при нагревании щавелевой и серной кислоты.
Физические свойства CO
Оксид углерода (2) обладает следующими физическими свойствами – это бесцветный газ, не имеющий ярко выраженного запаха. Все посторонние запахи, появляющиеся при утечке угарного газа, являются продуктами распада органических примесей. Он намного легче воздуха, чрезвычайно токсичен, очень плохо растворяется в воде и отличается высокой степенью горючести.
Самое главное свойство CO – его отрицательное воздействие на организм человека. Отравление угарным газом может привести к летальному исходу. Более подробно о воздействии оксида углерода на организм человека будет рассказано ниже.
Химические свойства CO
Основные химические реакции, в которых могут применяться оксиды углерода (2) – это окислительно-восстановительная реакция, а также реакция присоединения. Окислительно-восстановительная реакция выражается в способности CO восстанавливать металл из оксидов при помощи их смешивания с дальнейшим нагреванием.
При взаимодействии с кислородом происходит образование углекислого газа с выделением значительного количества теплоты. Угарный газ горит синеватым пламенем. Очень важная функция оксида углерода – его взаимодействие с металлами. В результате подобных реакций образуются карбонилы металлов, подавляющее большинство которых являются кристаллическими веществами. Они применяются для изготовления сверхчистых металлов, а также для нанесения металлического покрытия. Кстати, карбонилы неплохо себя зарекомендовали в качестве катализаторов химических реакций.
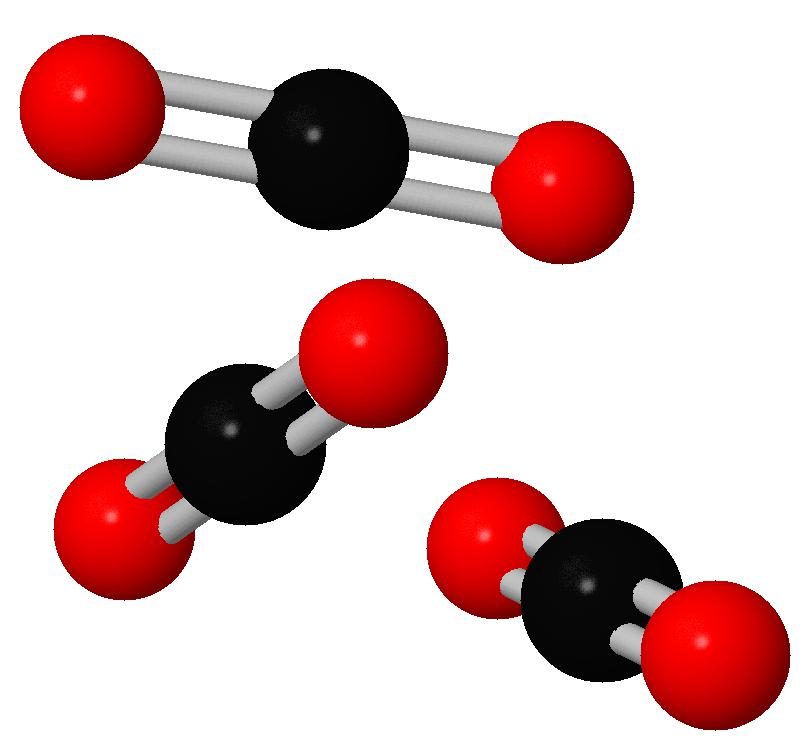
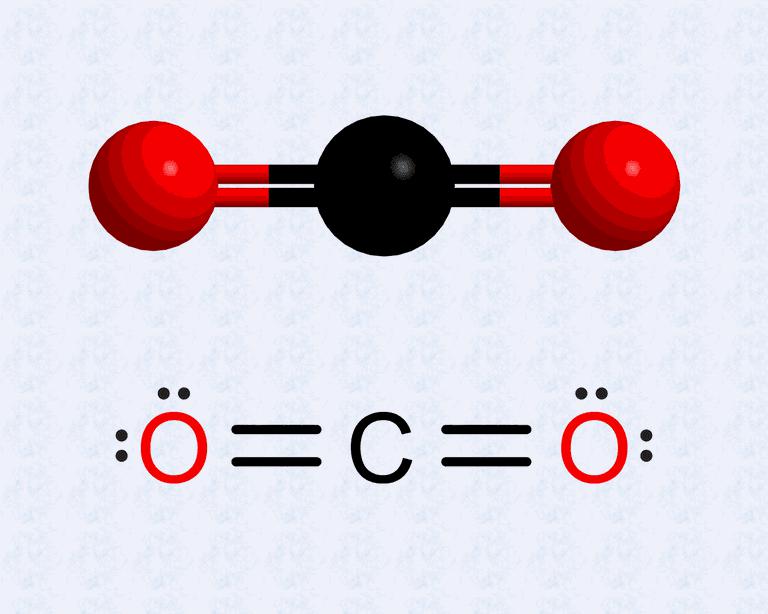
Химическая формула и способ получения углекислого газа
Углекислый газ, или двуокись углерода, имеет химическую формулу CO2. Структура молекулы несколько отличается от структуры CO. В данном образовании углерод имеет степень окисления, равную +4. Структура молекулы линейная, а значит, неполярная. Молекула CO2 не обладает такой сильной прочностью, как CO. В земной атмосфере содержится около 0,03% углекислоты по общему объему. Увеличение этого показателя разрушает озоновый слой Земли. В науке это явление называется парниковым эффектом.
Получить углекислый газ можно различными путями. В промышленности он образуется в результате горения дымовых газов. Может быть побочным продуктом в процессе изготовления алкоголя. Его можно получить в процессе разложения воздуха на основные составляющие, такие как азот, кислород, аргон и другие. В лабораторных условиях оксид углерода (4) можно получить в процессе обжига известняка, а в домашних условиях добыть углекислый газ можно при помощи реакции лимонной кислоты и пищевой соды. Кстати, именно таким образом изготавливались газированные напитки в самом начале их производства.
Физические свойства CO2
Углекислый газ представляет собой бесцветное газообразное вещество без характерного резкого запаха. Из-за высокого числа окисления данный газ обладает слегка кисловатым привкусом. Данный продукт не поддерживает процесс горения, так как сам является результатом горения. При повышенной концентрации углекислого газа человек утрачивает способность дышать, что приводит к летальному исходу. Более подробно о воздействии углекислого газа на организм человека будет рассказано далее. CO2 намного тяжелее воздуха и прекрасно растворяется в воде даже при комнатной температуре.
Одним из самых интересных свойств углекислого газа является то, что у него нет жидкого агрегатного состояния при нормальном атмосферном давлении. Однако если воздействовать на структуру углекислого газа воздействие температурой в -56,6 °С и давлением около 519 кПа, то он трансформируется в бесцветную жидкость.
При существенном понижении температуры газ находится в состоянии так называемого «сухого льда» и испаряется при температуре выше чем -78 оС.
Химические свойства CO2
По своим химическим свойствам оксид углерода (4), формула которого CO2, является типичным кислотным оксидом и обладает всеми его свойствами.
1. При взаимодействии с водой образуется угольная кислота, обладающая слабой кислотностью и малой устойчивостью в растворах.
2. При взаимодействии с щелочами углекислый газ образует соответствующую соль и воду.
3. Во время взаимодействия с оксидами активного металла способствует образованию солей.
4. Не поддерживает процесс горения. Активировать данный процесс могут только некоторые активные металлы, такие как литий, калий, натрий.
Влияние угарного газа на организм человека
Вернемся к основной проблеме всех газов – влиянию на организм человека. Угарный газ относится к группе крайне опасных для жизни газов. Для человека и животного он является чрезвычайно сильным ядовитым веществом, которое при попадании в организм серьезно поражает кровь, нервную систему организма и мышцы (в том числе и сердце).
Оксид углерода в воздухе невозможно распознать, так как этот газ не имеет никакого ярко выраженного запаха. Именно этим он и опасен. Попадая через легкие в организм человека, угарный газ активизирует свою разрушительную деятельность в крови и в сотни раз быстрее кислорода начинает взаимодействовать с гемоглобином. В результате этого появляется очень стойкое соединение под названием карбоксигемоглобин. Оно препятствует доставке кислорода из легких к мышцам, что приводит к мышечному голоданию тканей. Особенно серьезно страдает от этого головной мозг.
Из-за отсутствия возможности распознать отравление угарным газом через обоняние, следует знать некоторые основные признаки, которые проявляются на ранних этапах:
- головокружение, сопровождающееся головной болью;
- шум в ушах и мерцание перед глазами;
- сильное сердцебиение и одышка;
- покраснение лица.
В дальнейшем у жертвы отравления появляется сильная слабость, иногда рвота. В тяжелых случаях отравления возможны непроизвольные судороги, сопровождающиеся дальнейшей потерей сознания и комой. Если же пациенту своевременно не будет оказана соответствующая медицинская помощь, то возможен летальный исход.
Влияние углекислого газа на организм человека
Оксиды углерода с кислотностью +4 относятся к разделу удушающих газов. Иными словами, углекислый газ не является токсичным веществом, однако может существенно влиять на приток кислорода к организму. При повышении уровня углекислого газа до 3-4% у человека возникает серьезная слабость, его начинает клонить в сон. При повышении уровня до 10% начинают развиваться сильнейшие головные боли, головокружение, ухудшение слуха, иногда наблюдается потеря сознания. Если концентрация углекислого газа поднимается до уровня 20%, то наступает смерть от кислородного голодания.
Лечение отравления углекислым газом очень простое – дать жертве доступ к чистому воздуху, при необходимости сделать искусственное дыхание. В крайнем случае нужно подключить пострадавшего к аппарату искусственной вентиляции легких.
Из описаний влияния двух данных оксидов углерода на организм мы можем сделать вывод, что большую опасность для человека все же представляет угарный газ с его высокой токсичностью и направленным воздействием на организм изнутри.
Углекислый газ не отличается таким коварством и менее вреден для человека, поэтому именно это вещество человек активно применяет даже в пищевой промышленности.
Применение оксидов углерода в промышленности и их влияние на различные аспекты жизни
Оксиды углерода имеют очень широкое применение в разных сферах деятельности человека, причем спектр их чрезвычайно богат. Так, окись углерода вовсю применяется в металлургии в процессе выплавки чугуна. Широкую популярность CO получил в качестве материала для хранения продуктов питания в охлажденном виде. Данный оксид применяют для обработки мяса и рыбы, чтобы придать им свежий вид и не изменить вкус. Важно не забывать про токсичность данного газа и помнить, что допустимая доза не должна превышать 200 мг на 1 кг продукта. CO в последнее время все чаще применяют в автомобильной промышленности в качестве топлива для автомобилей на газу.
Диоксид углерода нетоксичен, поэтому сфера его применения широко внедрена в пищевую промышленность, где его применяют в качестве консерванта или разрыхлителя. Также CO2 применяется при изготовлении минеральных и газированных вод. В твердом состоянии («сухой лед») он часто используется в морозильных установках для поддержания стабильно низкой температуры в помещении или приборе.
Большую популярность приобрели углекислотные огнетушители, пена из которых полностью изолирует огонь от кислорода и не дает пожару разгореться. Соответственно, еще одна сфера применения – пожарная безопасность. Баллоны в пневматических пистолетах также заряжены углекислотой. И конечно же, практически каждый из нас читал, из чего состоит освежитель воздуха для помещений. Да, одной из составляющих является углекислый газ.
Как видим, из-за своей минимальной токсичности углекислый газ больше и чаще встречается в повседневной жизни человека, тогда как угарный газ нашел применение в тяжелой промышленности.
Существуют и другие углеродные соединения с кислородом, благо формула углерода и кислорода позволяет применять различные варианты соединений с разным количеством атомов углерода и кислорода. Ряд оксидов может разниться от C2O2 до C32O8. И чтобы описать каждый из них, потребуется не одна страница.
Оксиды углерода в природе
Оба вида рассматриваемых здесь оксидов углерода так или иначе присутствуют в природном мире. Так, угарный газ может быть продуктом сгорания лесов или результатом жизнедеятельности человека (выхлопные газы и вредные отходы промышленных предприятий).
Уже известный нам диоксид углерода также является частью сложного состава воздуха. Его содержание в нем составляет около 0,03 % от всего объема. При увеличении этого показателя возникает так называемый «парниковый эффект», которого так опасаются современные ученые. Углекислый газ выделяют животные и человек путем выдыхания. Он является основным источником такого полезного для растений элемента, как углерод, поэтому многие ученые и бьют на сполох, указывая на недопустимость масштабных вырубок леса. Если растения перестанут поглощать углекислый газ, то процент его содержания в воздухе может повыситься до критических для человеческой жизнедеятельности показателей.
Видимо, многие власть держащие забыли пройденный в детстве материал учебника «Общая химия. 8 класс», иначе вопросу вырубки лесов во многих частях света уделялось бы более серьезное внимание. Это, кстати, касается и проблемы наличия угарного газа в окружающей среде. Количество отходов человеческой жизнедеятельности и процент выбросов этого необычайно токсичного материала в окружающую среду растет изо дня в день. И не факт, что не повторится судьба мира, описанная в прекрасном мультфильме «Волли», когда человечеству пришлось покинуть загаженную до основания Землю и отправиться в другие миры на поиски лучшей жизни.
www.syl.ru
Формула оксида углерода в химии
Определение и формула оксида углерода
Углерод образует два оксида – оксид углерода (II) и оксид углерода (IV) (углекислый газ).
Оксид углерода (II)
Оксид углерода (II) (монооксид углерода, угарный газ, окись углерода)
Химическая формула: CO.

Молярная масса: 28,01 г/моль
В молекуле оксида углерода (II) две связи образованы по обменному механизму за счет неспаренных электронов атомов углерода и кислорода.Но у атома кислорода есть еще неподеленная пара электронов на 2р-орбитали, а у атома углерода – свободная 2р-орбиталь. Пара электронов переходит от атома кислорода к атому углерода, образуя еще одну связь по донорно-акцепторному механизму.
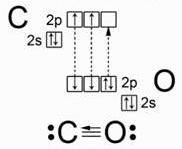
Молекула оксида углерода (II) слабо поляризована, причем электронная плотность смещена к атому углерода: C−←O+. Из-за наличия тройной связи молекула весьма прочная и имеет небольшое межъядерное расстояние.
При нормальных условиях оксид углерода (II) – газ без цвета, вкуса и запаха. Горючий. Мало растворим в воде.
Оксид углерода (II) – несолеобразующий оксид.
Химические свойства оксида углерода (II)
При стандартной температуре оксид углерода (II) малоактивен, химическая активность резко повышается пр и повышении температуры и в растворах.
Основные типы химических реакций оксида углерода (II):
Очень важной с практической точки зрения является реакция оксида углерода (II) с водородом с образованием разнообразных органических соединений:
xCO + yh3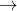 спирты + линейные алканы.
спирты + линейные алканы.
Оксид углерода (II) – токсичный газ. Попадая при дыхании в кровь, он быстро соединяется с гемоглобином, образуя карбоксигемоглобин – прочный карбонильный комплекс, более прочный, чем комплекс гемоглобина с кислородом, тем блокируя процессы транспорта кислорода и клеточного дыхания. Содержание в воздухе более 0,1% угарного газа может привести к потере сознания и смерти.
Примеры решения задач
ru.solverbook.com



















