Углекислый газ. Свойства, получение, применение. Углекислота и ее применение
свойства, получение, применение :: SYL.ru
Вы уже знаете, что при выдохе из легких выходит углекислый газ. А вот что вам известно об этом веществе? Наверное, немного. Сегодня я отвечу на все вопросы, касающиеся углекислого газа.
Определение
Это вещество в нормальных условиях является бесцветным газом. Во многих источниках его могут называть по-разному: и оксидом углерода (IV), и угольным ангидридом, и двуокисью углерода, и диоксидом углерода.
Свойства
Углекислый газ (формула СО2) является бесцветным газом, имеющим кислые запах и вкус, растворимым в воде веществом. Если его как следует охладить, то образуется снегообразная масса, называемая сухим льдом (фотография ниже), которая сублимирует при температуре -78оС. Является одним из продуктов гниения или горения любого органического вещества. Растворяется в воде только при температуре 15оС и только в том случае, если отношение вода:углекислый газ равно 1:1. Плотность углекислого газа может быть разной, но в стандартных условиях она равняется 1,976 кг/м3. Это если он находится в газообразном виде, а в других состояниях (жидком/газообразном) значения плотности тоже будут другими. Данное вещество является кислотным оксидом, его добавление в воду приводит к получению угольной кислоты. Если соединить углекислый газ с любой щелочью, то в результате последующей реакции образуются карбонаты и гидрокарбонаты. Этот оксид не может поддерживать горение, кроме некоторых исключений. Это активные металлы, и при реакции такого вида они забирают у него кислород.
Получение
Углекислый и еще некоторые газы в больших количествах выделяются, когда производят алкоголь или разлагаются природные карбонаты. Затем полученные газы проходят промывание растворенным карбонатом калия. Далее следует поглощение ими углекислого газа, продуктом данной реакции является гидрокарбонат, при нагревании раствора которого получают искомый оксид. Но сейчас его с успехом заменяет растворенный водой этаноламин, который абсорбирует содержащийся в дымовом газе оксид углерода и отдает его при нагревании. Также этот газ является побочным продуктом тех реакций, при которых получают чистые азот, кислород и аргон. В лаборатории немного углекислоты получается, когда карбонаты и гидрокарбонаты взаимодействуют с кислотами. Еще она образуется, когда реагируют пищевая сода и лимонный сок или тот же гидрокарбонат натрия и уксус (фото).
Применение
Пищевая промышленность не может обойтись без использования углекислоты, где она известна в качестве консерванта и разрыхлителя, имеющего код E290. Ее в виде жидкости содержит любой огнетушитель. Также оксид четырехвалентного углерода, который выделяется в процессе брожения, служит хорошей подкормкой аквариумным растениям. Он содержится и во всем известной газировке, которую многие довольно часто покупают в продуктовом магазине. Сварка проволокой происходит в углекислой среде, но если температура данного процесса очень высока, то он сопровождается диссоциацией углекислоты, при которой выделяется кислород, окисляющий металл. Тогда сварка не обходится без раскислителей (марганца или кремния). Углекислым газом накачивают велосипедные колеса, он присутствует и в баллончиках пневматического оружия (такая его разновидность называется газобаллонной). Также данный оксид в твердом состоянии, называемый сухим льдом, нужен как хладагент в торговле, научных исследованиях и при починке некоторой техники.
Заключение
Вот до чего полезен для человека углекислый газ. И не только в промышленности, он играет и важную биологическую роль: без него не может происходить газообмен, регуляция сосудистого тонуса, фотосинтез и многие другие природные процессы. Но его переизбыток или недостача в воздухе некоторое время могут негативно влиять на физическое состояние всех живых организмов.
www.syl.ru
Углекислота Википедия
| Диоксид углерода | |
| Диоксид углерода | |
| углекислый газ, углекислота, двуокись углерода, сухой лёд (в твёрдом состоянии) | |
| CO2 | |
| бесцветный газ | |
| 44,01 г/моль | |
| газ (0 °C): 1,9768 кг/м³жидкость (0 °С, 35,5 ат): 925 кг/м³тв. (−78,5 °C): 1560 кг/м³ | |
| 8,5·10−5 Па·с (10°C, 5,7 МПа) | |
| 13,77±0,01 эВ[1] | |
| −78,5 °C | |
| −56,6 °C, 0,52 МПа | |
| 31,1 °C, 7,38 МПа | |
| 846 Дж/(кг·К) | |
| 25,13 кДж/моль | |
| 56,5±0,1 атм[1] | |
| 1,45 кг/м³ | |
| 124-38-9 | |
| 280 | |
| 204-696-9 | |
| E290 | |
| FF6400000 | |
| 16526 | |
| 1013 | |
| 274 | |
| 9 000 мг/м3 | |
| LC50: 90 000 мг/м3*5 мин (человек, ингаляция) | |
| Нетоксичен. Опасен лишь в очень больших количествах (обладает удушающим действием). Негорюч. | |
| S9, S23, S36 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диокси́д углеро́да или двуо́кись углеро́да (также углеки́слый газ, углекислотá, окси́д углеро́да(IV), у́гольный ангидри́д) — бесцветный газ (в нормальных условиях), почти без запаха (в больших концентрациях с кисловатым «содовым» запахом), с химической формулой CO2.
Плотность при нормальных условиях 1,98 кг/м³ (в 1,5 раза тяжелее воздуха). При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное (возгонка). Твёрдый диоксид углерода называют сухим льдом. При повышенном давлении и обычных температурах углекислый газ переходит в жидкость, что используется для его хранения.
Концентрация углекислого газа в атмосфере Земли составляет в среднем 0,04 %[2]. Углекислый газ легко пропускает излучение в ультрафиолетовой и видимой частях спектра, которое поступают на Землю от Солнца и обогревает её. В то же время он поглощает испускаемое Землёй инфракрасное излучение и является одним из парниковых газов, вследствие чего принимает участие в процессе глобального потепления. Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала индустриальной эпохи.
Свойства
Физические
Оксид углерода (IV) — углекислый газ, бесцветный газ, при малых концентрациях в воздухе не имеет запаха, при больших концентрациях имеет характерный кисловатый запах газированной воды. Тяжелее воздуха приблизительно в 1,5 раза.
Молекула углекислого газа линейна, расстояние от центра центрального атома углерода до центров двух атомов кислорода 116,3 пм.
При температуре −78,3 °С кристаллизуется в виде белой снегообразной массы — «сухого льда». Сухой лёд при атмосферном давлении не плавится, а испаряется, не переходя в жидкое состояние, температура сублимации −78 °С. Жидкий углекислый газ можно получить при повышении давления. Так, при температуре 20 °С и давлении свыше 6 МПа (~60 атм) газ сгущается в бесцветную жидкость.
Негорюч, но в его атмосфере может поддерживаться горение активных металлов, например, щелочных металлов и щелочноземельных — магния, кальция, бария.
Углекислый газ образуется при гниении и горении органических веществ. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Растворим в воде (0,738 объёмов углекислого газа в одном объёме воды при 15 °С).
Химические
По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует угольную кислоту. Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
Оксид углерода(IV) не поддерживает горения. В нём горят только некоторые активные металлы:[3]:
2Mg+CO2→2MgO+C{\displaystyle {\mathsf {2Mg+CO_{2}\to 2MgO+C}}}Взаимодействие с оксидом активного металла:
CaO+CO2→CaCO3{\displaystyle {\mathsf {CaO+CO_{2}\to CaCO_{3}}}}При растворении в воде образует равновесную смесь раствора диоксида углерода и угольной кислоты, причём равновесие сильно сдвинуто в сторону разложения кислоты:
CO2+h3O⇄h3CO3{\displaystyle {\mathsf {CO_{2}+H_{2}O\rightleftarrows H_{2}CO_{3}}}}Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов:
Ca(OH)2+CO2→CaCO3↓+h3O{\displaystyle {\mathsf {Ca(OH)_{2}+CO_{2}\to CaCO_{3}\downarrow +H_{2}O}}} (качественная реакция на углекислый газ)KOH+CO2→KHCO3{\displaystyle {\mathsf {KOH+CO_{2}\to KHCO_{3}}}}
Биологические
Организм человека выделяет приблизительно 1 кг углекислого газа в сутки[4].
Этот углекислый газ переносится от тканей, где он образуется в качестве одного из конечных продуктов метаболизма, по венозной системе и затем выделяется с выдыхаемым воздухом через лёгкие. Таким образом, содержание углекислого газа в крови велико в венозной системе, уменьшается в капиллярной сети лёгких, и мало в артериальной крови. Содержание углекислого газа в пробе крови часто выражают в терминах парциального давления, то есть давления, которое бы имел содержащийся в пробе крови в данном количестве углекислый газ, если бы весь объём пробы крови занимал только он[5].
Содержание углекислого газа в крови человека приблизительно таково:
| кПа | 5,5[6]—6,8[6] | 4,8 | 4,7[6]—6,0[6] |
| мм рт. ст. | 41—51 | 36 | 35[7]—45[7] |
Углекислый газ транспортируется в крови тремя различными способами (точное соотношение каждого из этих трёх способов транспортировки зависит от того, является ли кровь артериальной или венозной).
- Бо́льшая часть углекислого газа (от 70 % до 80 %) преобразуется ферментом карбоангидразой эритроцитов в ионы гидрокарбоната[8] при помощи реакции CO₂ + H₂O → H₂CO₃ → H⁺ + HCO₃⁻.
- Около 5—10 % углекислого газа растворено в плазме крови[8].
- Около 5—10 % углекислого газа связано с гемоглобином в виде карбаминосоединений (карбогемоглобин)[8].
Гемоглобин, основной кислород-транспортирующий белок эритроцитов крови, способен транспортировать как кислород, так и углекислый газ. Однако углекислый газ связывается с гемоглобином в ином месте, чем кислород. Он связывается с N-терминальными концами цепей глобина, а не с гемом. Однако благодаря аллостерическим эффектам, которые приводят к изменению конфигурации молекулы гемоглобина при связывании, связывание углекислого газа понижает способность кислорода к связыванию с ним же, при данном парциальном давлении кислорода, и наоборот — связывание кислорода с гемоглобином понижает способность углекислого газа к связыванию с ним же, при данном парциальном давлении углекислого газа. Помимо этого, способность гемоглобина к преимущественному связыванию с кислородом или с углекислым газом зависит также и от pH среды. Эти особенности очень важны для успешного захвата и транспорта кислорода из лёгких в ткани и его успешного высвобождения в тканях, а также для успешного захвата и транспорта углекислого газа из тканей в лёгкие и его высвобождения там.
Углекислый газ является одним из важнейших медиаторов ауторегуляции кровотока. Он является мощным вазодилататором. Соответственно, если уровень углекислого газа в ткани или в крови повышается (например, вследствие интенсивного метаболизма — вызванного, скажем, физической нагрузкой, воспалением, повреждением тканей, или вследствие затруднения кровотока, ишемии ткани), то капилляры расширяются, что приводит к увеличению кровотока и соответственно к увеличению доставки к тканям кислорода и транспорта из тканей накопившейся углекислоты. Кроме того, углекислый газ в определённых концентрациях (повышенных, но ещё не достигающих токсических значений) оказывает положительное инотропное и хронотропное действие на миокард и повышает его чувствительность к адреналину, что приводит к увеличению силы и частоты сердечных сокращений, величины сердечного выброса и, как следствие, ударного и минутного объёма крови. Это также способствует коррекции тканевой гипоксии и гиперкапнии (повышенного уровня углекислоты).
Ионы гидрокарбоната очень важны для регуляции pH крови и поддержания нормального кислотно-щелочного равновесия. Частота дыхания влияет на содержание углекислого газа в крови. Слабое или замедленное дыхание вызывает респираторный ацидоз, в то время как учащённое и чрезмерно глубокое дыхание приводит к гипервентиляции и развитию респираторного алкалоза.
Кроме того, углекислый газ также важен в регуляции дыхания. Хотя наш организм требует кислорода для обеспечения метаболизма, низкое содержание кислорода в крови или в тканях обычно не стимулирует дыхание (вернее, стимулирующее влияние нехватки кислорода на дыхание слишком слабо и «включается» поздно, при очень низких уровнях кислорода в крови, при которых человек нередко уже теряет сознание). В норме дыхание стимулируется повышением уровня углекислого газа в крови. Дыхательный центр гораздо более чувствителен к повышению уровня углекислого газа, чем к нехватке кислорода. Как следствие этого, дыхание сильно разрежённым воздухом (с низким парциальным давлением кислорода) или газовой смесью, вообще не содержащей кислорода (например, 100 % азотом или 100 % закисью азота) может быстро привести к потере сознания без возникновения ощущения нехватки воздуха (поскольку уровень углекислоты в крови не повышается, ибо ничто не препятствует её выдыханию). Это особенно опасно для пилотов военных самолётов, летающих на больших высотах (в случае аварийной разгерметизации кабины пилоты могут быстро потерять сознание). Эта особенность системы регуляции дыхания также является причиной того, почему в самолётах стюардессы инструктируют пассажиров в случае разгерметизации салона самолёта в первую очередь надевать кислородную маску самим, прежде чем пытаться помочь кому-либо ещё — делая это, помогающий рискует быстро потерять сознание сам, причём даже не ощущая до последнего момента какого-либо дискомфорта и потребности в кислороде[8].
Дыхательный центр человека пытается поддерживать парциальное давление углекислого газа в артериальной крови не выше 40 мм ртутного столба. При сознательной гипервентиляции содержание углекислого газа в артериальной крови может снизиться до 10-20 мм ртутного столба, при этом содержание кислорода в крови практически не изменится или увеличится незначительно, а потребность сделать очередной вдох уменьшится как следствие уменьшения стимулирующего влияния углекислого газа на активность дыхательного центра. Это является причиной того, почему после некоторого периода сознательной гипервентиляции легче задержать дыхание надолго, чем без предшествующей гипервентиляции. Такая сознательная гипервентиляция с последующей задержкой дыхания может привести к потере сознания до того, как человек ощутит потребность сделать вдох. В безопасной обстановке такая потеря сознания ничем особенным не грозит (потеряв сознание, человек потеряет и контроль над собой, перестанет задерживать дыхание и сделает вдох, дыхание, а вместе с ним и снабжение мозга кислородом восстановится, а затем восстановится и сознание). Однако в других ситуациях, например, перед нырянием, это может быть опасным (потеря сознания и потребность сделать вдох наступят на глубине, и в отсутствие сознательного контроля в дыхательные пути попадёт вода, что может привести к утоплению)[источник не указан 322 дня]. Именно поэтому гипервентиляция перед нырянием опасна и не рекомендуется.
Получение
В промышленных количествах углекислота выделяется из дымовых газов, или как побочный продукт химических процессов, например, при разложении природных карбонатов[9] (известняк, доломит) или при производстве алкоголя (спиртовое брожение). Смесь полученных газов промывают раствором карбоната калия, которые поглощают углекислый газ, переходя в гидрокарбонат. Раствор гидрокарбоната при нагревании или при пониженном давлении разлагается, высвобождая углекислоту. В современных установках получения углекислого газа вместо гидрокарбоната чаще применяется водный раствор моноэтаноламина, который при определённых условиях способен абсорбировать СО2, содержащийся в дымовом газе, а при нагреве отдавать его; таким образом отделяется готовый продукт от других веществ.
Также углекислый газ получают на установках разделения воздуха как побочный продукт получения чистого кислорода, азота и аргона.
В лабораторных условиях небольшие количества получают взаимодействием карбонатов и гидрокарбонатов с кислотами, например мрамора, мела или соды с соляной кислотой, используя, например, аппарат Киппа.[9]
CaCO3+2HCl⟶CaCl2+h3O+CO2↑{\displaystyle {\ce {CaCO3 + 2HCl -> CaCl2 + h3O + CO2 ^}}}
Использование реакции серной кислоты с мелом или мрамором приводит к образованию малорастворимого сульфата кальция, который мешает реакции, и который удаляется значительным избытком кислоты.
Для приготовления напитков может быть использована реакция пищевой соды с лимонной кислотой или с кислым лимонным соком. Именно в таком виде появились первые газированные напитки. Их изготовлением и продажей занимались аптекари.
Применение
В пищевой промышленности углекислота используется как консервант и разрыхлитель, обозначается на упаковке кодом Е290.
В криохирургии используется как одно из основных веществ для криоабляции новообразований.
Жидкая углекислота широко применяется в системах пожаротушения и в огнетушителях. Автоматические углекислотные установки для пожаротушения различаются по системам пуска, которые бывают пневматическими, механическими или электрическими.
Устройство для подачи углекислого газа в аквариум может включать в себя резервуар с газом. Простейший и наиболее распространенный метод получения углекислого газа основан на конструкции для изготовления алкогольного напитка браги. При брожении, выделяемый углекислый газ вполне может обеспечить подкормку аквариумных растений[10]
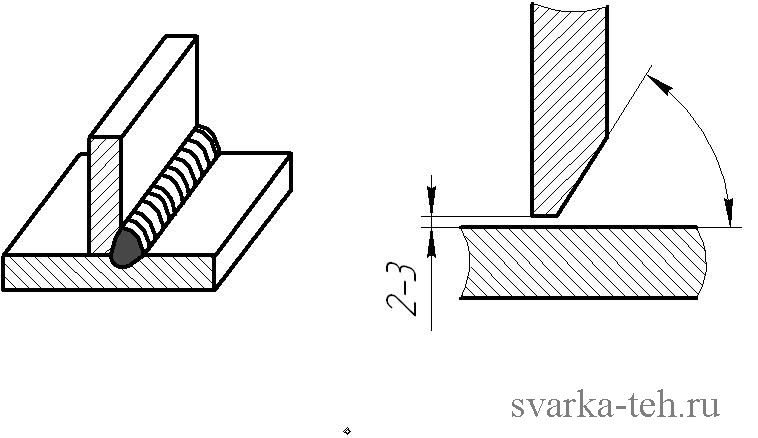
Углекислый газ используется для газирования лимонада и газированной воды. Углекислый газ используется также в качестве защитной среды при сварке проволокой, но при высоких температурах происходит его распад с выделением кислорода. Выделяющийся кислород окисляет металл. В связи с этим приходится в сварочную проволоку вводить раскислители, такие как марганец и кремний. Другим следствием влияния кислорода, также связанного с окислением, является резкое снижение поверхностного натяжения, что приводит, среди прочего, к более интенсивному разбрызгиванию металла, чем при сварке в инертной среде.
Углекислота в баллончиках применяется в пневматическом оружии (в газобаллонной пневматике) и в качестве источника энергии для двигателей в авиамоделировании.
Хранение углекислоты в стальном баллоне в сжиженном состоянии выгоднее, чем в виде газа. Углекислота имеет сравнительно низкую критическую температуру +31 °С. В стандартный 40-литровый баллон заливают около 30 кг сжиженного углекислого газа, и при комнатной температуре в баллоне будет находиться жидкая фаза, а давление составит примерно 6 МПа (60 кгс/см²). Если температура будет выше +31 °С, то углекислота перейдёт в сверхкритическое состояние с давлением выше 7,36 МПа. Стандартное рабочее давление для обычного 40-литрового баллона составляет 15 МПа (150 кгс/см²), однако он должен безопасно выдерживать давление в 1,5 раза выше, то есть 22,5 МПа, — таким образом, работа с подобными баллонами может считаться вполне безопасной.
Твёрдая углекислота — «сухой лёд» — используется в качестве хладагента в лабораторных исследованиях, в розничной торговле, при ремонте оборудования (например: охлаждение одной из сопрягаемых деталей при посадке внатяг) и т. д. Для сжижения углекислого газа и получения сухого льда применяются углекислотные установки.
Методы регистрации
Измерение парциального давления углекислого газа требуется в технологических процессах, в медицинских применениях — анализ дыхательных смесей при искусственной вентиляции лёгких и в замкнутых системах жизнеобеспечения. Анализ концентрации CO₂ в атмосфере используется для экологических и научных исследований, для изучения парникового эффекта. Углекислый газ регистрируют с помощью газоанализаторов основанных на принципе инфракрасной спектроскопии и других газоизмерительных систем. Медицинский газоанализатор для регистрации содержания углекислоты в выдыхаемом воздухе называется капнограф. Для измерения низких концентраций CO₂ (а также CO) в технологических газах или в атмосферном воздухе можно использовать газохроматографический метод с метанатором и регистрацией на пламенно-ионизационном детекторе[11].
Углекислый газ в природе
Ежегодные колебания концентрации атмосферной углекислоты на планете определяются, главным образом, растительностью средних (40—70°) широт Северного полушария.
Вегетация в тропиках практически не зависит от сезона, сухой пояс пустынь 20—30° (обоих полушарий) даёт малый вклад в круговорот углекислоты, а полосы суши, наиболее покрытые растительностью, расположены на Земле асимметрично (в Южном полушарии в средних широтах находится океан). Поэтому с марта по сентябрь вследствие фотосинтеза содержание СО2 в атмосфере падает, а с октября по февраль — повышается. Вклад в зимний прирост дают как окисление древесины (гетеротрофное дыхание растений, гниение, разложение гумуса, лесные пожары), так и сжигание ископаемого топлива (угля, нефти, газа), заметно увеличивающееся в зимний сезон[12].
Большое количество углекислоты растворено в океане.
Углекислый газ составляет значительную часть атмосфер некоторых планет Солнечной системы: Венеры, Марса.
Физиологическое действие
Углекислый газ нетоксичен, но при вдыхании его повышенных концентраций в воздухе по воздействию на воздуходышащие живые организмы его относят к удушающим газам (англ.)русск.. По ГОСТу (ГОСТ 8050-85) углекислота относится к 4-му классу опасности.
Незначительные повышения концентрации, вплоть до 2—4 %, в помещениях приводят к развитию у людей сонливости и слабости. Опасными для здоровья концентрациями считаются концентрации около 7—10 %, при которых развиваются симптомы удушья, проявляющиеся в виде головной боли, головокружения, расстройстве слуха и в потере сознания (симптомы, сходные с симптомами высотной болезни), эти симптомы развиваются, в зависимости от концентрации, в течение времени от нескольких минут до одного часа.
При вдыхании воздуха с очень высокими концентрациями газа смерть наступает очень быстро от удушья, вызванного гипоксией[13].
Несмотря на то, что даже концентрация 5—7 % CO₂ в воздухе несмертельна, но при концентрации 0,1 % (такое содержание углекислого газа иногда наблюдается в воздухе мегаполисов), люди начинают чувствовать слабость, сонливость. Это показывает, что даже при высоком уровне кислорода, большая концентрация CO₂ существенно влияет на самочувствие человека.
Вдыхание воздуха с повышенной концентрацией этого газа не приводит к долговременным расстройствам здоровья. После удаления пострадавшего из атмосферы с высокой концентрацией углекислого газа быстро наступает полное восстановление здоровья и самочувствия[14].
См. также
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0103.html
- ↑ Trends in Atmospheric Carbon Dioxide (англ.). National Oceanic and Atmospheric Administration. Проверено 24 сентября 2013.
- ↑ А. С. Егоров. Репетитор по химии — Ростов-на-Дону: «Феникс», 2009.
- ↑ How much carbon dioxide do humans contribute through breathing?. Проверено 30 апреля 2009. Архивировано 2 февраля 2011 года.
- ↑ Charles Henrickson. Chemistry. — Cliffs Notes, 2005. — ISBN 0-7645-7419-1.
- ↑ 1 2 3 4 Пересчитано из значений в мм. рт. ст. с использованием коэффициента пересчёта 0,133322 кПа/мм. рт. ст.
- ↑ 1 2 Таблица референсных значений. Юго-Западный медицинский центр при Университете Далласа.
- ↑ 1 2 3 4 Carbon dioxide. solarnavigator.net. Проверено 12 октября 2007.
- ↑ 1 2 Glinka, Nikolaj Leonidovič (1882-1965). Obŝaâ himiâ. — Izd. 27-e ster. — Leningrad: "Himiâ", 1988. — 702, [2] s. с. — ISBN 5724500035, 9785724500036.
- ↑ Большая Энциклопедия Нефти и Газа.
- ↑ ГОСТ 31371.6-2008 (ИСО 6974-6:2002). Газ природный. ОПРЕДЕЛЕНИЕ СОСТАВА МЕТОДОМ ГАЗОВОЙ ХРОМАТОГРАФИИ С ОЦЕНКОЙ НЕОПРЕДЕЛЕННОСТИ. Часть 6. ОПРЕДЕЛЕНИЕ ВОДОРОДА, ГЕЛИЯ, КИСЛОРОДА, АЗОТА, ДИОКСИДА УГЛЕРОДА И УГЛЕВОДОРОДОВ C1 — C8 С ИСПОЛЬЗОВАНИЕМ ТРЕХ КАПИЛЛЯРНЫХ КОЛОНОК.
- ↑ А. В. Бялко. Растения убыстряют рост. «Природа». No 10, 1996. (по Keeling C.D., Whorf Т.P., Wahlen M., van der Plicht J. // Nature. 1995. V. 375, № 6533. P.666-670)
- ↑ (англ.) Carbon Dioxide as a Fire Suppressant: Examining the Risks, U.S. Environmental Protection Agency:.
- ↑ (англ.) Glatte Jr H. A., Motsay G. J., Welch B. E. (1967). «Carbon Dioxide Tolerance Studies». Brooks AFB, TX School of Aerospace Medicine Technical Report SAM-TR-67-77. Проверено 2008-05-02.
Литература
- Вукалович М. П., Алтунин В. В. Теплофизические свойства двуокиси углерода. — М.: Атомиздат, 1965. — 456 с.
- Тезиков А. Д. Производство и применение сухого льда. — М.: Госторгиздат, 1960. — 86 с.
- Гродник М. Г., Величанский А. Я. Проектирование и эксплуатация углеслотных установок. — М.: Пищевая промышленность, 1966. — 275 с.
- Талянкер Ю. Е. Особенности хранения баллонов со сжиженным газом // Сварочное производство. — 1972. — № 11.
Ссылки
wikiredia.ru
Углекислота инструкция по применению, описание препарата.
Наименование: Углекислота
Наименование: Углекислота (Carbonei dioxydum)Показания к применению:Углекислоту применяют с кислородом при угнетении деятельности дыхательного центра: при отравлениях летучими наркотиками, окисью углерода, сероводородом, при асфиксии (отсутствии дыхания) новорожденных и т. п.В хирургической практике ее применяют во время наркоза и в последствии операции для стимулирования дыхания, для предупреждения ателектаза легких (спадения легочной ткани) и пневмоний (воспаления легких). Вдыхание углекислоты показано также при сосудистом коллапсе (резком падении артериального давления).При резком ослаблении дыхания применение углекислоты должно производиться с осторожностью, так как в результате недостаточной вентиляции она может накопиться в организме в избыточном количестве. В этих случаях могут наблюдаться такие же осложнения, как при использовании углекислоты в больших концентрациях.Жидкая углекислота, выпускаемая из баллона, помещенного вниз вентилем, попадая в условия комнатной температуры и обычного давления, быстро испаряется, при всем этом поглощается так много тепла, что она превращается в твердую белую снегообразную массу. Этим пользуются при замораживании тканей для гистологических срезов (образцов ткани для микроскопических исследований). Если смешать твердый угольный ангидрид с эфиром, то температура падает до - 80 °С.
Фармакологическое действие:Углекислота постоянно образуется в тканях организма в процессе обмена веществ и играет важную роль в регуляции дыхания и кровообращения. Она оказывает прямое и рефлекторное (через каротидные клубочки) влияние на дыхательный центр и является его специфическим возбудителем.Вдыхание небольших концентраций углекислоты (3-5-7%) вызывает учащение и углубление дыхательных движений и увеличение легочной вентиляции; одновременно возбуждаются сосудодвигательные центры, в связи с чем происходит сужение кровеносных сосудов и повышается артериальное давление.Большие концентрации углекислоты вызывают сильный ацидоз (закисление), одышку, судороги и паралич (остановку) дыхательного центра.
Углекислота способ применения и дозы:Для стимуляции дыхания и сосудодвигательного центра используют ингаляции 5-7% углекислоты с 93-95% кислорода.“Углекислый снег” имеет применение при кожных заболеваниях (при красной волчанке, лепрозных узлах, бородавках и т. п.). При образовании “углекислого снега” его собирают в специальные мешочки, потом набивают в формочки из картона или стеклянные трубочки и прикладывают к участкам кожи, подлежащим разрушению. Имеются данные об эффективности замораживания очагов поражения кожи (криотерапия) при нейродермитах (заболеваниях кожи, обусловленных нарушением функции центральной нервной системы).Напитки, содержащие в растворенном виде углекислоту (углекислые минеральные воды, газированные напитки), вызывают гиперемию (покраснение) слизистой оболочки и усиливают секреторную (выделение пищеварительного сока), всасывательную и двигательную активность желудочно-кишечного тракта.Углекислота, содержащаяся в естественных минеральных водах, используемых для лечебных ванн (например, нарзанные ванны), может оказывать сложное влияние на организм, вызывая возникновение центростремительных импульсов с рецепторов кожи и появление рефлекторных изменений в деятельности сердечно-сосудистой системы и других органов, также изменение трофики (питания) тканей.
Углекислота противопоказания:Резкое ослабление дыхания.
Углекислота побочные действия:При вдыхании углекислоты в чрезмерной концентрации может развиться ацидоз (закисление), сильная одышка, потеря сознания, подергивания мышц, судороги, кома (полная потеря сознания, характеризующаяся отсутствием реакции организма на внешние раздражители), остановка дыхания вследствие паралича дыхательного центра.
Форма выпуска:Жидкая углекислота поступает в продажу в стальных цилиндрах (баллонах) черного цвета под давлением более 60 атм.
Синонимы:!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!Ангидрид угольной кислоты, Диоксид углерода, СО2.
Условия хранения:В прохладном месте.
Внимание!Перед применением медикамента "Углекислота" необходимо проконсультироваться с врачом.Инструкция предоставлена исключительно для ознакомления с «Углекислота».
Групповая принадлежность:
medprep.info
Углекислый газ. Свойства, получение, применение
Углекислый газ – вещество, которое имеет множество названий: оксид углерода (IV), диоксид углерода или же двуокись углерода. Также его еще называют угольным ангидридом. Он является совершенно бесцветным газом, который не имеет запаха, с кисловатым вкусом. Углекислый газ тяжелее воздуха и плохо растворяется в воде. При температуре ниже – 78 градусов Цельсия кристаллизуется и становится похожим на снег.
Из газообразного состояния это вещество переходит в твердое, поскольку не может существовать в жидком состоянии в условиях атмосферного давления. Плотность углекислого газа в нормальных условиях составляет 1,97 кг/м3 – в 1,5 раза выше плотности воздуха. Диоксид углерода в твердом виде называется «сухой лед». В жидкое состояние, в котором его можно хранить длительное время, он переходит при повышении давления. Рассмотрим подробнее данное вещество и его химическое строение.
Углекислый газ, формула которого CO2, состоит из углерода и кислорода, а получается он в результате сжигания или гниения органических веществ. Оксид углерода содержится в воздухе и подземных минеральных источниках. Люди и животные тоже выделяют углекислый газ при выдыхании воздуха. Растения без освещения выделяют его, а во время фотосинтеза интенсивно поглощают. Благодаря процессу метаболизма клеток всех живых существ оксид углерода является одним из главных составляющих окружающей природы.
Этот газ не токсичен, но если он скапливается в большой концентрации, может начаться удушье (гиперкапния), а при его недостатке развивается противоположное состояние – гипокапния. Диоксид углерода пропускает ультрафиолетовые лучи и отражает инфракрасные. Он является парниковым газом, который непосредственно влияет на глобальное потепление. Это происходит из-за того, что уровень его содержания в атмосфере постоянно растет, что и приводит к парниковому эффекту.
Диоксид углерода получают промышленным путем из дымных или печных газов, или же путем разложения карбонатов доломита и известняка. Смесь этих газов тщательно промывается специальным раствором, состоящим из карбоната калия. Далее она переходит в гидрокарбонат и при нагревании разлагается, в результате чего высвобождается углекислота. Углекислота (h3CO3) образуется из углекислого газа, растворенного в воде, но в современных условиях получают ее и другими, более прогрессивными методами. После того как углекислый газ очищен, его сжимают, охлаждают и закачивают в баллоны.
В промышленности это вещество широко и повсеместно применяется. Пищевики используют его как разрыхлитель (например, для приготовления теста) или в качестве консерванта (Е290). С помощью углекислого газа производят различные тонизирующие напитки и газировки, которые так любимы не только детьми, но и взрослыми. Диоксид углерода используют при изготовлении пищевой соды, пива, сахара, шипучих вин.
Углекислый газ применяется и при производстве эффективных огнетушителей. С помощью углекислого газа создается активная среда, необходимая при сварке проволокой. При высокой температуре сварочной дуги углекислый газ распадается на кислород и угарный газ. Кислород взаимодействует с жидким металлом и окисляет его. Углекислота в баллончиках применяется в пневматических ружьях и пистолетах.
Авиамоделисты используют это вещество в качестве топлива для своих моделей. С помощью углекислого газа можно значительно повысить урожайность культур, выращиваемых в оранжерее. Также в промышленности широко используется сухой лед, в котором продукты питания сохраняются значительно лучше. Его применяют в качестве хладагента в холодильниках, морозильных камерах, электрических генераторах и других теплоэнергетических установках.
fb.ru
Применение - углекислота - Большая Энциклопедия Нефти и Газа, статья, страница 1
Применение - углекислота
Cтраница 1
Применение углекислоты для хранения пищевых продуктов основано на сравнительно небольшой ее токсичности при низкой концентраци. Углекислота ограничивает жизнедеятельность вредных микроорганизмов, уничтожая их только в условиях высокой концентрации. Из 37 форм гнилостных бактерий только 5 не поддаются воздействию углекислоты. [1]
Применение углекислоты для питания растений основано на процессе фотосинтеза. Листья растений с помощью хлорофилла поглощают углекислоту воздуха и вместе с водой перерабатывают ее в питательные органические вещества, необходимые для их развития и роста. Этот процесс сопровождается выделением кислорода, то есть происходит газообмен на основе дыхания растений. Для усиленного построения органических питательных веществ растения должны получать больше воды и углекислоты. [2]
Применение углекислоты при электрической сварке основано на принципе защиты расплавленного металла от вредного воздействия атмосферного воздуха. Содержащиеся в воздухе активные газы - кислород, водород и азот - вступают в различные химические соединения с расплавленным металлом: окисляют его, выделяют влагу или растворяются в металле, в результате чего сварные швы получаются пористыми и неплотными. Углекислота оттесняет атмосферный воздух от расплавленного металла, обеспечивая тем нормальное качество сварных соединений. [3]
Применение углекислоты повышает производительность станков и снижает потери времени на переточки. [4]
Применение углекислоты для взрывных работ основано на быстром переходе ее-под влиянием нагрева из жидкого в газообразное состояние с, последующим взрывом без образования пламени. [5]
Применение углекислоты с радиоактивным углеродом, и исследование продуктов обмена показало, что углерод С02 переходит в карбоксильную группу образующейся при этом янтарной кислоты. Очевидно, углекислота может быть ассимилирована микробами для синтетических реакций. Не исключена возможность значительного обогащения почвенною слоя за счет реакций аналогичного характера, пока еще совершенно не изученных. [6]
Сфера применения углекислоты, потребляемой на пищевые и разнообразные технические нужды, непрерывно расширяется. Выработка ее, особенно в летний период, не покрывает предъявляемого спроса. В РСФСР углекислоту вырабатывают только в 30 областях, краях и автономных республиках, что вызывает значительные межобластные перевозки. Железнодорожные перевозки углекислоты, как взрывоопасного груза, регламентированы специальными правилами. [7]
Оценка применения углекислоты на опытном участке Александровской площади Туймазинского месторождения, проведенная БашНИПИ - нефтью, позволила констатировать, что закачка СО2 на участке, выработанном с применением обычного заводнения привела к увеличению дебитов скважин по нефти в 2 раза. [8]
К преимуществам применения углекислоты для продувки следует отнести и возможность поглощения ее из ацетилена карбидным илом. [10]
Шлифование с применением углекислоты позволяет уменьшить расход абразивов и машинное время. Тепловые напряжения при этом уменьшаются, что позволяет избежать трещин на обработанной поверхности. [11]
Интересным и перспективным является применение углекислоты в качестве средства для улучшения погоды в туманные дни. [12]
Одной из крупных областей применения углекислоты является выработка газированной воды. Газирование производится растворением углекислоты в воде - Насыщение воды углекислотой производится с предварительным охлаждением и под давлением в торговых сатураторах. [13]
Указанные технологические схемы осуществляют с применением углекислоты или же ее смеси с ПАВ. [14]
По данным исследований нефтеотдача при применении углекислоты возрастает при создании оторочки до 10 % порового объема пласта. [15]
Страницы: 1 2 3
www.ngpedia.ru
Углекислота - это... Что такое Углекислота?
| Другие названия | углекислый газ, углекислота,сухой лед(твердый) |
| Формула | CO2 |
| Молярная масса | 44.0095(14) г/моль |
| В твердом виде | сухой лед |
| Вид | бесцветный газ |
| Номер CAS | [124-38-9] |
| Плотность и фазовое состояние | 1.98 кг/м³, при н.у.;771 кг/м³, жидкий;1512 кг/м³, твёрдый |
| Растворимость в воде | 1.45 кг/м³ |
| Удельная теплота плавления | 25.13 кДж/моль |
| Точка плавления | −57 °C (216 K), под давлением |
| Точка кипения | −78 °C (195 K), возгоняется |
| Константа диссоциации кислоты (pKa) | 6.35 and 10.33 |
| Вязкость | 0.07 пз при −78 °C |
| Форма молекулы | линейная |
| Кристаллическая решётка | кварцевидная |
| Дипольный момент | ноль |
| MSDS | External MSDS |
| Главные опасности | удушающее, раздражающее |
| NFPA 704 | 0 0 0
(жидкость) |
| R-phrases | R: As, Fb |
| S-phrases | S9, S23, S36 (ж) |
| RTECS number | FF6400000 |
| Структура и свойства | n, εr, и т. д. |
| Спектр | УФ, ИК, ЯМР, Масс-спектроскопия |
| Оксиды | COC3O2C2OCO3 |
| Если не указано иное, данные даны дляматериалов при стандартных условиях (25 °C, 100 кПа)Infobox disclaimer and references | |
Диокси́д углеро́да (двуо́кись углеро́да, углеки́слый газ, окси́д углеро́да (IV), диокси́д углеро́да, у́гольный ангидрид, углекислота́) — CO2, бесцветный газ со слегка кисловатым запахом и вкусом.
Концентрация углекислого газа в атмосфере Земли составляет 0,038 %.
Не следует путать с Диоксин.Свойства
Физические
Плотность при нормальных условиях 1,98 г/л. При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное. Твёрдый диоксид углерода называют сухим льдом. При повышенном давлении и обычных температурах углекислый газ переходит в жидкость, что используется для его хранения.
Углекислый газ легко пропускает ультрафиолетовые лучи и лучи видимой части спектра, которые поступают на Землю от Солнца и обогревают её. В то же время он поглощает испускаемые Землёй инфракрасные лучи и является одним из парниковых газов, вследствие чего принимает участие в процессе глобального потепления. Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала индустриальной эпохи.
Химические
По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует угольную кислоту. Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом — реакция Кольбе) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
Биологические
Диоксид углерода играет одну из главных ролей в живой природе, участвуя во многих процессах метаболизма живой клетки. Диоксид углерода получается в результате множества окислительных реакций у животных, и выделяется в атмосферу с дыханием. Углекислый газ атмосферы — основной источник углерода для растений. Однако, ошибкой будет утверждение, что животные только выделяют углекислый газ, а растения — только поглощают его. Растения поглощают углекислый газ в процессе фотосинтеза, а без освещения они тоже его выделяют.
Диоксид углерода не токсичен, но не поддерживает дыхание. Большая концентрация в воздухе вызывает удушье (см. Гиперкапния). Недостаток углекислого газа тоже опасен (см. Гипокапния)
Углекислый газ в организмах животных имеет и физиологическое значение, например, участвует в регуляции сосудистого тонуса (см. Артериолы).
Получение
В промышленности получают из печных газов, из продуктов разложения природных карбонатов (известняк, доломит). Смесь газов промывают раствором карбоната калия, который поглощает углекислый газ, переходя в гидрокарбонат. Раствор гидрокарбоната при нагревании разлагается, высвобождая углекислоту. При промышленном производстве закачивается в баллоны.
В лабораторных условиях небольшие количества получают взаимодействием карбонатов и гидрокарбонатов с кислотами, например мрамора с соляной кислотой.
Применение
В пищевой промышленности диоксид углерода используется как консервант и обозначается на упаковке под кодом Е290, а также в качестве разрыхлителя теста.
Жидкая углекислота (жидкая пищевая углекислота) — сжиженный углекислый газ, хранящийся под высоким давлением (~ 65-70 Атм). Бесцветная жидкость. При выпуске жидкой углекислоты из баллона в атмосферу часть её испаряется, а другая часть образует хлопья сухого льда.
Баллоны с жидкой углекислотой широко применяются в качестве огнетушителей и для производства газированной воды и лимонада. Углекислый газ используется в качестве активной среды при сварке проволокой так как при температуре дуги углекислота разлагается на угарный газ СО и кислород который в свою очередь и входит в заимодействие с жидким металом окисляя его. Углекислота в баллончиках применяется в пневматическом оружии и в качестве источника энергии для двигателей в авиамоделировании.
Твёрдая углекислота — сухой лёд — используется в качестве хладагента в ледниках и морозильных установках.
Методы регистрации
Измерение парциального давления углекислого газа требуется в технологических процессах, в медицинских применениях — анализ дыхательных смесей при искусственной вентиляции лёгких и в замкнутых системах жизнеобеспечения. Анализ концентрации CO2 в атмосфере используется для экологических и научных исследований, для изучения парникового эффекта.
Углекислый газ регистрируют с помощью газоанализаторов основанных на принципе инфракрасной спектроскопии и других газоизмерительных систем. Медицинский газоанализатор для регистрации содержания углекислоты в выдыхаемом воздухе называется капнограф.
Концентрация
- Подземное животное голый землекоп отличается терпимостью к большим (смертельным для других животных) концентрациям углекислого газа.[1]
Примечания
См. также
Ссылки
Wikimedia Foundation. 2010.
dic.academic.ru
УГЛЕКИСЛОТА - это... Что такое УГЛЕКИСЛОТА?
углекислота — углекислота … Орфографический словарь-справочник
углекислота — ы; ж. Неправильное (обиходное) название двуокиси углерода. * * * углекислота неправильное название диоксида углерода. * * * УГЛЕКИСЛОТА УГЛЕКИСЛОТА, неправильное название углерода диоксида (см. УГЛЕРОДА ДИОКСИД) … Энциклопедический словарь
УГЛЕКИСЛОТА — (угольный ангидрид, двуокись углерода, углекислый газ, С02) была известна еще в 16 в. Парацельсу и ван Гель монту как составная часть воздуха и как продукт, образующийся при брожении, дыхании и т. д. У."бесцветна, имеет слабый запах и слегка … Большая медицинская энциклопедия
УГЛЕКИСЛОТА — УГЛЕКИСЛОТА, углекислоты, мн. нет, жен. (хим.). Двуокись углерода, то же, что углекислый газ. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
УГЛЕКИСЛОТА — УГЛЕКИСЛОТА, ы, жен. Обиходное название двуокиси углерода. | прил. углекислотный, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
УГЛЕКИСЛОТА — неправильное название углерода диоксида … Большой Энциклопедический словарь
УГЛЕКИСЛОТА — (Н2СО3), чрезвычайно слабая кислота, которая образуется при растворении диоксида углерода (СО2) в воде. Она образует два ряда солей карбонаты и гидрокарбонаты. Карбонаты играют важную роль в природе, из них сложены горные породы и раковины… … Научно-технический энциклопедический словарь
Углекислота — ж. разг. Название двуокиси углерода. Толковый словарь Ефремовой. Т. Ф. Ефремова. 2000 … Современный толковый словарь русского языка Ефремовой
углекислота — сущ., кол во синонимов: 1 • углекислый газ (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
углекислота — УГЛЕКИСЛОТА, ы ж Обиходное название двуокиси углерода. Углекислоту используют при изготовлении различных газированных напитков … Толковый словарь русских существительных
dic.academic.ru